Clear Sky Science · zh
Orai1 作为一种新型 Ca2+ 信号开关,通过调控 KLF1 平衡红细胞生成
为何红细胞的分子开关很重要
你的身体每秒钟都会产生数百万个新的红细胞来运输氧气。为了输血、缓解血液短缺以及未来的细胞治疗,科学家们急切希望在实验室中高效培养这些细胞。然而,红细胞成熟的最后阶段出奇地难以控制。本研究揭示了一个隐蔽的分子“调光开关”,它决定了幼稚血细胞是继续发育还是暂停,这为提高体外制备血液的效率并更好理解某些贫血提供了新途径。 
红细胞生长的最后阶段
红细胞起源于逐渐缩小、充填血红蛋白并最终排出细胞核的不成熟前体。这个最后阶段称为终末成熟,由激素促红细胞生成素(erythropoietin)引导,指示细胞何时存活、分裂或特化。名为 KLF1 的关键基因调控因子像主程序一样启动红细胞特异性基因,包括血红蛋白和去核相关基因。然而,促红细胞生成素既能促进也能延缓成熟,它如何在不同阶段时序性地影响 KLF1 活性一直不清楚。
一种在早期放慢成熟的钙通道
作者将注意力集中在钙——一种普遍的信号离子——以及一种叫做 Orai1 的膜通道上,Orai1 允许钙流入细胞。使用人类红系细胞系、脐带血来源的细胞和由多能干细胞培养的红细胞,他们发现幼稚前体细胞表达高水平的 Orai1 并显示强烈的钙内流,而更成熟的细胞则表现出较低的 Orai1 和较弱的钙信号。阻断一般蛋白降解途径的实验表明,随着细胞成熟,Orai1 主要通过自噬–溶酶体途径被清除。在功能层面上,当通过突变体或 CRISPR–Cas9 敲除使 Orai1 失活时,钙内流下降,但 KLF1 水平上升。这促使细胞表达更多红细胞基因、生成更多球蛋白、成熟更快并且去核效率更高。
细胞内开关如何工作
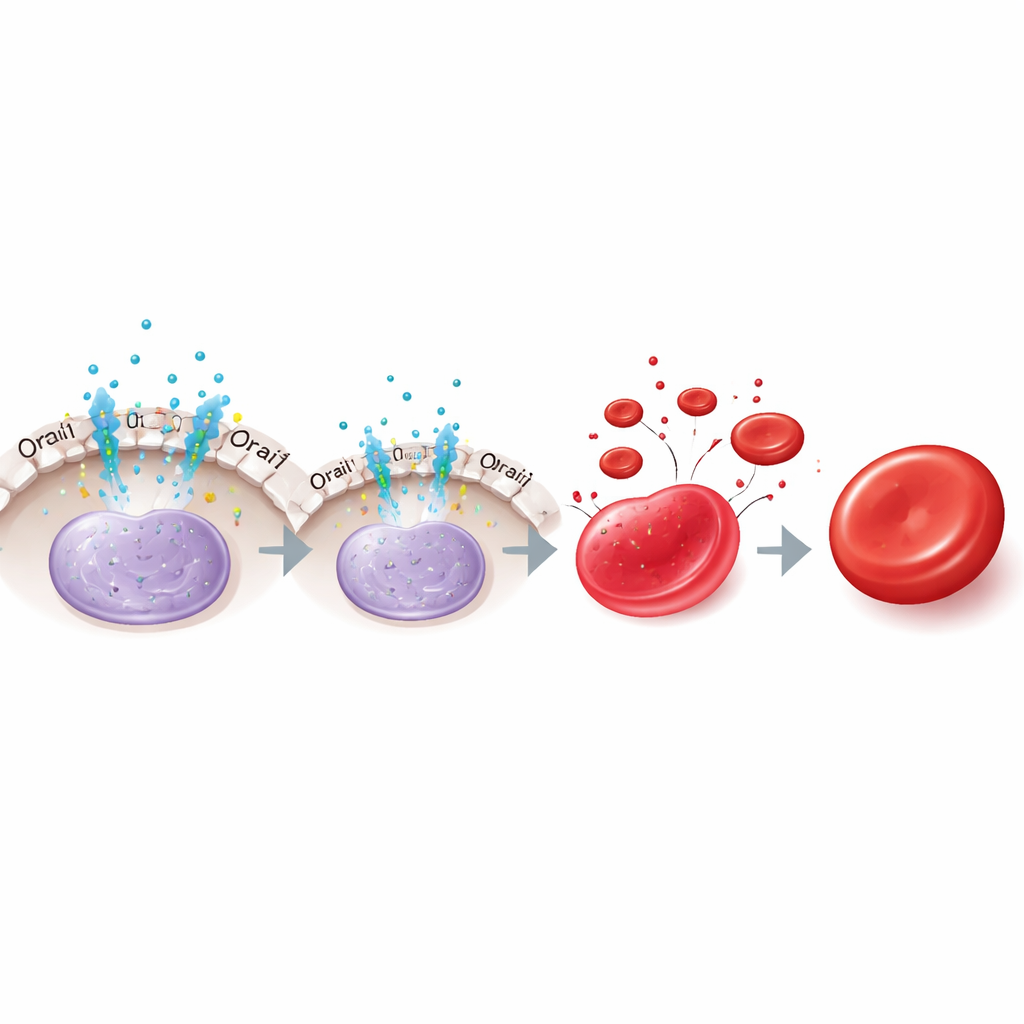
向第二条激素通路的交接
有趣的是,促红细胞生成素的作用会随时间改变。在早期细胞中,去除促红细胞生成素或阻断 Orai1 会增加 KLF1 并加速成熟,这与解除 NFAT2 介导的抑制一致。但在晚期细胞中,去掉促红细胞生成素反而会降低 KLF1 并损害成熟,即便此时抑制 Orai1 已不再起作用。作者将这一晚期对 KLF1 的支持追溯到促红细胞生成素的另一条通路,涉及信号蛋白 STAT5 及其下游伙伴 TAL1 和 DDX5,它们在 Orai1–NFAT2 刹车消失后帮助维持 KLF1。因此,促红细胞生成素先通过 Orai1–NFAT2 抑制 KLF1,随后又通过 STAT5 及其共因子维持 KLF1。
迈向更好的体外培养血液
简单而言,这项工作表明 Orai1 作为一种基于钙的开关,使促红细胞生成素得以微调幼稚红细胞前体何时暂停或继续。当 Orai1 “打开” 时,钙信号激活 NFAT2 以抑制 KLF1 和完全成熟;当 Orai1 “关闭” 时,促红细胞生成素转向 STAT5 路径以维持较高的 KLF1,推动向携氧细胞的最终转变。通过在恰当阶段降低 Orai1 或暂时移除促红细胞生成素,可能更有效地诱导干细胞来源的前体成为功能性、去核的红细胞,这将使用于输血的体外培养血液更接近现实。
引用: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
关键词: 红细胞成熟, 钙信号, Orai1 通道, 促红细胞生成素, KLF1