Clear Sky Science · es
Orai1 actúa como un nuevo interruptor de señal de Ca2+, equilibrando la eritropoyesis mediante la regulación de KLF1
Por qué importa un interruptor molecular para los glóbulos rojos
Cada segundo, tu cuerpo produce millones de glóbulos rojos nuevos para transportar oxígeno. Para transfusiones, la escasez de sangre y futuras terapias celulares, los científicos buscan cultivar estas células con eficiencia en el laboratorio. Sin embargo, los pasos finales de la maduración de los glóbulos rojos son sorprendentemente difíciles de controlar. Este estudio revela un “atenuador” molecular oculto que decide si los precursores sanguíneos jóvenes continúan desarrollándose o se detienen, abriendo nuevas vías para aumentar la producción de sangre en laboratorio y comprender mejor ciertas anemias. 
Los pasos finales del crecimiento de los glóbulos rojos
Los glóbulos rojos nacen de precursores inmaduros que gradualmente se encogen, se llenan de hemoglobina y finalmente expulsan su núcleo. Este tramo final, llamado maduración terminal, está guiado por la hormona eritropoyetina, que indica a las células cuándo sobrevivir, dividirse o especializarse. Un controlador génico clave llamado KLF1 actúa como un programa maestro que activa genes específicos de los glóbulos rojos, incluidos los de la hemoglobina y la enucleación. Sin embargo, la eritropoyetina puede tanto promover como frenar la maduración, y cómo temporiza la actividad de KLF1 en distintas etapas no estaba claro.
Un canal de calcio que ralentiza la maduración temprana
Los autores se centraron en el calcio, un ion de señalización universal, y en un canal de membrana llamado Orai1 que permite la entrada de calcio en las células. Usando líneas celulares eritroides humanas, células derivadas de sangre de cordón y glóbulos rojos cultivados a partir de células madre pluripotentes, encontraron que los precursores jóvenes expresan altos niveles de Orai1 y muestran una entrada de calcio fuerte, mientras que las células más maduras presentan mucho menos Orai1 y señales de calcio débiles. Bloquear la degradación proteica general mostró que Orai1 se elimina principalmente a través de la vía autofagia–lisosoma a medida que las células maduran. Funcionalmente, cuando Orai1 fue inhabilitado por una forma mutante o por la eliminación con CRISPR–Cas9, la entrada de calcio disminuyó, pero los niveles de KLF1 aumentaron. Esto impulsó a las células a expresar más genes de glóbulo rojo, producir más globina, madurar más rápido y enuclearse con mayor eficacia.
Cómo funciona el interruptor dentro de la célula
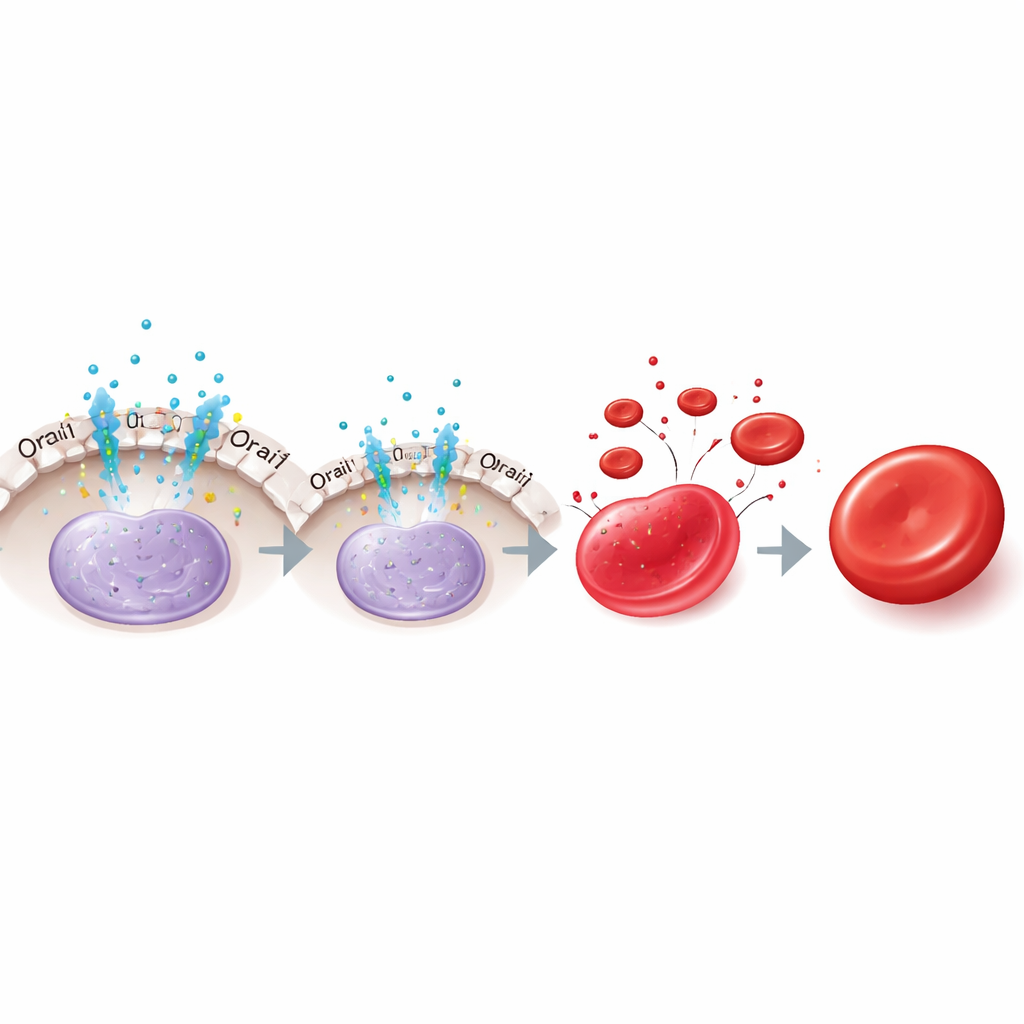
Un traspaso a una segunda vía hormonal
Curiosamente, el papel de la eritropoyetina cambia con el tiempo. En las células tempranas, retirar la eritropoyetina o bloquear Orai1 aumentó KLF1 y aceleró la maduración, coherente con la liberación de la supresión mediada por NFAT2. Pero en células de etapas más avanzadas, quitar la eritropoyetina redujo KLF1 y perjudicó la maduración, aunque la inhibición de Orai1 ya no tenía efecto. Los autores rastrearon este soporte tardío de KLF1 a otra vía de la eritropoyetina que involucra a la proteína de señalización STAT5 y sus colaboradores en aval TAL1 y DDX5, que ayudan a mantener KLF1 una vez que el freno Orai1–NFAT2 ha desaparecido. Así, la eritropoyetina primero restringe KLF1 vía Orai1–NFAT2, y después sostiene KLF1 mediante STAT5 y sus cofactores.
Hacia una mejor sangre cultivada en laboratorio
En términos sencillos, este trabajo muestra que Orai1 funciona como un interruptor basado en calcio que permite a la eritropoyetina afinar cuándo los precursores jóvenes de glóbulos rojos deben detenerse o seguir adelante. Cuando Orai1 está “encendido”, las señales de calcio activan NFAT2 para mantener KLF1 y la maduración completa bajo control; cuando Orai1 está “apagado”, la eritropoyetina cambia a una vía STAT5 que mantiene KLF1 alto y promueve la transformación final en células portadoras de oxígeno. Al disminuir Orai1 o retirar temporalmente la eritropoyetina en la etapa adecuada, podría ser posible inducir a los precursores derivados de células madre a convertirse en glóbulos rojos funcionales y enucleados con mayor eficiencia, acercando la perspectiva de sangre cultivada en laboratorio para transfusiones un paso más hacia la realidad.
Cita: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Palabras clave: maduración de los glóbulos rojos, señalización por calcio, canal Orai1, eritropoyetina, KLF1