Clear Sky Science · sv
Orai1 fungerar som en ny Ca2+-signalknapp, och balanserar erytropoesen genom KLF1-reglering
Varför en molekylär strömbrytare för röda blodkroppar är viktig
Varje sekund producerar din kropp miljontals nya röda blodkroppar för att transportera syre. För transfusioner, blodbrist och framtida cellterapier vill forskare odla dessa celler effektivt i labbet. Ändå är de sista stegen i röda blodkroppars mognad förvånansvärt svåra att styra. Denna studie avslöjar en dold molekylär ”dimmer” som avgör om unga blodceller fortsätter utvecklas eller stannar upp, vilket öppnar nya vägar för att öka produktionen av labbodlat blod och för att bättre förstå vissa anemier. 
De sista stegen i röda blodkroppars tillväxt
Röda blodkroppar uppstår från omogna föregångare som gradvis krymper, fylls med hemoglobin och slutligen kastar ut sin kärna. Denna sista fas, kallad terminal mognad, styrs av hormonet erytropoietin, som signalerar när celler ska överleva, dela sig eller specialisera sig. En nyckelgenreglerare kallad KLF1 fungerar som ett huvudprogram som slår på genuttryck specifikt för röda blodkroppar, inklusive gener för hemoglobin och enukleering. Men erytropoietin kan både främja och bromsa mognaden, och hur det tidställer KLF1-aktivitet i olika stadier har varit oklart.
En kalciumkanal som bromsar tidig mognad
Författarna fokuserade på kalcium, en universell signaljon, och en membrankanalen Orai1 som tillåter kalciumflöde in i celler. Med hjälp av humana erytroida cellinjer, celler från navelsträngsblod och röda blodkroppar odlade från pluripotenta stamceller fann de att unga föregångare uttrycker höga nivåer av Orai1 och uppvisar starkt kalciuminflöde, medan mer mogna celler visar mycket lägre Orai1 och svagare kalciumsignaler. Blockering av generell proteinnedbrytning visade att Orai1 framför allt avlägsnas via en autofagi–lysosom-väg när cellerna mognar. Funktionellt, när Orai1 inaktiverades genom en mutant form eller med CRISPR–Cas9-knockout, föll kalciuminflödet, men nivåerna av KLF1 ökade. Detta fick cellerna att uttrycka fler gener för röda blodkroppar, producera mer globin, mogna snabbare och enukleera mer effektivt.
Hur strömbrytaren fungerar inne i cellen
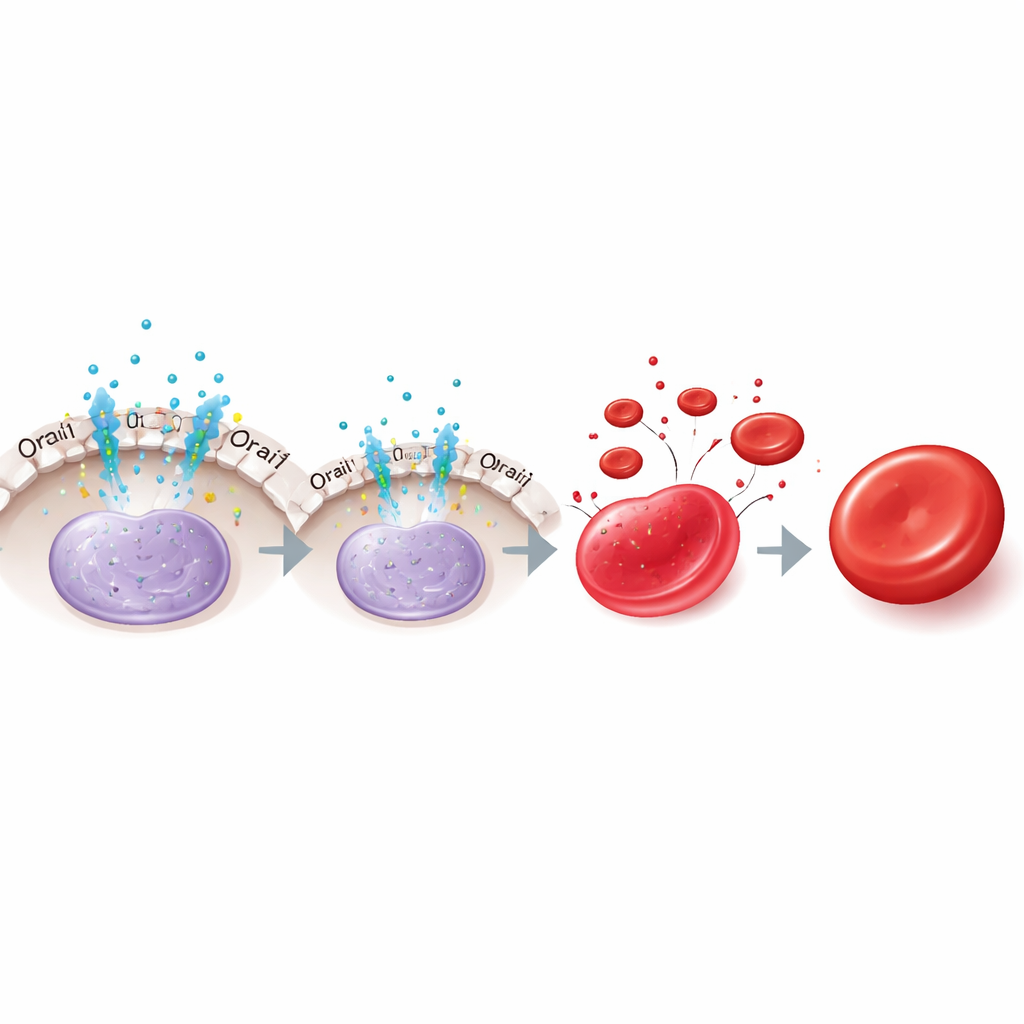
En överlämning till en andra hormonväg
Intressant nog ändras erytropoietins roll över tiden. I tidiga celler ökade borttagning av erytropoietin eller blockering av Orai1 KLF1 och påskyndade mognaden, vilket stämmer med lättnad från NFAT2-medierad suppression. Men i senare stadier minskade borttagning av erytropoietin istället KLF1 och försämrade mognaden, även om inhibering av Orai1 inte längre hade någon effekt. Författarna spårade detta sena stöd för KLF1 till en annan erytropoietinväg som involverar signalproteinet STAT5 och dess nedströms partners TAL1 och DDX5, vilka hjälper till att upprätthålla KLF1 när Orai1–NFAT2-bromsen har avtatt. Således hämmar erytropoietin först KLF1 via Orai1–NFAT2, för att senare understödja KLF1 genom STAT5 och dess medhjälpare.
Mot bättre labbodlat blod
Enkelt uttryckt visar detta arbete att Orai1 fungerar som en kalciumbaserad strömbrytare som tillåter erytropoietin att finsjustera när unga föregångare till röda blodkroppar ska pausa eller fortsätta. När Orai1 är “på” aktiverar kalciumsignaler NFAT2 för att hålla KLF1 och full mognad tillbaka; när Orai1 är “av” växlar erytropoietin till en STAT5-väg som håller KLF1 högt och driver den slutliga omvandlingen till syretransporterande celler. Genom att dämpa Orai1 eller tillfälligt ta bort erytropoietin i rätt stadium kan det bli möjligt att få stamcells‑härledda föregångare att bli funktionella, enukleerade röda blodkroppar mer effektivt, vilket förflyttar utsikten om labbodlat blod för transfusioner ett steg närmare verklighet.
Citering: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Nyckelord: mognad av röda blodkroppar, calciumsignalering, Orai1-kanal, erytropoietin, KLF1