Clear Sky Science · pl
Orai1 działa jako nowy przełącznik sygnału Ca2+, równoważąc erytropoezę przez regulację KLF1
Dlaczego molekularny przełącznik dla erytrocytów ma znaczenie
Co sekundę w twoim ciele powstają miliony nowych czerwonych krwinek przenoszących tlen. W kontekście transfuzji, niedoborów krwi i przyszłych terapii komórkowych naukowcy chcą wydajnie hodować te komórki w laboratorium. Mimo to końcowe etapy dojrzewania erytrocytów są zaskakująco trudne do kontrolowania. To badanie ujawnia ukryty molekularny „ściemniacz”, który decyduje, czy młode komórki krwi kontynuują rozwój, czy robią przerwę, otwierając nowe możliwości zwiększenia produkcji krwi w laboratorium i lepszego zrozumienia niektórych anemii. 
Końcowe etapy wzrostu czerwonych krwinek
Czerwone krwinki powstają z niedojrzałych prekursorów, które stopniowo zmniejszają objętość, wypełniają się hemoglobiną i w końcu pozbywają się jądra komórkowego. Ten ostatni etap, nazywany dojrzewaniem terminalnym, jest kierowany przez hormon erytropoetynę, która mówi komórkom, kiedy przetrwać, dzielić się lub specjalizować. Kluczowy regulator genowy o nazwie KLF1 działa jak główny program włączający geny specyficzne dla erytrocytów, w tym te odpowiedzialne za hemoglobinę i enukleację. Jednak erytropoetyna może zarówno przyspieszać, jak i hamować dojrzewanie, a to, jak reguluje aktywność KLF1 na różnych etapach, pozostawało niejasne.
Kanał wapniowy, który spowalnia wczesne dojrzewanie
Autorzy skupili się na wapniu, uniwersalnym kationie sygnałowym, oraz na kanale błonowym o nazwie Orai1, który umożliwia napływ wapnia do komórek. Na ludzkich liniach erytroidalnych, komórkach pochodzących z krwi pępowinowej oraz erytrocytach wyhodowanych ze zróżnicowanych komórek macierzystych pluripotentnych stwierdzili, że młode prekursory wykazują wysoką ekspresję Orai1 i silny napływ Ca2+, podczas gdy bardziej dojrzałe komórki mają znacznie niższy poziom Orai1 i słabsze sygnały wapniowe. Blokada ogólnego rozkładu białek pokazała, że Orai1 jest usuwany głównie przez szlak autofagia–lizosom w miarę dojrzewania komórek. Funkcjonalnie, gdy Orai1 był unieruchomiony przez formę mutantną lub przez knockout CRISPR–Cas9, napływ wapnia malał, ale poziomy KLF1 rosły. Skłoniło to komórki do zwiększonej ekspresji genów erytrocytarnych, wytwarzania większej ilości globiny, szybszego dojrzewania i efektywniejszej enukleacji.
Jak przełącznik działa wewnątrz komórki
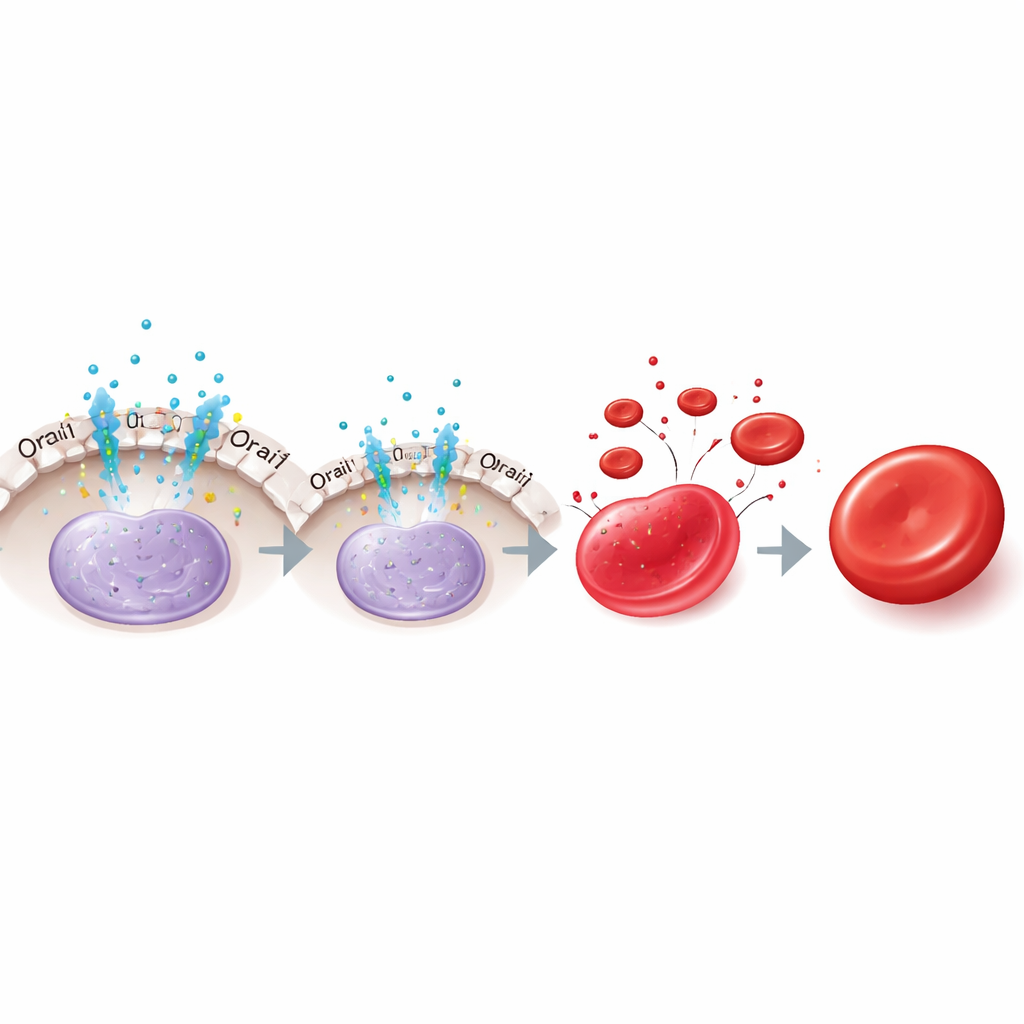
Przekazanie pałeczki do drugiej ścieżki hormonalnej
Ciekawie, rola erytropoetyny zmienia się w czasie. W komórkach we wczesnym stadium usunięcie erytropoetyny lub zablokowanie Orai1 zwiększało KLF1 i przyspieszało dojrzewanie, zgodnie z ustąpieniem tłumienia przez NFAT2. Jednak w późniejszych stadiach pozbawienie erytropoetyny obniżało KLF1 i upośledzało dojrzewanie, mimo że inhibicja Orai1 nie miała już efektu. Autorzy powiązali to późne wsparcie KLF1 z inną ścieżką erytropoetyny obejmującą białko sygnalizacyjne STAT5 oraz jego następców TAL1 i DDX5, którzy pomagają utrzymać KLF1 po zaniknięciu hamulca Orai1–NFAT2. Tak więc erytropoetyna najpierw hamuje KLF1 przez Orai1–NFAT2, a później podtrzymuje KLF1 poprzez STAT5 i jego kofaktory.
W kierunku lepszej krwi hodowanej w laboratorium
Prosto mówiąc, praca ta pokazuje, że Orai1 pełni rolę przełącznika opartego na wapniu, który pozwala erytropoetynie precyzyjnie dostosować moment, kiedy młode prekursory erytrocytów powinny się zatrzymać lub iść dalej. Gdy Orai1 jest „włączony”, sygnały wapniowe aktywują NFAT2, aby utrzymywać KLF1 i hamować pełne dojrzewanie; gdy Orai1 jest „wyłączony”, erytropoetyna przełącza się na ścieżkę STAT5, która utrzymuje wysoki poziom KLF1 i napędza końcową przemianę w komórki przenoszące tlen. Poprzez przyciszenie Orai1 lub tymczasowe usunięcie erytropoetyny na odpowiednim etapie, może być możliwe skłonienie prekursorów pochodzących z komórek macierzystych do wydajniejszego stawania się funkcjonalnymi, enukleowanymi krwinkami czerwonymi, co przybliża perspektywę hodowanej w laboratorium krwi do zastosowań transfuzjologicznych.
Cytowanie: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Słowa kluczowe: dojrzewanie czerwonych krwinek, sygnalizacja wapniowa, kanał Orai1, erytropoetyna, KLF1