Clear Sky Science · pt
Orai1 age como um novo interruptor de sinal de Ca2+, equilibrando a eritropoiese via regulação de KLF1
Por que um interruptor molecular para glóbulos vermelhos importa
Cada segundo, seu corpo produz milhões de novos glóbulos vermelhos para transportar oxigênio. Para transfusões, diante de faltas de sangue e para futuras terapias celulares, cientistas buscam cultivar essas células de forma eficiente em laboratório. Ainda assim, os passos finais da maturação dos glóbulos vermelhos são surpreendentemente difíceis de controlar. Este estudo revela um “dimmer” molecular oculto que decide se as células sanguíneas jovens continuam a se desenvolver ou fazem uma pausa, abrindo novas possibilidades para aumentar a produção de sangue em laboratório e entender melhor certas anemias. 
Os passos finais do crescimento dos glóbulos vermelhos
Os glóbulos vermelhos nascem de precursores imaturos que gradualmente encolhem, se enchem de hemoglobina e finalmente expulsam o núcleo. Esse trecho final, chamado maturação terminal, é guiado pelo hormônio eritropoietina, que informa às células quando sobreviver, dividir-se ou se especializar. Um controlador gênico chave chamado KLF1 atua como um programa mestre que liga genes específicos dos glóbulos vermelhos, incluindo os envolvidos na hemoglobina e na enucleação. No entanto, a eritropoietina pode tanto promover quanto retardar a maturação, e como ela temporiza a atividade de KLF1 em diferentes estágios permanecia pouco claro.
Um canal de cálcio que retarda a maturação precoce
Os autores se concentraram no cálcio, um íon de sinalização universal, e em um canal de membrana chamado Orai1 que permite a entrada de cálcio nas células. Usando linhagens celulares eritroides humanas, células derivadas de sangue do cordão umbilical e glóbulos vermelhos cultivados a partir de células-tronco pluripotentes, eles descobriram que precursores jovens expressam níveis altos de Orai1 e apresentam forte entrada de cálcio, enquanto células mais maduras exibem Orai1 muito mais baixo e sinais de cálcio mais fracos. Bloquear a degradação proteica geral mostrou que Orai1 é removido principalmente via autófago–lisossomo conforme as células amadurecem. Funcionalmente, quando Orai1 foi desativado por uma forma mutante ou por knockout com CRISPR–Cas9, a entrada de cálcio caiu, mas os níveis de KLF1 aumentaram. Isso impulsionou as células a expressar mais genes de glóbulos vermelhos, produzir mais globina, amadurecer mais rápido e enuclear com maior eficiência.
Como o interruptor funciona dentro da célula
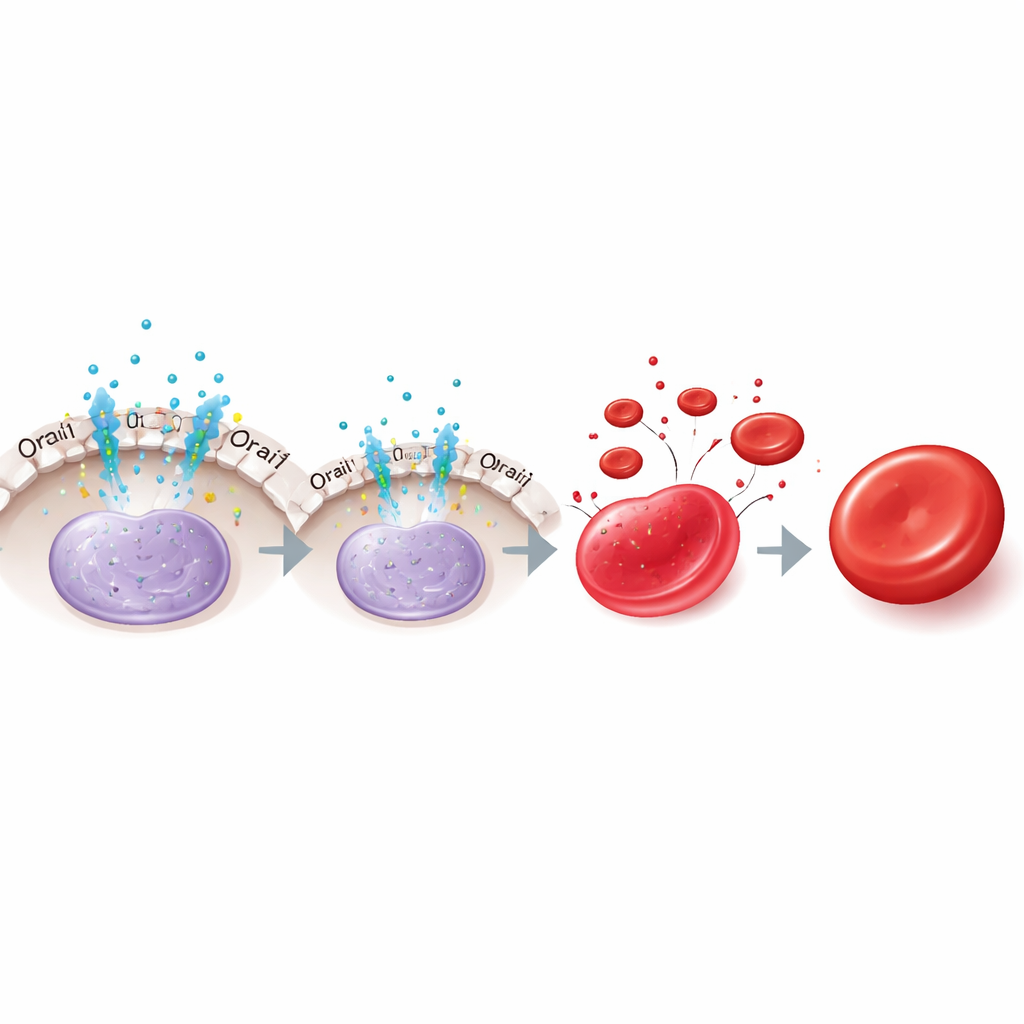
Uma passagem para uma segunda via hormonal
Curiosamente, o papel da eritropoietina muda ao longo do tempo. Em células precoces, remover a eritropoietina ou bloquear Orai1 aumentou KLF1 e acelerou a maturação, consistente com o alívio da supressão mediada por NFAT2. Mas em células em estágio mais avançado, a retirada da eritropoietina reduziu KLF1 e prejudicou a maturação, mesmo que a inibição de Orai1 não tivesse mais efeito. Os autores rastrearam esse suporte tardio a KLF1 para outra via da eritropoietina envolvendo a proteína de sinalização STAT5 e seus parceiros a jusante TAL1 e DDX5, que ajudam a manter KLF1 once o freio Orai1–NFAT2 tenha desaparecido. Assim, a eritropoietina primeiro restringe KLF1 via Orai1–NFAT2 e, mais tarde, sustenta KLF1 por meio de STAT5 e seus cofatores.
Rumo a um sangue cultivado em laboratório melhor
Em termos simples, este trabalho mostra que Orai1 funciona como um interruptor baseado em cálcio que permite à eritropoietina ajustar quando precursores jovens de glóbulos vermelhos devem pausar ou prosseguir. Quando Orai1 está “ligado”, sinais de cálcio ativam NFAT2 para manter KLF1 e a maturação completa sob controle; quando Orai1 está “desligado”, a eritropoietina muda para a via STAT5 que mantém KLF1 elevado e impulsiona a transformação final em células transportadoras de oxigênio. Ao reduzir Orai1 ou remover temporariamente a eritropoietina no estágio certo, pode ser possível induzir precursores derivados de células-tronco a se tornarem glóbulos vermelhos funcionalmente enucleados de forma mais eficiente, aproximando a perspectiva de sangue cultivado em laboratório para transfusões de uma etapa mais próxima da realidade.
Citação: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Palavras-chave: maturação de glóbulos vermelhos, sinalização por cálcio, canal Orai1, eritropoietina, KLF1