Clear Sky Science · de
Orai1 wirkt als neuartiger Ca2+-Signalschalter und balanciert die Erythropoese über KLF1-Regulation
Warum ein molekularer Schalter für rote Blutkörperchen wichtig ist
Jede Sekunde produziert Ihr Körper Millionen neuer roter Blutkörperchen, die Sauerstoff transportieren. Für Transfusionen, Blutknappheit und künftige Zelltherapien möchten Forschende diese Zellen effizient im Labor züchten. Doch die letzten Schritte der Reifung roter Blutkörperchen sind überraschend schwer zu steuern. Diese Studie offenbart einen verborgenen molekularen „Dimmerschalter“, der bestimmt, ob junge Blutzellen weiterreifen oder pausieren, und eröffnet neue Wege, die Herstellung von im Labor erzeugtem Blut zu verbessern und bestimmte Anämien besser zu verstehen. 
Die letzten Schritte des Wachstums roter Blutkörperchen
Rote Blutkörperchen entstehen aus unreifen Vorläuferzellen, die allmählich schrumpfen, sich mit Hämoglobin füllen und schließlich ihren Zellkern ausstoßen. Dieser letzte Abschnitt, die terminale Reifung, wird durch das Hormon Erythropoietin gesteuert, das den Zellen signalisiert, wann sie überleben, sich teilen oder sich spezialisieren sollen. Ein Schlüsselregulator namens KLF1 fungiert wie ein Masterprogramm, das erythrozytenspezifische Gene einschaltet, einschließlich jener für Hämoglobin und Enukleation. Allerdings kann Erythropoietin sowohl die Reifung fördern als auch verlangsamen, und wie es die KLF1-Aktivität in verschiedenen Stadien zeitlich steuert, war bisher unklar.
Ein Calciumkanal, der frühe Reifung verlangsamt
Die Autoren konzentrierten sich auf Calcium, ein universelles Signalmolekül, und auf einen Membrankanals namens Orai1, der Calcium in Zellen einströmen lässt. Mit menschlichen erythroiden Zelllinien, aus Nabelschnurblut gewonnenen Zellen und aus pluripotenten Stammzellen gezüchteten roten Blutkörperchen fanden sie, dass junge Vorläufer hohe Orai1-Spiegel und starke Calcium-Einstromantworten zeigen, während reifere Zellen deutlich weniger Orai1 und schwächere Calcium-Signale aufweisen. Das Blockieren allgemeiner Proteinabbaumechanismen zeigte, dass Orai1 beim Reifen vor allem über einen Autophagie–Lysosom-Weg entfernt wird. Funktionell führte das Ausschalten von Orai1, entweder durch eine mutierte Form oder durch CRISPR–Cas9-Knockout, zu reduziertem Calcium-Einstrom, während KLF1-Spiegel stiegen. Dadurch schalteten die Zellen mehr erythrozytenspezifische Gene ein, produzierten mehr Globin, reiften schneller und enukleierten effizienter.
Wie der Schalter innerhalb der Zelle funktioniert
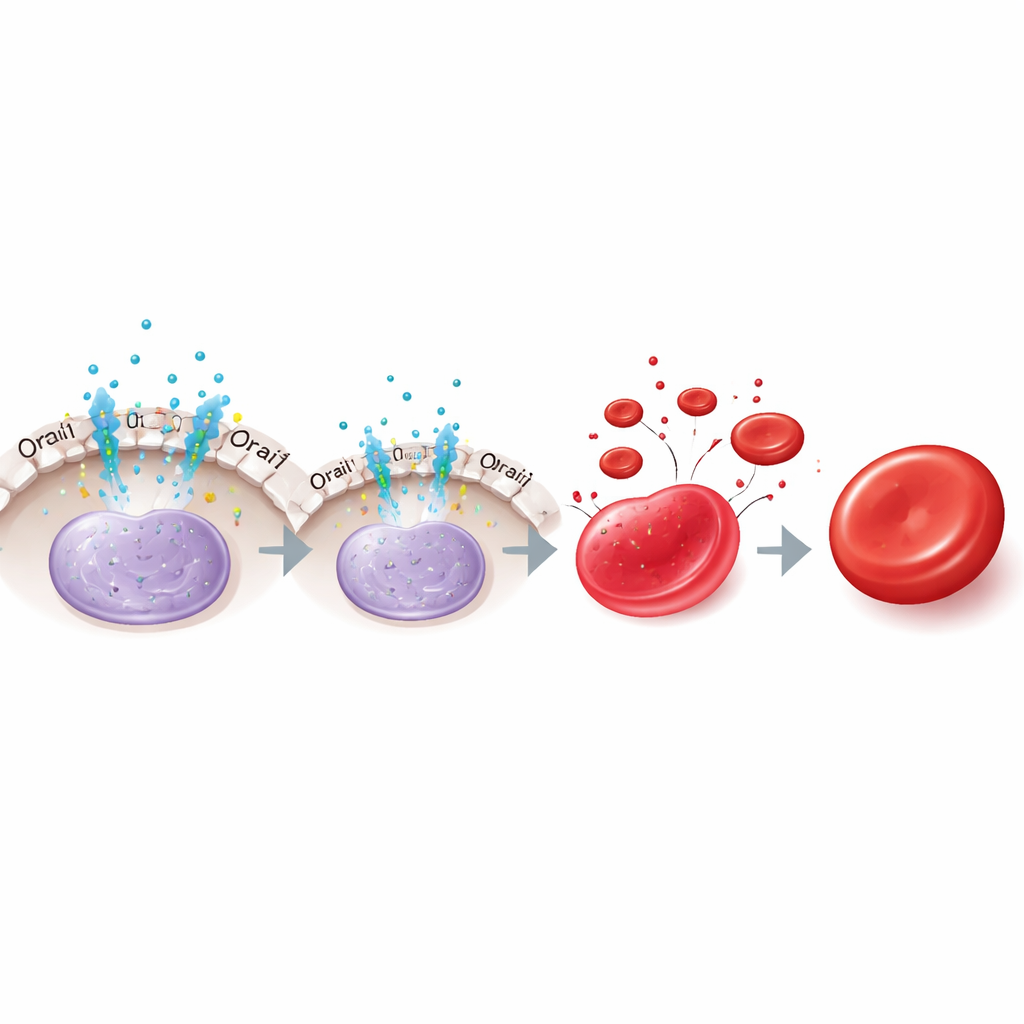
Ein Übergang zu einem zweiten Hormonweg
Interessanterweise ändert sich die Rolle von Erythropoietin im Verlauf der Reifung. In frühen Zellen führte das Entfernen von Erythropoietin oder die Blockade von Orai1 zu erhöhtem KLF1 und beschleunigter Reifung, was mit der Aufhebung der NFAT2-vermittelten Unterdrückung übereinstimmt. In späteren Stadien hingegen reduzierte das Wegnehmen von Erythropoietin nun KLF1 und beeinträchtigte die Reifung, obwohl die Orai1-Hemmung keine Wirkung mehr zeigte. Die Autoren führten diese späte Unterstützung von KLF1 auf einen anderen Erythropoietin-vermittelten Weg zurück, der das Signalmolekül STAT5 und dessen nachgeschaltete Partner TAL1 und DDX5 umfasst, die helfen, KLF1 aufrechtzuerhalten, sobald die Orai1–NFAT2-Bremse abgeklungen ist. Somit hemmt Erythropoietin zunächst KLF1 über Orai1–NFAT2 und unterstützt es später über STAT5 und seine Ko-Faktoren.
Auf dem Weg zu besserem im Labor gezüchtetem Blut
Einfach ausgedrückt zeigt diese Arbeit, dass Orai1 als calciumbasierter Schalter fungiert, der Erythropoietin erlaubt, fein zu steuern, wann junge Vorläufer roter Blutkörperchen pausieren oder fortschreiten sollen. Wenn Orai1 „an“ ist, aktivieren Calcium-Signale NFAT2, um KLF1 und die vollständige Reifung in Schach zu halten; wenn Orai1 „aus“ ist, schaltet Erythropoietin auf einen STAT5-Weg um, der KLF1 hoch hält und die abschließende Umwandlung in sauerstofftransportierende Zellen vorantreibt. Durch gezieltes Herunterregeln von Orai1 oder das vorübergehende Entfernen von Erythropoietin zum richtigen Zeitpunkt könnte man Vorläufer aus Stammzellen effizienter dazu bringen, funktionelle, enukleierte rote Blutkörperchen zu werden, was die Aussicht auf im Labor erzeugtes Blut für Transfusionen einen Schritt näher an die Realität rückt.
Zitation: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Schlüsselwörter: Reifung roter Blutkörperchen, Calcium-Signalübertragung, Orai1-Kanal, Erythropoietin, KLF1