Clear Sky Science · fr
Orai1 agit comme un nouvel interrupteur de signal Ca2+, équilibrant l’érythropoïèse via la régulation de KLF1
Pourquoi un commutateur moléculaire pour les globules rouges importe
Chaque seconde, votre corps produit des millions de nouveaux globules rouges pour transporter l’oxygène. Pour les transfusions, les pénuries de sang et les futures thérapies cellulaires, les chercheurs veulent cultiver ces cellules efficacement en laboratoire. Pourtant, les étapes finales de la maturation des globules rouges sont étonnamment difficiles à contrôler. Cette étude révèle un « variateur » moléculaire caché qui décide si les jeunes cellules sanguines continuent de se développer ou font une pause, ouvrant de nouvelles voies pour augmenter la production de sang en laboratoire et mieux comprendre certaines anémies. 
Les étapes finales de la croissance des globules rouges
Les globules rouges naissent de précurseurs immatures qui rétrécissent progressivement, se remplissent d’hémoglobine et expulsent finalement leur noyau. Cette dernière phase, appelée maturation terminale, est guidée par l’hormone érythropoïétine, qui indique aux cellules quand survivre, se diviser ou se spécialiser. Un contrôleur génétique clé nommé KLF1 joue le rôle d’un programme maître qui active les gènes spécifiques des globules rouges, y compris ceux de l’hémoglobine et de l’exnucléation. Cependant, l’érythropoïétine peut à la fois favoriser et ralentir la maturation, et la façon dont elle module l’activité de KLF1 à différents stades restait floue.
Un canal calcique qui ralentit la maturation précoce
Les auteurs se sont concentrés sur le calcium, ion de signalisation universel, et sur un canal membranaire appelé Orai1 qui permet l’entrée de calcium dans les cellules. En utilisant des lignées cellulaires érythroïdes humaines, des cellules dérivées de sang de cordon et des globules rouges cultivés à partir de cellules souches pluripotentes, ils ont constaté que les précurseurs jeunes expriment des niveaux élevés d’Orai1 et présentent une forte entrée calcique, tandis que les cellules plus matures montrent des niveaux beaucoup plus faibles d’Orai1 et des signaux calciques atténués. Le blocage de la dégradation protéique générale a montré que Orai1 est éliminé principalement via la voie autophagie–lysosome au fur et à mesure de la maturation. Fonctionnellement, lorsque Orai1 était inactivé par une forme mutante ou par un knock-out CRISPR–Cas9, l’entrée calcique diminuait, mais les niveaux de KLF1 augmentaient. Ceci poussait les cellules à exprimer davantage de gènes des globules rouges, à produire plus de globine, à maturer plus rapidement et à exnucléer plus efficacement.
Comment le commutateur fonctionne à l’intérieur de la cellule
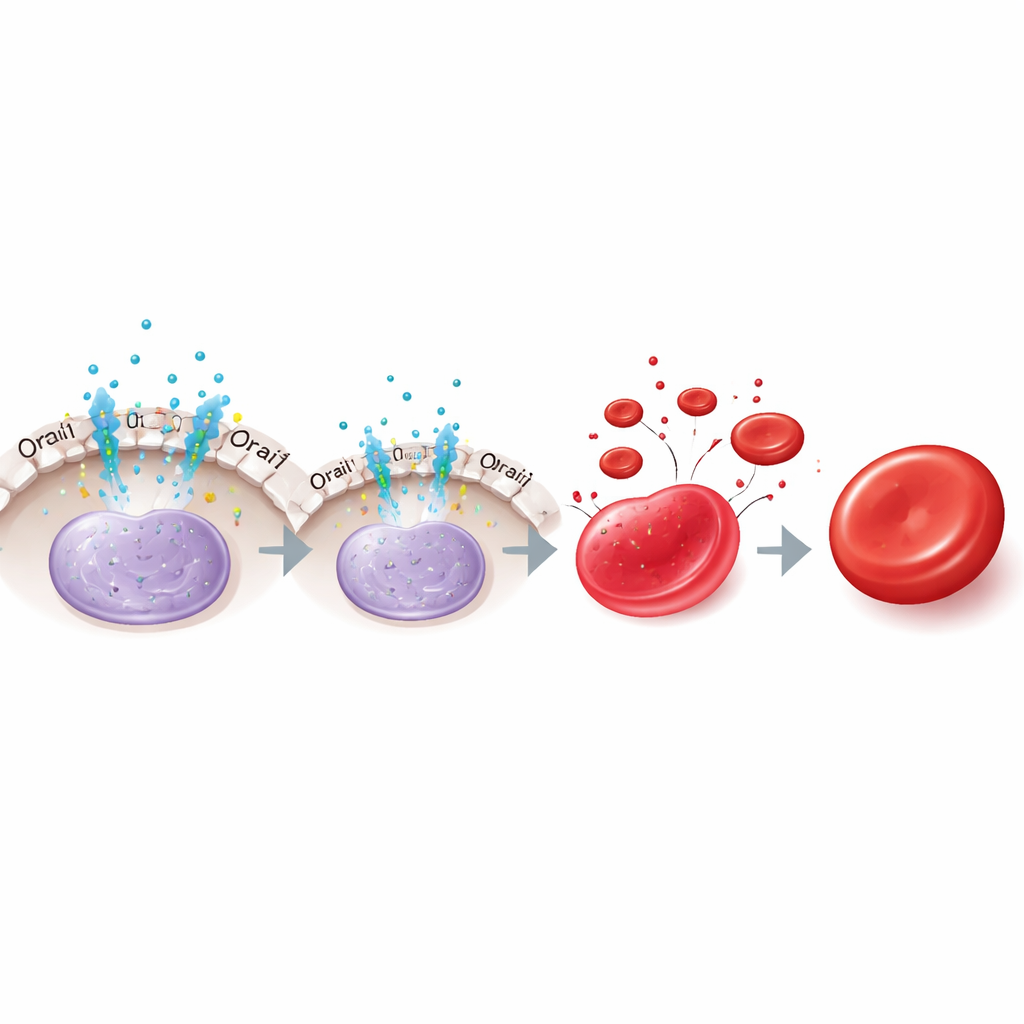
Un relais vers une seconde voie hormonale
Fait intéressant, le rôle de l’érythropoïétine change avec le temps. Dans les cellules précoces, la suppression de l’érythropoïétine ou le blocage d’Orai1 augmentait KLF1 et accélèrait la maturation, cohérent avec la levée de la répression médiée par NFAT2. Mais aux stades plus avancés, la suppression de l’érythropoïétine réduisait maintenant KLF1 et entravait la maturation, même si l’inhibition d’Orai1 n’avait plus d’effet. Les auteurs ont attribué ce soutien tardif de KLF1 à une autre voie de l’érythropoïétine impliquant la protéine de signalisation STAT5 et ses partenaires en aval TAL1 et DDX5, qui contribuent à maintenir KLF1 une fois que le frein Orai1–NFAT2 s’est estompé. Ainsi, l’érythropoïétine freine d’abord KLF1 via Orai1–NFAT2, puis soutient plus tard KLF1 via STAT5 et ses cofacteurs.
Vers un meilleur sang cultivé en laboratoire
En termes simples, ce travail montre que Orai1 fonctionne comme un commutateur calcique qui permet à l’érythropoïétine d’ajuster précisément le moment où les précurseurs jeunes des globules rouges doivent faire une pause ou avancer. Quand Orai1 est « activé », les signaux calciques activent NFAT2 pour maintenir KLF1 et freiner la maturation complète ; quand Orai1 est « désactivé », l’érythropoïétine bascule vers la voie STAT5 qui maintient KLF1 élevé et conduit la transformation finale en cellules porteuses d’oxygène. En diminuant Orai1 ou en supprimant temporairement l’érythropoïétine au bon stade, il pourrait être possible d’encourager les précurseurs dérivés de cellules souches à devenir plus efficacement des globules rouges fonctionnels et exnucléés, rapprochant la perspective du sang cultivé en laboratoire pour les transfusions d’une étape vers la réalité.
Citation: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Mots-clés: maturation des globules rouges, signalisation calcique, canal Orai1, érythropoïétine, KLF1