Clear Sky Science · nl
Orai1 functioneert als een nieuw Ca2+-signaalschakelaar en balanceert erytropoëse via KLF1-regulatie
Waarom een moleculaire schakelaar voor rode bloedcellen belangrijk is
Elke seconde produceert uw lichaam miljoenen nieuwe rode bloedcellen om zuurstof te vervoeren. Voor transfusies, bloedtekorten en toekomstige celtherapieën proberen wetenschappers deze cellen efficiënt in het laboratorium te kweken. Toch zijn de laatste stappen van de rijping van rode bloedcellen verrassend moeilijk te sturen. Deze studie onthult een verborgen moleculaire “dimknop” die bepaalt of jonge bloedcellen blijven ontwikkelen of pauzeren, en opent nieuwe mogelijkheden om de productie van in het lab gemaakte bloed te verbeteren en bepaalde vormen van anemie beter te begrijpen. 
De laatste fasen van de groei van rode bloedcellen
Rode bloedcellen ontstaan uit onrijpe voorlopercellen die geleidelijk krimpen, zich met hemoglobine vullen en uiteindelijk hun kern uitdrijven. Deze laatste fase, terminale rijping genoemd, wordt gestuurd door het hormoon erytropoëtine, dat cellen signaleert om te overleven, zich te delen of te differentiëren. Een belangrijke genregelaar genaamd KLF1 werkt als een masterprogramma dat roodbloedcel-specifieke genen activeert, waaronder die voor hemoglobine en enucleatie. Erytropoëtine kan echter zowel de rijping bevorderen als vertragen, en hoe het de timing van KLF1-activiteit in verschillende stadia regelt, was onduidelijk.
Een calciumkanaal dat vroege rijping vertraagt
De auteurs richtten zich op calcium, een universeel signaalion, en een membraankanaal genaamd Orai1 waardoor calcium cellen binnenstroomt. Met menselijke erytroïde cellijnen, uit navelstrengbloed afkomstige cellen en rode bloedcellen gekweekt uit pluripotente stamcellen, vonden ze dat jonge voorlopercellen hoge niveaus van Orai1 tot expressie brengen en sterke calciuminstromen vertonen, terwijl rijpere cellen veel lagere Orai1-waarden en zwakkere calciumsignalen laten zien. Het blokkeren van algemene eiwitafbraak liet zien dat Orai1 tijdens de rijping voornamelijk via het autophagie–lysosoompad wordt verwijderd. Functioneel gezien, wanneer Orai1 werd uitgeschakeld door een mutant of door CRISPR–Cas9-knockout, daalde de calciuminflux, maar steeg het KLF1‑niveau. Dit zette de cellen ertoe aan meer roodbloedcelgenen tot expressie te brengen, meer globine te maken, sneller te rijpen en efficiënter te enucleëren.
Hoe de schakelaar binnenin de cel werkt
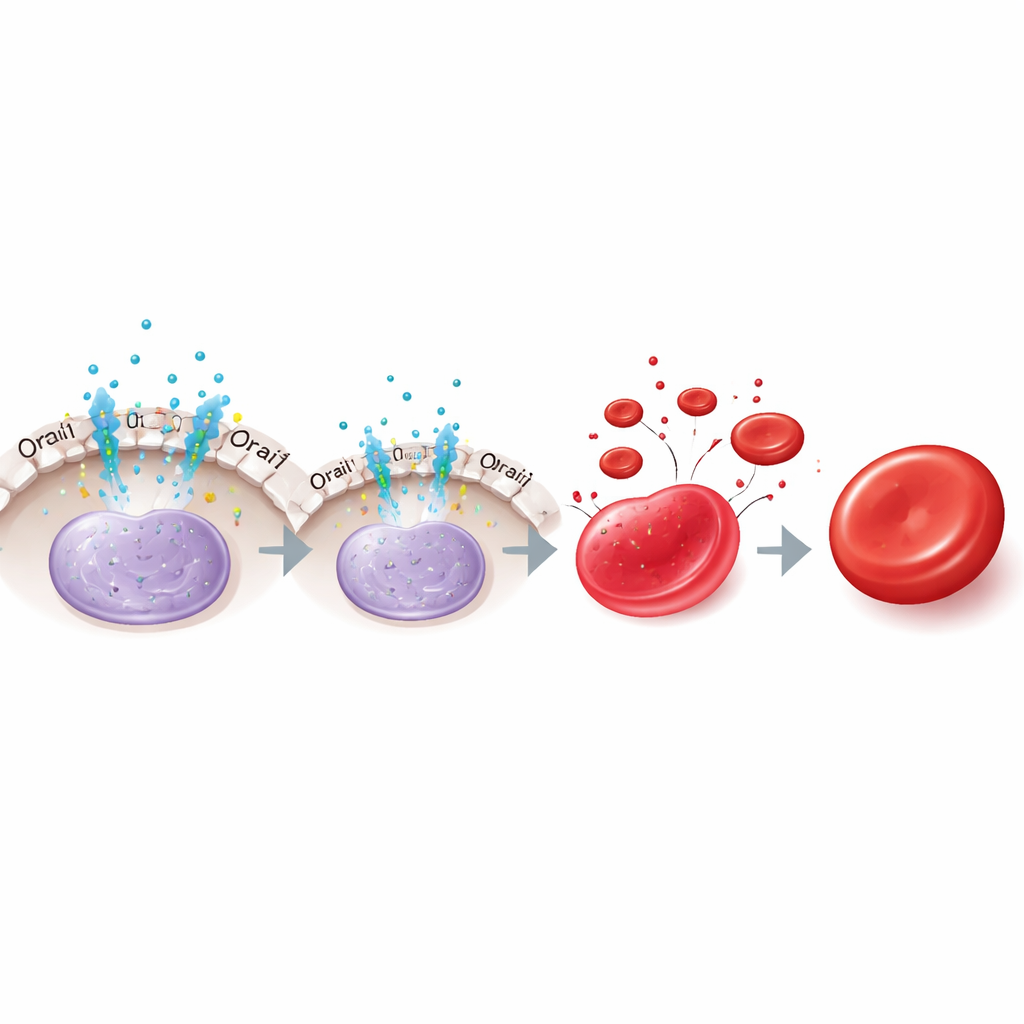
Een overdracht naar een tweede hormoonpad
Interessant genoeg verandert de rol van erytropoëtine in de tijd. In vroege cellen leidde het weghalen van erytropoëtine of het blokkeren van Orai1 tot een toename van KLF1 en versnelde rijping, wat in overeenstemming is met het opheffen van NFAT2‑gemedieerde suppressie. Maar in latere stadia resulteerde het weghalen van erytropoëtine juist in een vermindering van KLF1 en verslechterde rijping, hoewel Orai1‑remming toen geen effect meer had. De auteurs herkenden deze late ondersteuning van KLF1 in een ander erytropoëtinepad met de signaalproteïne STAT5 en diens downstreampartners TAL1 en DDX5, die helpen KLF1 te behouden zodra de Orai1–NFAT2‑rem is verdwenen. Zo remt erytropoëtine eerst KLF1 via Orai1–NFAT2 en onderhoudt het later KLF1 via STAT5 en zijn cofactoren.
Op weg naar beter in het lab gekweekt bloed
In eenvoudige bewoordingen laat dit werk zien dat Orai1 functioneert als een calciumafhankelijke schakelaar waarmee erytropoëtine nauwkeurig kan afstemmen wanneer jonge roodbloedcelvoorlopers moeten pauzeren of doorgaan. Als Orai1 “aan” staat, activeren calciumsignalen NFAT2 om KLF1 en volledige rijping in toom te houden; als Orai1 “uit” staat, schakelt erytropoëtine over op een STAT5‑route die KLF1 hoog houdt en de uiteindelijke transformatie naar zuurstofdragende cellen stimuleert. Door Orai1 omlaag te brengen of erytropoëtine tijdelijk op het juiste moment weg te nemen, zou het mogelijk zijn om stamcel‑afgeleide voorlopercellen efficiënter te laten uitrijpen tot functionele, enucleërende rode bloedcellen, waardoor de mogelijkheid van in het lab geproduceerd bloed voor transfusies een stap dichterbij komt.
Bronvermelding: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Trefwoorden: rijping van rode bloedcellen, calciumsignaalverlening, Orai1-kanaal, erytropoëtine, KLF1