Clear Sky Science · ar
يعمل Orai1 كمفتاح إشارة Ca2+ جديد، موازنًا لتكوين كريات الدم الحمراء عبر تنظيم KLF1
لماذا يهم وجود مفتاح جزيئي لكريات الدم الحمراء
تنتج أجسامنا ملايين خلايا الدم الحمراء الجديدة كل ثانية لحمل الأكسجين. ولأجل عمليات النقل ونقص الإمدادات والعلاجات الخلوية المستقبلية، يسعى العلماء إلى زراعة هذه الخلايا بكفاءة في المختبر. ومع ذلك، فإن المراحل النهائية لنضج كريات الدم الحمراء صعبة الضبط بشكل مدهش. تكشف هذه الدراسة عن "مفتاح تعتيم" جزيئي مخفي يقرر ما إذا كانت الخلايا الدموية الشابة ستستمر في التطور أم تتوقف، ويفتح طرقًا جديدة لتعزيز إنتاج الدم المصنع مختبريًا وفهم أنواع معينة من الأنيميا بشكل أفضل. 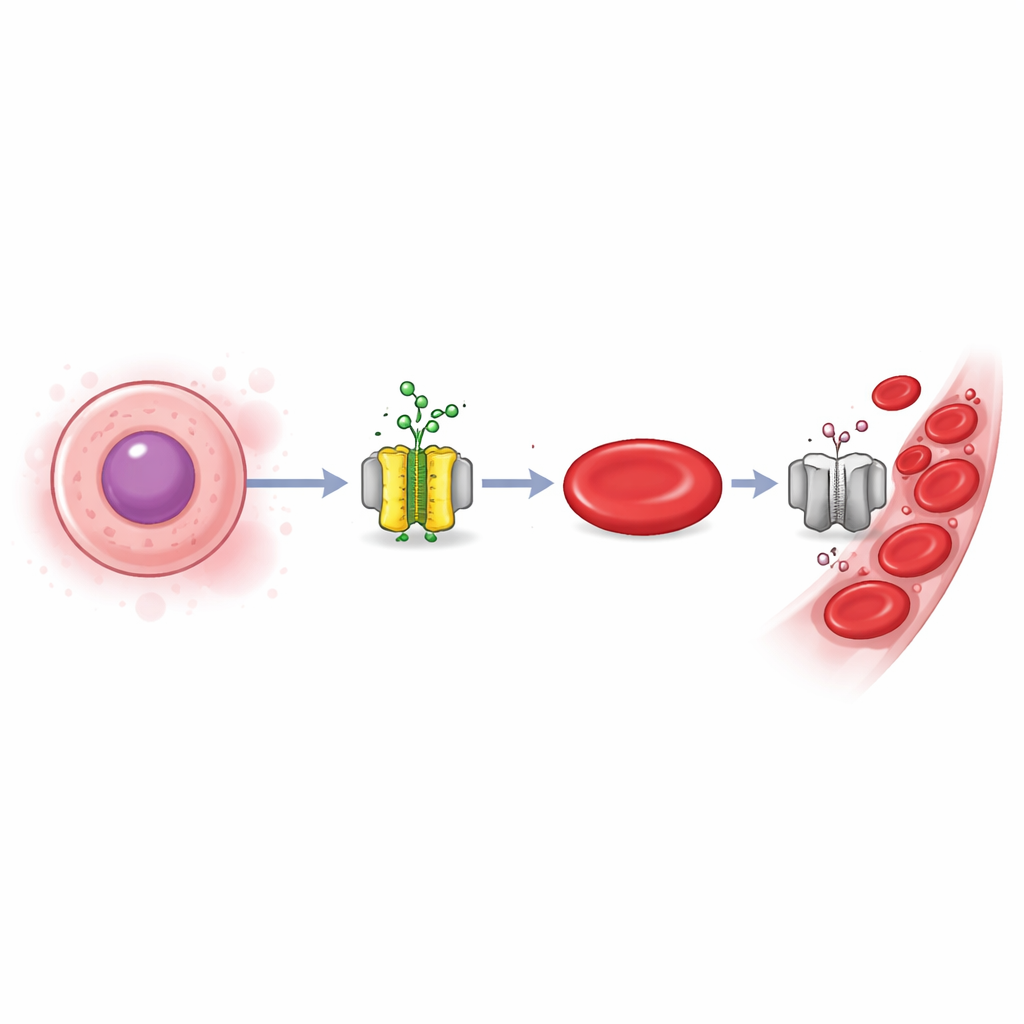
المراحل النهائية لنمو كريات الدم الحمراء
تولد كريات الدم الحمراء من خلايا سلفية غير ناضجة تتقلص تدريجيًا، وتمتلئ بالهيموغلوبين، وفي النهاية تتخلص من نواتها. تُسمى هذه المرحلة الأخيرة النضج النهائي، ويقودها هرمون الإريثروبويتين الذي يخبر الخلايا متى تبقى على قيد الحياة ومتى تنقسم أو تتخصص. يعمل عامل ضبط جيني رئيسي يدعى KLF1 كالبرنامج الرئيسي الذي يشغل الجينات الخاصة بكريات الدم الحمراء، بما في ذلك جينات الهيموغلوبين وعملية فقدان النواة. ومع ذلك، يمكن للإريثروبويتين أن يعزز النضج ويبطئه في آن واحد، وكان من غير الواضح كيف يوقّت نشاط KLF1 في مراحل مختلفة.
قناة كالسيوم تبطئ النضج المبكر
ركز المؤلفون على الكالسيوم، الأيون المستخدَم عالميًا في الإشارات، وقناة غشائية تسمى Orai1 تسمح بتدفق الكالسيوم إلى داخل الخلايا. باستخدام خطوط خلايا حمراء بشرية وسلاسل مأخوذة من دم الحبل السري وخلايا دم مُنتَجة من الخلايا الجذعية متعددة القدرات، وجدوا أن السلفيات الشابة تُعبّر عن مستويات عالية من Orai1 وتُظهر دخولًا قويًا للكالسيوم، بينما تُظهر الخلايا الأكثر نضجًا مستويات أقل بكثير من Orai1 وإشارات كالسيوم أضعف. أظهر تعطيل التحلل البروتيني العام أن Orai1 يزال بشكل رئيسي عبر مسار التحلل الذاتي–الليزوزوم أثناء النضج. وظيفيًا، عندما عُطّل Orai1 بواسطة شكل طافر أو عن طريق حذف جيني بواسطة CRISPR–Cas9، انخفض دخول الكالسيوم، لكن ارتفعت مستويات KLF1. دفع ذلك الخلايا للتعبير عن المزيد من جينات كريات الدم الحمراء، وإنتاج مزيد من الجلوبين، والنضج بسرعة أكبر، وفقدان النواة بكفاءة أعلى.
كيف يعمل المفتاح داخل الخلية
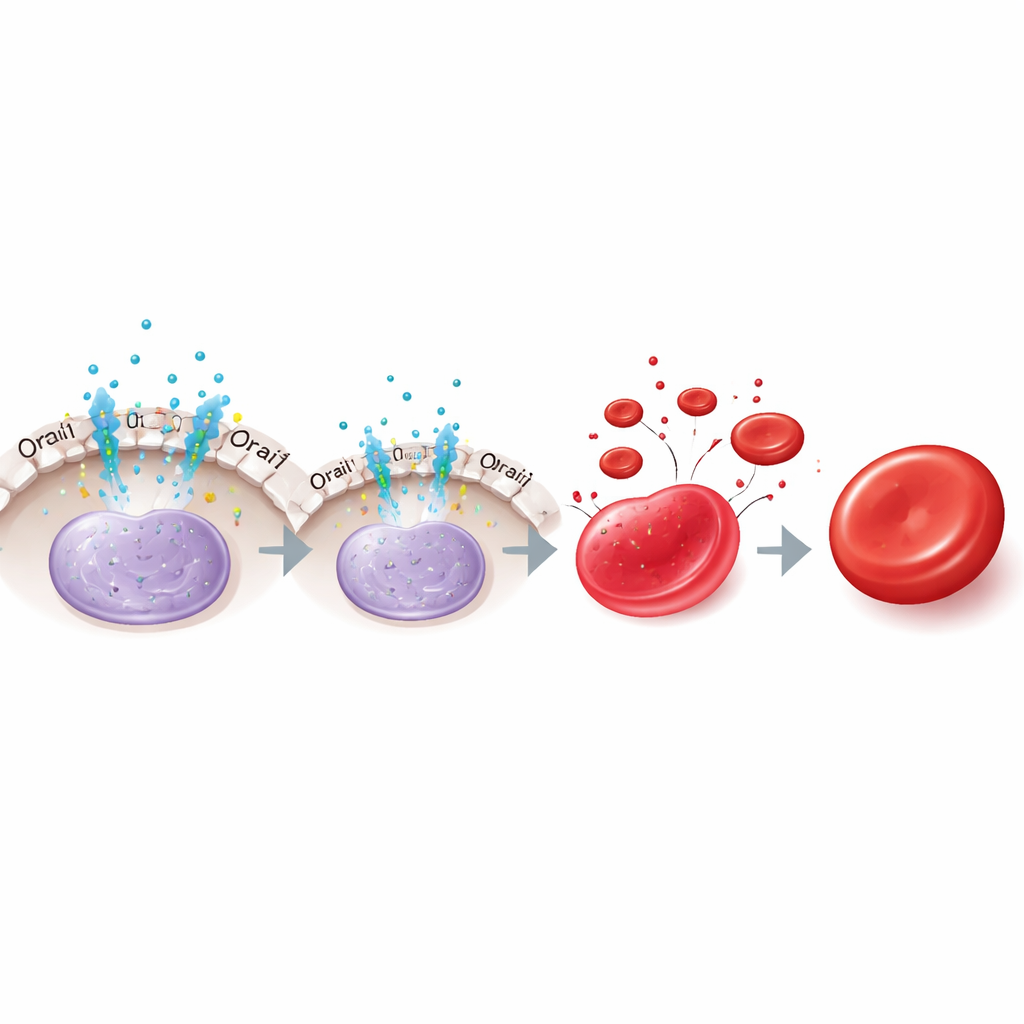
نقل الولاية إلى مسار هرموني ثانٍ
ومن اللافت أن دور الإريثروبويتين يتغير مع الزمن. في الخلايا المبكرة، أدى إزالة الإريثروبويتين أو حجب Orai1 إلى زيادة KLF1 وتسريع النضج، تماشيًا مع إزالة كبح NFAT2. لكن في الخلايا المتأخرة، أدى فقدان الإريثروبويتين إلى خفض KLF1 وإضعاف النضج، على الرغم من أن تثبيط Orai1 لم يعد له تأثير. عزَّى المؤلفون هذا الدعم المتأخر لـ KLF1 إلى مسار إريثروبويتين ثانٍ يشمل بروتين الإشارة STAT5 وشركاءه اللاحقين TAL1 وDDX5، الذين يساعدون في صيانة KLF1 بعد تلاشي فرامل Orai1–NFAT2. وهكذا، يقيد الإريثروبويتين أولًا KLF1 عبر Orai1–NFAT2، ثم يدعمه لاحقًا عبر STAT5 وعوامله المساعدة.
نحو دم مُنتَج مخبريًا أفضل
بعبارة بسيطة، تُظهر هذه الدراسة أن Orai1 يعمل كمفتاحٍ مبني على الكالسيوم يسمح للإريثروبويتين بضبط توقيت توقُّف سلفيات كريات الدم الحمراء الشابة أو تقدمها. عندما يكون Orai1 "قيد التشغيل"، تُفعل إشارات الكالسيوم NFAT2 للحفاظ على كبح KLF1 والنضج الكامل؛ وعندما يكون Orai1 "مطفأ"، يتحول تأثير الإريثروبويتين إلى مسار STAT5 الذي يحافظ على KLF1 مرتفعًا ويدفع التحول النهائي إلى خلايا حاملة للأكسجين. عبر خفض نشاط Orai1 أو إزالة الإريثروبويتين مؤقتًا في المرحلة المناسبة، قد يصبح من الممكن حث السلفيات المأخوذة من الخلايا الجذعية لتتحول بكفاءة أكبر إلى كريات دم حمراء وظيفية وخالية من النواة، مما يقرب إمكانية الحصول على دم مُنتَج مخبريًا لغرض النقل خطوة أقرب إلى التطبيق العملي.
الاستشهاد: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
الكلمات المفتاحية: نضوج كريات الدم الحمراء, إشارات الكالسيوم, قناة Orai1, الإريثروبويتين, KLF1