Clear Sky Science · it
Orai1 agisce come un nuovo interruttore di segnalazione Ca2+, bilanciando l’eritropoiesi tramite la regolazione di KLF1
Perché uno switch molecolare per i globuli rossi è importante
Ogni secondo il tuo corpo produce milioni di nuovi globuli rossi per trasportare ossigeno. Per le trasfusioni, per le carenze di sangue e per future terapie cellulari, gli scienziati vogliono coltivare queste cellule in laboratorio in modo efficiente. Tuttavia, gli stadi finali della maturazione dei globuli rossi sono sorprendentemente difficili da controllare. Questo studio rivela un nascosto “dimmer” molecolare che decide se le giovani cellule del sangue continuano a svilupparsi o si fermano, aprendo nuove strade per aumentare la produzione di sangue coltivato e per comprendere meglio alcune anemie. 
Gli ultimi passi della crescita dei globuli rossi
I globuli rossi nascono da precursori immaturi che progressivamente si riducono di dimensione, si riempiono di emoglobina e infine espellono il nucleo. Questa fase finale, chiamata maturazione terminale, è guidata dall’ormone eritropoietina, che indica alle cellule quando sopravvivere, dividersi o specializzarsi. Un importante regolatore genico chiamato KLF1 funziona come un programma maestro che attiva i geni specifici dei globuli rossi, inclusi quelli per l’emoglobina e l’enucleazione. Tuttavia, l’eritropoietina può sia promuovere sia rallentare la maturazione, e non era chiaro come temporizzasse l’attività di KLF1 nelle diverse fasi.
Un canale del calcio che rallenta la maturazione precoce
Gli autori si sono concentrati sul calcio, un ione di segnalazione universale, e su un canale di membrana chiamato Orai1 che permette l’ingresso di calcio nelle cellule. Utilizzando linee cellulari eritroidi umane, cellule derivate da sangue cordonale e globuli rossi cresciuti da cellule staminali pluripotenti, hanno riscontrato che i precursori giovani esprimono alti livelli di Orai1 e mostrano un forte ingresso di calcio, mentre le cellule più mature presentano livelli molto più bassi di Orai1 e segnali calciici più deboli. Bloccare la degradazione proteica generale ha mostrato che Orai1 viene rimosso principalmente attraverso la via autofagia–lisosoma man mano che le cellule maturano. A livello funzionale, quando Orai1 è stato disattivato da una forma mutante o con knockout CRISPR–Cas9, l’ingresso di calcio è diminuito, ma i livelli di KLF1 sono aumentati. Questo ha spinto le cellule a esprimere più geni dei globuli rossi, produrre più globina, maturare più rapidamente e enuclearsi in modo più efficiente.
Come funziona lo switch all’interno della cellula
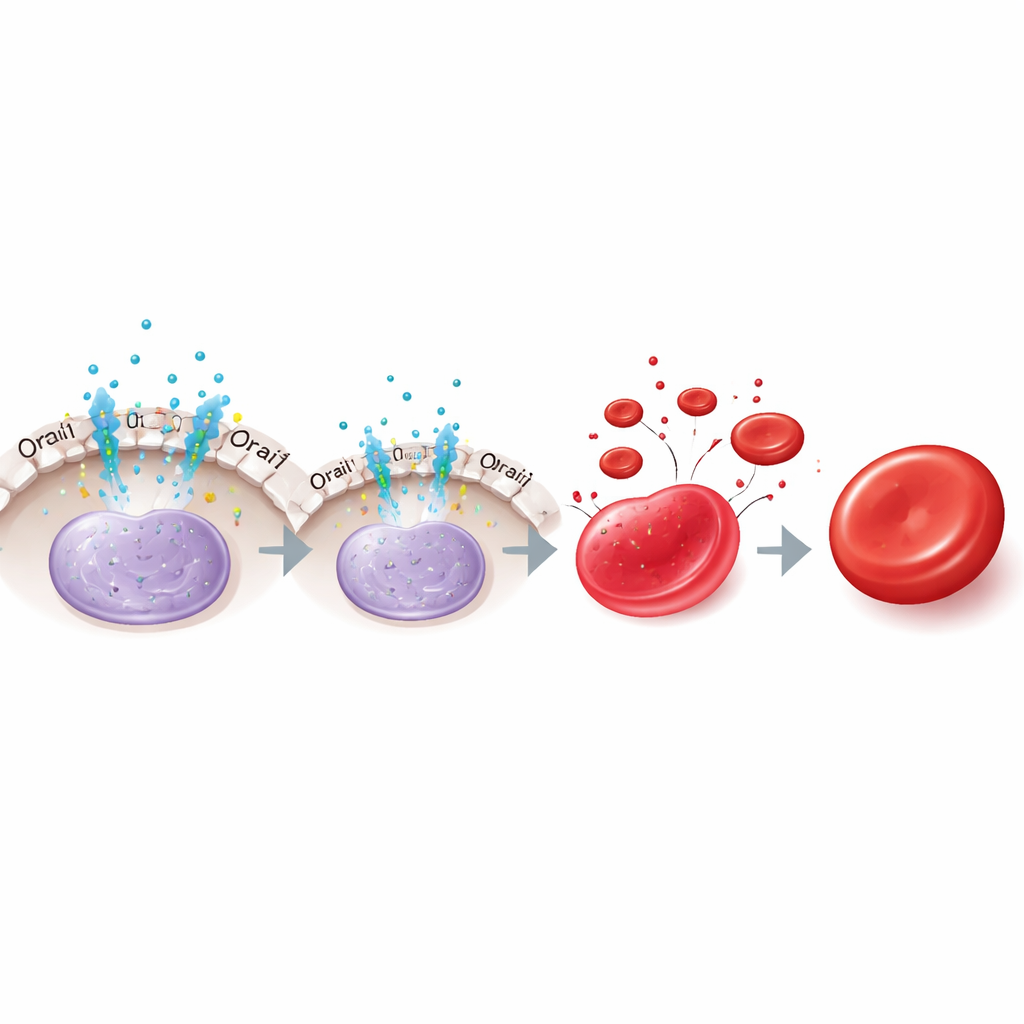
Un passaggio a una seconda via ormonale
È interessante che il ruolo dell’eritropoietina cambi nel tempo. Nelle cellule precoci, rimuovere l’eritropoietina o bloccare Orai1 aumentava KLF1 e accelerava la maturazione, coerentemente con l’eliminazione della soppressione mediata da NFAT2. Ma nelle cellule in stadio avanzato, l’assenza di eritropoietina riduceva invece KLF1 e comprometteva la maturazione, anche se l’inibizione di Orai1 non aveva più effetto. Gli autori hanno identificato questo supporto tardivo di KLF1 in un’altra via dell’eritropoietina che coinvolge la proteina di segnalazione STAT5 e i suoi partner a valle TAL1 e DDX5, che aiutano a mantenere KLF1 una volta che il freno Orai1–NFAT2 è svanito. Così, l’eritropoietina prima limita KLF1 tramite Orai1–NFAT2, poi più tardi sostiene KLF1 attraverso STAT5 e i suoi cofattori.
Verso un sangue coltivato migliore
In termini semplici, questo lavoro mostra che Orai1 funziona come uno switch a base di calcio che permette all’eritropoietina di modulare con precisione quando i precursori dei globuli rossi giovani devono fermarsi o procedere. Quando Orai1 è “acceso”, i segnali calciici attivano NFAT2 per mantenere KLF1 e la maturazione completa sotto controllo; quando Orai1 è “spento”, l’eritropoietina si sposta su una via STAT5 che mantiene KLF1 elevato e guida la trasformazione finale in cellule trasportatrici di ossigeno. Abbassando Orai1 o rimuovendo temporaneamente eritropoietina nella fase giusta, potrebbe essere possibile indurre i precursori derivati da cellule staminali a diventare globuli rossi funzionali ed enucleati in modo più efficiente, avvicinando la prospettiva del sangue coltivato per trasfusioni a una realtà più pratica.
Citazione: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Parole chiave: maturazione dei globuli rossi, segnalazione del calcio, canale Orai1, eritropoietina, KLF1