Clear Sky Science · ru
Orai1 действует как новый переключатель Ca2+-сигнала, балансируя эритропоэз через регуляцию KLF1
Почему важен молекулярный переключатель для эритроцитов
Каждую секунду ваш организм производит миллионы новых эритроцитов для транспортировки кислорода. Для переливаний, при дефиците крови и в будущих клеточных терапиях учёные стремятся эффективно выращивать эти клетки в лаборатории. Тем не менее последние этапы созревания эритроцитов удивительно трудно контролировать. В этом исследовании обнаружен скрытый молекулярный «регулятор яркости», который решает, продолжат ли молодые клетки развитие или приостановят его, что открывает новые пути для увеличения производства лабораторно выращенной крови и лучшего понимания некоторых анемий. 
Финальные этапы роста эритроцитов
Эритроциты рождаются из незрелых прекурсоров, которые постепенно уменьшаются в размере, заполняются гемоглобином и в конце концов выбрасывают ядро. Этот заключительный этап, называемый терминальным созреванием, регулируется гормоном эритропоэтином, который сообщает клеткам, когда выживать, делиться или специализироваться. Ключевой регулятор генов KLF1 действует как мастер‑программа, включающая гены, специфичные для эритроцитов, в том числе ответственные за гемоглобин и энуклеацию. Однако эритропоэтин может как стимулировать, так и замедлять созревание, и было неясно, как он координирует активность KLF1 на разных стадиях.
Кальциевый канал, замедляющий раннее созревание
Авторы сосредоточились на кальции, универсальном сигнальном ионе, и на мембранном канале Orai1, который обеспечивает вхождение кальция в клетки. Используя линии человеческих эритроидных клеток, клетки из пуповинной крови и эритроциты, выращенные из плюрипотентных стволовых клеток, они обнаружили, что молодые прекурсоры экспрессируют высокий уровень Orai1 и демонстрируют сильный вход кальция, в то время как более зрелые клетки имеют значительно меньший Orai1 и слабые кальциевые сигналы. Блокирование общего белкового распада показало, что Orai1 удаляется главным образом через путь аутофагии–лизосомы по мере созревания клеток. Функционально, когда Orai1 был отключён мутантной формой или с помощью нокаута CRISPR–Cas9, вход кальция уменьшался, но уровни KLF1 росли. Это заставляло клетки активнее экспрессировать гены эритроцитов, производить больше глобина, созревать быстрее и эффективнее проходить энуклеацию.
Как переключатель работает внутри клетки
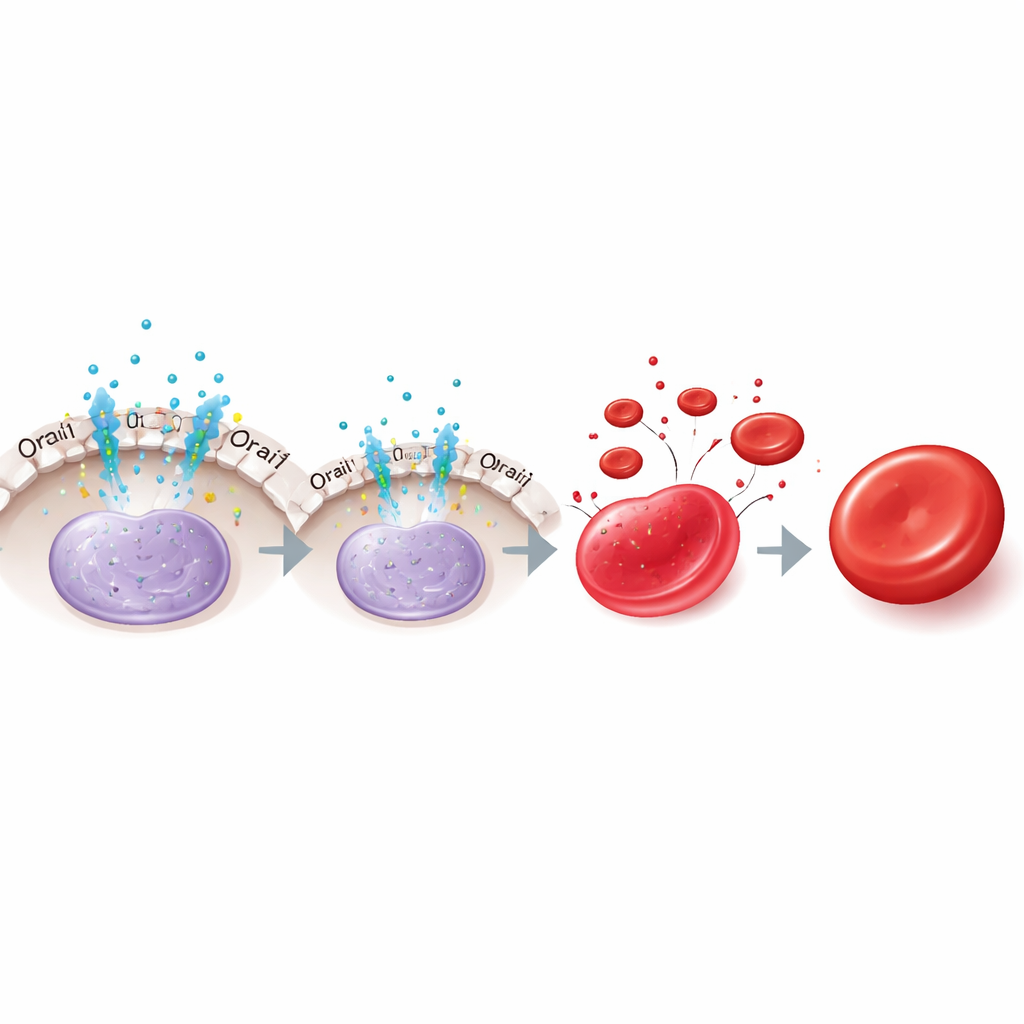
Передача управления на второй гормональный путь
Интересно, что роль эритропоэтина меняется со временем. В ранних клетках удаление эритропоэтина или блокада Orai1 увеличивала KLF1 и ускоряла созревание, что согласуется с ослаблением подавления со стороны NFAT2. Но на поздних стадиях лишение эритропоэтина теперь снижало KLF1 и нарушало созревание, хотя ингибирование Orai1 уже не оказывало эффекта. Авторы проследили эту позднюю поддержку KLF1 до другого пути эритропоэтина, включающего сигнальный белок STAT5 и его вспомогательные партнёры TAL1 и DDX5, которые помогают поддерживать KLF1 после того, как тормоз Orai1–NFAT2 ослабевает. Таким образом, эритропоэтин сначала сдерживает KLF1 через Orai1–NFAT2, а затем позже поддерживает KLF1 через STAT5 и его со‑факторы.
К шагам навстречу лучшей лабораторно выращенной крови
Проще говоря, эта работа показывает, что Orai1 функционирует как кальциевый переключатель, который позволяет эритропоэтину точно регулировать, когда молодые прекурсоры эритроцитов должны приостановиться или продолжить развитие. Когда Orai1 «включён», кальциевые сигналы активируют NFAT2, чтобы сдерживать KLF1 и полное созревание; когда Orai1 «выключен», эритропоэтин переключается на путь STAT5, который удерживает высокий уровень KLF1 и продвигает окончательное превращение в клетки, переносящие кислород. Понизив активность Orai1 или временно убрав эритропоэтин на нужной стадии, возможно, удастся подтолкнуть прекурсоры, полученные из стволовых клеток, к более эффективному формированию функциональных энуклеированных эритроцитов, что приблизит перспективу лабораторно выращенной крови для переливаний к реальности.
Цитирование: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
Ключевые слова: созревание эритроцитов, кальциевые сигналы, канал Orai1, эритропоэтин, KLF1