Clear Sky Science · he
Orai1 פועל כמתג סיגנל Ca2+ חדש, מתוך איזון אריתרופויזה באמצעות ויסות KLF1
מדוע מתג מולקולרי לתאי דם אדומים חשוב
כל שנייה, הגוף מייצר מיליוני תאי דם אדומים חדשים לנשיאת חמצן. עבור זילוח דם, מחסור בדם וטיפולים עתידיים בתאים, מדענים שואפים לגדל תאים אלה ביעילות במעבדה. עם זאת, השלבים האחרונים של הבשלת תאי דם אדומים קשים להפתיע בשליטה. מחקר זה חושף "דימר סודי" מולקולרי שמחליט האם תאים צעירים ימשיכו להתפתח או יעצרו, ופותח דרכים חדשות להגדיל את ייצור הדם במעבדה ולהבין טוב יותר אנמיות מסוימות. 
השלבים הסופיים של גידול תאי דם אדומים
תאי הדם האדומים נולדים מתאי-אם בלתי בשלים שהולכים ומצטמצמים, מתמלאים בהמוגלובין ולבסוף משליכים את גרעינם. מרחק זה האחרון, המוגדר בשלות סופית, מנווט על ידי ההורמון אריתרופוייטין, שמכריז לתאים מתי לשרוד, להתחלק או להתמחות. בקר גנים מרכזי בשם KLF1 פועל כתוכנית-על שמפעילה גנים ספציפיים לתאי דם אדומים, כולל אלו של המוגלובין והפליטת גרעין. עם זאת, אריתרופוייטין יכול גם לקדם וגם להאט את הבשלות, ואיך הוא מתזמן את פעילות KLF1 בשלבים שונים היה עד כה לא ברור.
תעלת סידן שמאטת הבשלות המוקדמת
המחברים התמקדו בסידן, יון איתות אוניברסלי, ובתעלת ממברנה בשם Orai1 שמאפשרת זרימת סידן לתאים. באמצעות קווי תאים אריתרואידים אנושיים, תאים שמקורם בדם חבל טבור ותאי דם אדומים שגודלו מתאי גזע פלוריפוטנטיים, הם גילו שתאים צעירים מבטאים רמות גבוהות של Orai1 ומראים כניסת סידן מוגברת, בעוד שתאים בשלים יותר מציגים Orai1 נמוך יותר ואותות סידן חלשים יותר. חסימת פירוק חלבונים כללי הראתה כי Orai1 מוסר בעיקר דרך מסלול אוטופאגיה–ליזוזום ככל שהתאים מתבגרים. מבחינה פונקציונלית, כאשר Orai1 הושבת על ידי צורה מוטנטית או על ידי חיתוך CRISPR–Cas9, כניסת הסידן ירדה אך רמות KLF1 עלו. הדבר דחף את התאים לבטא יותר גנים של תאי דם אדומים, לייצר יותר גלובין, לבשל מהר יותר ולהפליט את גרעינם ביעילות גבוהה יותר.
כיצד המתג פועל בתוך התא
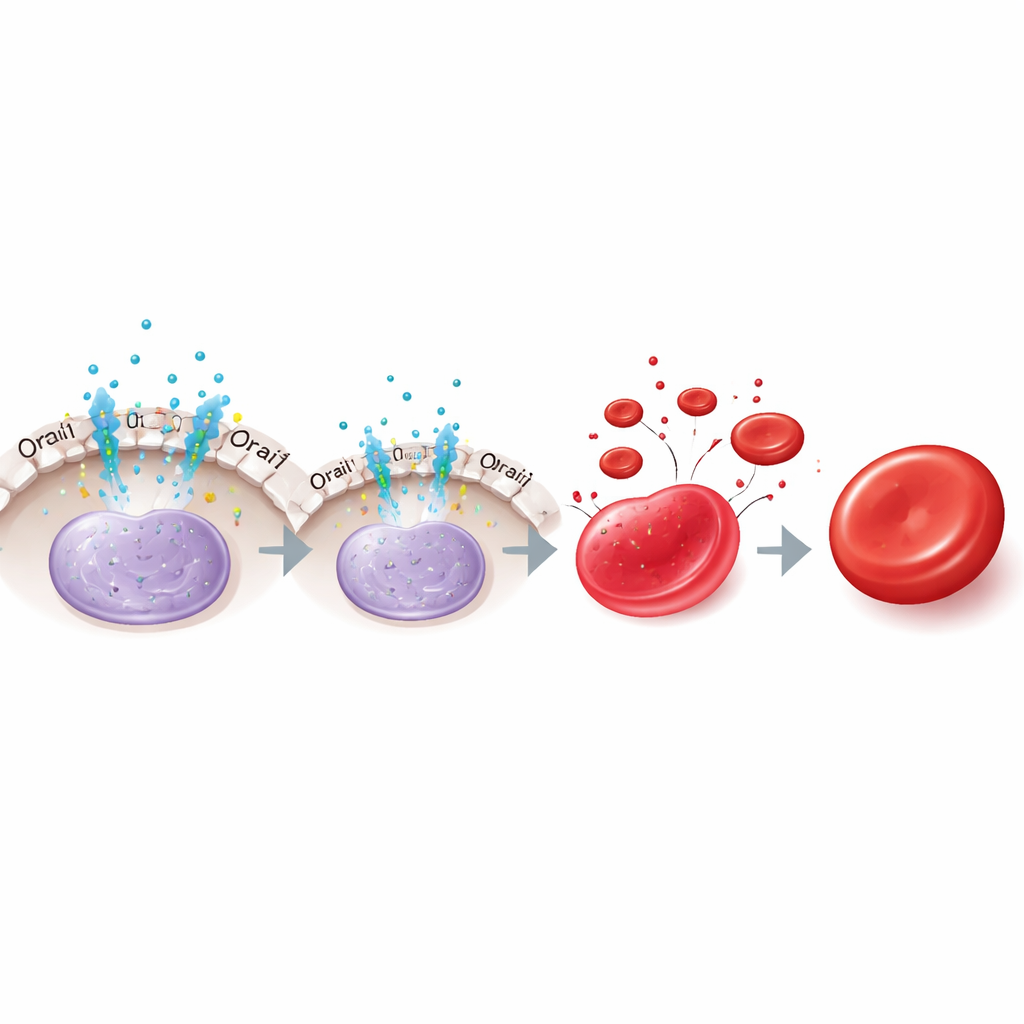
העברה למסלול הורמונלי שני
באופן מעניין, תפקידו של אריתרופוייטין משתנה עם הזמן. בתאים מוקדמים, הסרת אריתרופוייטין או חסימת Orai1 העלתה את KLF1 וזרזה את הבשלות, בהתיישבות עם שחרור מדיכוי מתווך על ידי NFAT2. אבל בשלבים מאוחרים יותר, הוצאת אריתרופוייטין עכשיו הקטינה את KLF1 ופגעה בבשלות, אף על פי שעיכוב Orai1 כבר לא השפיע. המחברים עקבו אחרי התמיכה המאוחרת הזו של KLF1 למסלול אריתרופוייטין נוסף הכולל את חלבון האיתות STAT5 ואת שותפיו היורדים TAL1 ו-DDX5, המסייעים לשמר את KLF1 לאחר שבלם Orai1–NFAT2 נשחק. לפיכך, אריתרופוייטין תחילה מרסן את KLF1 דרך Orai1–NFAT2, ואחר כך שומר עליו דרך STAT5 וקו-פקטורים שלו.
לקראת דם משובח שגודל במעבדה
בקצרה, עבודה זו מראה כי Orai1 מתפקד כמתג מבוסס סידן שמאפשר לאריתרופוייטין לכוונן מתי תאי אם צעירים של הדם האדום צריכים לעצור או להתקדם. כאשר Orai1 "פעיל", אותות סידן מפעילים NFAT2 כדי לשמור על KLF1 ועל הבשלות המלאה במגבלות; כאשר Orai1 "כבוי", אריתרופוייטין עובר למסלול STAT5 ששומר על KLF1 גבוה ודוחף את ההמרה הסופית לתאים נושאי חמצן. על ידי כיבוי Orai1 או הסרת אריתרופוייטין לזמן קצר בשלב המתאים, יתכן שניתן לאלץ תאים-אם נגזרים להפוך לתאי דם אדומים פונקציונליים ומולקולי-מופרדים ביתר יעילות, וכך לקרב את אפשרות הדם המשובח שגודל במעבדה לשימוש בזילוחים.
ציטוט: Lee, Y.Y., Koh, H., Kim, J. et al. Orai1 acts as a novel Ca2+ signal switch, balancing erythropoiesis through KLF1 regulation. Exp Mol Med 58, 696–708 (2026). https://doi.org/10.1038/s12276-026-01651-0
מילות מפתח: בשלת תאי דם אדומים, אותות סידן, תעלת Orai1, אריתרופוייטין, KLF1