Clear Sky Science · tr
Akışta derin öğrenmeli holografi kullanarak kanser hastalarında dolaşımdaki tümör hücresi tespiti
Basit Bir Kan Alma İşleminde Kanser İpuçları Bulmak
Kanser, bir tümör görüntüde ortaya çıkmadan çok önce dolaşıma hücreler bırakarak yayılabilir. Bu dolaşan “tümör hücreleri” nadir ancak güçlü ipuçlarıdır: kanserin varlığını işaret edebilir, tedaviye yanıtını izleyebilir ve gelecekte neler olabileceğine dair göstergeler sunabilirler. Bu makale, milyarlarca kan hücresi arasından bu birkaç tehlikeli kaçkını hızlı, nazik ve yüksek doğrulukla ayıklayabilen yeni bir teknolojiyi anlatıyor — kanseri gerçek zamanlı izleyen rutin kan testleri olasılığını gündeme getiriyor.
Bu Nadir Hücrelerin Neden Önemi Var
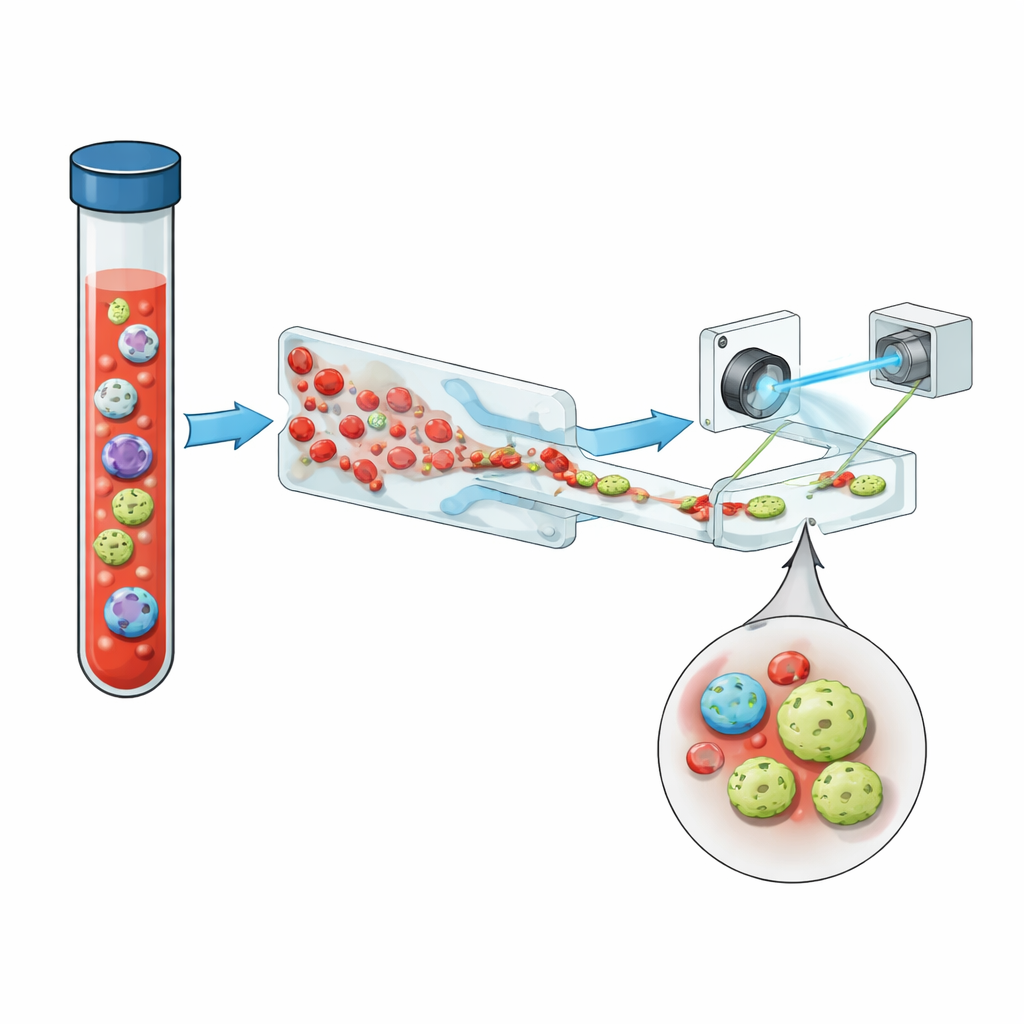
Dolaşımdaki tümör hücreleri (CTC’ler), bir primer veya metastatik tümörden kopup kana karışmış kanser hücreleridir. İleri hastalıkta bile bir mililitre kanda milyarlarca normal kırmızı ve beyaz kan hücresi bulunurken CTC’ler sadece birkaç adet —bazı durumlarda birden az— olabilir. Yine de sayıları ve davranışları tümörün ne kadar agresif olduğu, tedaviye direnç geliştirme eğilimi ve hastanın yaşam süresiyle yakından ilişkilidir. Standart tespit yöntemleri genellikle EpCAM gibi yüzey belirteçlerine dayanır; bunlar birçok epitelial kanser hücresinin dış yüzeyindeki proteinlerdir. Ancak tümörler evrilip durum değiştirirken bu belirteçler kaybolabilir; bu da en tehlikeli hücrelerin tespit dışı kalmasına yol açabilir.
Mevcut Testlerin Eksiklikleri
Mevcut birçok CTC kan testi hücreleri moleküler “isimlikleri”ne ya da boyut ve sertlik gibi fiziksel özelliklerine göre yakalamaya çalışır. EpCAM taşıyan hücreleri manyetik olarak ayıran belirteç‑temelli sistemler, metastazla ilişkili biçim değiştirme sürecinde bu belirteçleri kapatan tümör hücrelerini kaçırabilir. Boyut- veya yoğunluk‑temelli filtreler de başarısız olabilir, çünkü bazı tümör hücreleri normal beyaz kan hücreleriyle benzer boyut ve yapıda olabilir. Birden fazla yöntemi birleştiren cihazlar—karma mikroakışkan çipler, mıknatıslar veya akustik kuvvetler—duyarlılığı artırırken genellikle daha yüksek karmaşıklık, maliyet ve hücre kaybı bedeli öder. Sonuç olarak birçok platform, günlük klinik kullanım için yeterince basit ve aynı zamanda tümör hücrelerinin tam çeşitliliğini yakalayacak kadar hassas olma açısından zorluk yaşar.
Hücreleri Akış Halindeyken Görmenin Yeni Bir Yolu
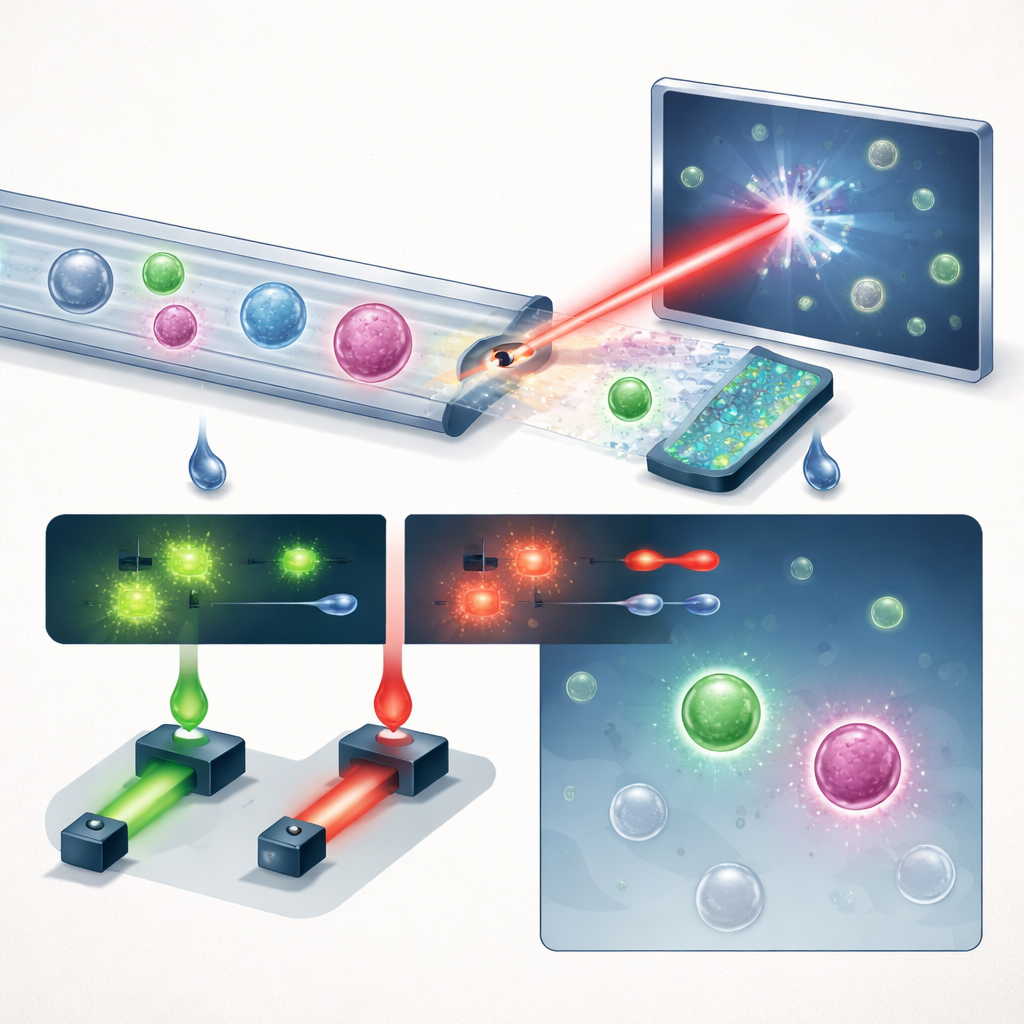
Araştırma ekibi üç ana fikri zincirleyen kompakt bir sistem sunuyor: akıllı sıvı yönetimi, holografik görüntüleme ve derin öğrenme; bunlara yardımcı olarak fluoresans da ekleniyor. Önce tam kan, “testere dişi” mikroakışkan çipten geçirilerek kırmızı kan hücrelerinin %99.999’dan fazlası ve neredeyse tüm beyaz kan hücreleri çıkarılıyor; buna karşın tümör hücrelerinin büyük çoğunluğu korunuyor. Bu, kalabalık bir örneği nadir hücrelerin daha kolay öne çıkabileceği bir akıma dönüştürüyor. Zenginleştirilmiş akım daha sonra dar ve düz bir kanaldan, darbeli morötesi lazer altından akıyor. Sistemin düz resimler almak yerine kaydettiği hologramlar —her hücrenin parlaklığını ve optik kalınlığını kodlayan girişim desenleri— tek bir görüntüde ince üç boyutlu yapıyı yakalıyor.
Sıradışı Olanları Tespit Etmesi İçin Bir Sinir Ağını Eğitmek
Gerçek CTC’ler nadir olduğundan algoritmayı eğitmek için yeterli gerçek hasta örneği doğrudan toplamak pratik değildir. Araştırmacılar bunun yerine derin öğrenme modeline sıradan kana benzemeyen her şeyi tanımayı öğrettiler. Modele sağlıklı donörlerden gelen milyonlarca hologram verildi; bu görüntüler beyaz ve kırmızı kan hücreleri ile kalıntıların tam çeşitliliğini gösteriyordu ve laboratuvarda yetiştirilen çeşitli kanser hücresi hatlarından alınan görüntülerle dengelendi. Özelleştirilmiş bir sinir ağı her hologramı olası tümör konumlarının bir ısı haritasına dönüştürüyor, hücreleri kutular yerine parlayan anahtar noktalar olarak ele alıyor. Sürekli elle etiketleme gerekmeksizin eğitimi ölçeklendirmek için yardımcı bir model önce saf kanser hücresi görüntülerindeki tüm hücreleri işaretliyor; ana model bu “sahte‑etiketleri” ve gerçek CTC’lerin nadirliğini yansıtacak şekilde ayarlanmış bir kayıp fonksiyonunu kullanarak yanlış alarmlara karşı katı olup sıra dışı hücreleri yakalamayı öğreniyor.
Sistemi Sınamak
Bilinen sayıda prostat kanseri hücresinin sağlıklı kana eklendiği kontrollü deneylerde, platform seçilen işletim noktasında bu hücrelerin yaklaşık %60’ını geri kazandı ve liberaller tespit eşiklerinde bile mililitre başına birin altında yanlış pozitif tutmayı başardı. Kararlarını daha da keskinleştirmek için sistem, PSMA (prostate‑specific membrane antigen) ve EpCAM’e karşı antikorlardan iki floresan sinyal de ölçüyor. Hasta testlerinde bir hücrenin CTC sayılması için hem holografik derin öğrenme eşiklerini geçmesi hem de güçlü bir PSMA sinali göstermesi gerekiyordu; böylece etiketsiz şekil bilgisi hedefe yönelik moleküler onayla birleştirildi. Araştırmacılar bunu ileri prostat kanseri olan 13 erkek ve 8 sağlıklı erkek donöre uyguladıklarında, kanser grubunda CTC sayıları kontrol grubuna göre çok daha yüksekti (medyan 1 mL başına 12,5 hücre vs. 1,5 hücre). Dikkat çekici olarak, PSMA‑pozitif hücrelerin yalnızca yaklaşık üçte biri EpCAM taşıyordu; bu da yalnızca EpCAM’e dayanan testlerin bu hastalardaki tümör hücrelerinin çoğunu kaçıracağına işaret ediyor.
Hastalar İçin Ne Anlama Gelebilir
Standart bir kan alma işleminden nadir kanser hücreleri için zengin, otomatik bir tarama elde ederek, bu platform daha uygulanabilir “sıvı biyopsiler”e işaret ediyor. Etiketsiz holografi, hedefe yönelik floresans ve derin öğrenmenin birleşimi düşük yanlış pozitif oranına ulaşırken geleneksel belirteç‑temelli sistemlerin gözden kaçırdığı CTC’leri yakalıyor. Bugün için bu, pilot prostat kanseri çalışmasında kanser hastalarını sağlıklı bireylerden daha iyi ayırma anlamına geliyor. İleride bu yaklaşım birçok tümör tipi ve farklı sıvılara uyarlanabilir ve sonunda tamamen floresan etiketlere ihtiyaç duymadan yalnızca hücrelerin holografik görünümüne dayanarak çalışabilir. Daha büyük ve çeşitli denemelerde tamamen kanıtlanırsa, böyle sistemler doktorların kan testiyle zaman içinde kanserin yükselişini ve gerilemesini izlemesine, tedavileri daha erken ayarlamasına ve canlı tümör hücrelerini detaylı moleküler analiz için geri kazanmasına olanak sağlayabilir—tüm bunlar bir skalpeldan bağımsız olarak.
Atıf: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Anahtar kelimeler: dolaşımdaki tümör hücreleri, sıvı biyopsi, dijital holografik mikroskopi, derin öğrenme tanı yöntemleri, prostat kanseri