Clear Sky Science · de
Nachweis zirkulierender Tumorzellen bei Krebspatienten mittels In‑Flow‑Deep‑Learning‑Holographie
Krebs‑Hinweise aus einer einfachen Blutentnahme
Krebs breitet sich oft lange aus, bevor ein Tumor im Bildgebungsverfahren sichtbar wird, indem er einzelne Zellen in den Blutkreislauf abgibt. Diese umherwandernden „zirkulierenden Tumorzellen“ sind zwar selten, liefern aber wichtige Hinweise: Sie können auf das Vorhandensein von Krebs hindeuten, zeigen, wie der Tumor auf eine Behandlung reagiert, und geben Hinweise auf den weiteren Verlauf. Diese Studie beschreibt eine neue Technologie, die Milliarden von Blutzellen durchsiebt, um diese wenigen gefährlichen Ausreißer schnell, schonend und mit hoher Genauigkeit zu finden — und damit die Aussicht auf routinemäßige Bluttests eröffnet, die Krebs in Echtzeit verfolgen.
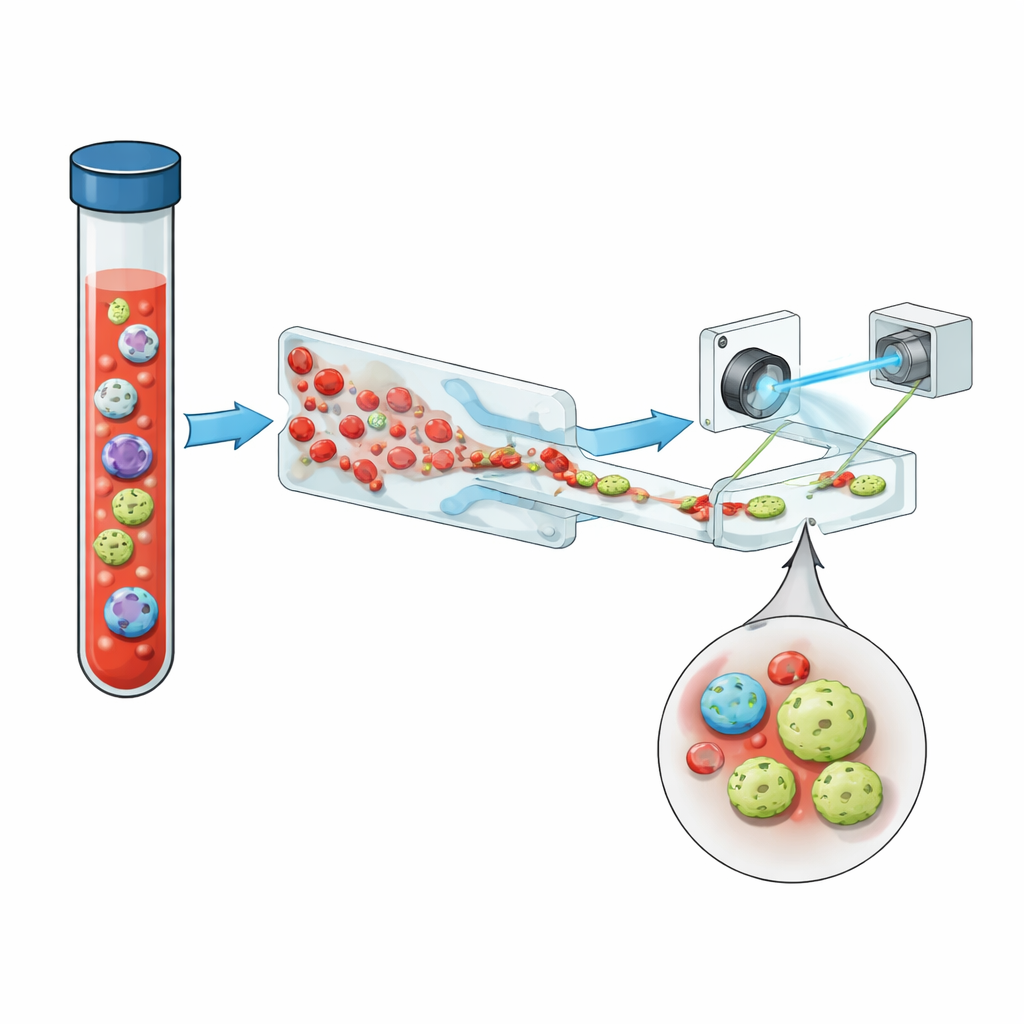
Warum diese seltenen Zellen wichtig sind
Zirkulierende Tumorzellen (CTCs) sind Krebszellen, die sich von einem primären oder metastatischen Tumor gelöst und in den Blutstrom gelangt sind. Selbst bei fortgeschrittener Erkrankung kann ein Milliliter Blut Milliarden normaler roter und weißer Blutkörperchen enthalten, jedoch nur eine Handvoll CTCs — manchmal weniger als eins. Dennoch korrelieren Anzahl und Verhalten dieser Zellen eng mit der Aggressivität eines Tumors, seiner Therapieresistenz und der Lebenserwartung eines Patienten. Übliche Nachweisverfahren stützen sich oft auf Oberflächenmarker wie EpCAM, Proteine auf der Außenseite vieler epithelialer Krebszellen. Wenn Tumoren sich jedoch weiterentwickeln und ihren Zustand ändern, können diese Marker verblassen, sodass einige der gefährlichsten Zellen unentdeckt bleiben.
Schwächen aktueller Tests
Viele bestehende Bluttests für CTCs versuchen, Zellen über molekulare „Namensschilder“ oder physikalische Eigenschaften wie Größe und Steifigkeit zu erfassen. Markerbasierte Systeme, etwa solche, die EpCAM‑tragende Zellen magnetisch herausziehen, können Tumorzellen übersehen, die diese Marker während eines formverändernden Prozesses im Zusammenhang mit der Metastasierung abgeschaltet haben. Filter, die nach Größe oder Dichte trennen, versagen ebenfalls, weil einige Tumorzellen in Größe und Beschaffenheit normalen weißen Blutkörperchen ähneln. Geräte, die mehrere Methoden kombinieren — komplexe mikrofluidische Chips, Magnete oder akustische Kräfte — gewinnen an Sensitivität, oft auf Kosten höherer Komplexität, Kosten und Zellverluste. Daher tun sich viele Plattformen schwer, zugleich einfach genug für den klinischen Alltag und sensibel genug für die volle Vielfalt der Tumorzellen zu sein.
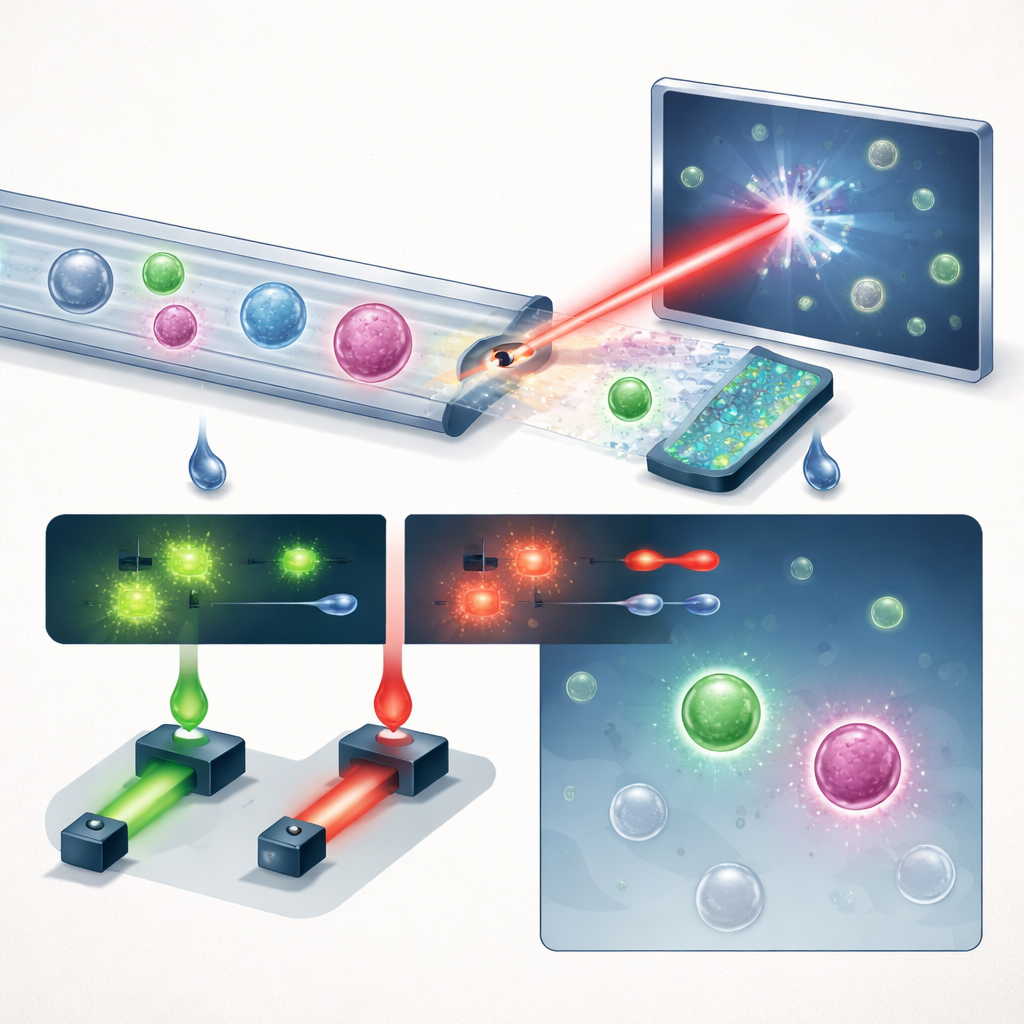
Eine neue Methode, Zellen im Fluss zu sehen
Das Team stellt ein kompaktes System vor, das drei zentrale Ideen verknüpft: intelligentes Fluidhandling, holografische Bildgebung und Deep Learning, ergänzt durch Fluoreszenz. Zunächst wird Vollblut durch einen „Sägezahn“-Mikrofluidikchip geleitet, der mehr als 99,999 % der roten Blutkörperchen und nahezu alle weißen Blutkörperchen entfernt, während der Großteil der Tumorzellen erhalten bleibt. So wird aus einer überfüllten Probe eine, in der seltene Zellen besser hervortreten können. Der angereicherte Strom fließt dann durch einen einfachen geraden Kanal unter einem gepulsten violetten Laser. Statt flacher Bilder zeichnet das System Hologramme auf — Interferenzmuster, die sowohl Helligkeit als auch optische Dicke jeder Zelle kodieren und subtile dreidimensionale Strukturen in einer einzigen Aufnahme erfassen.
Ein neuronales Netz darin schulen, die Ausreißer zu erkennen
Da echte CTCs so selten sind, ist das direkte Sammeln ausreichender realer Patientenbeispiele zur Algorithmus‑Schulung unpraktisch. Die Forscher haben daher ein Deep‑Learning‑Modell so trainiert, dass es alles erkennt, was nicht wie gewöhnliches Blut aussieht. Sie fütterten es mit Millionen von Hologrammen gesunder Spender, die die volle Vielfalt der weißen und roten Blutkörperchen und von Partikeln zeigen, und balancierten diese mit Bildern vieler verschiedener in Zellkulturen gezüchteter Krebszelllinien. Ein spezialisiertes neuronales Netz wandelt jedes Hologramm in eine Heatmap wahrscheinlicher Tumororte um und behandelt Zellen als leuchtende Punkte statt als begrenzende Kästen. Um das Training zu skalieren, ohne endlose manuelle Beschriftung, markiert ein Hilfsmodell zunächst alle Zellen in reinen Krebszellbildern; das Hauptmodell verwendet diese „Pseudo‑Labels“ sowie eine Verlustfunktion, die die Seltenheit echter CTCs widerspiegelt, um streng gegenüber Fehlalarmen zu sein und zugleich ungewöhnliche Zellen zu erfassen.
Das System im Praxistest
In kontrollierten Experimenten, bei denen bekannte Mengen an Prostatakrebszellen in gesundes Blut gegeben wurden, konnte die Plattform etwa 60 % dieser Zellen an einem gewählten Betriebspunkt zurückgewinnen und gleichzeitig die falsch‑positiven Treffer unter einem pro Milliliter halten — selbst bei großzügigen Detektionsschwellen. Zur weiteren Verfeinerung misst das System zudem zwei fluoreszente Signale von Antikörpern gegen PSMA, einen prostataspezifischen Marker, und EpCAM. Bei Patiententests musste eine als CTC gezählte Zelle sowohl die holografisch‑deep‑learning‑Schwelle passieren als auch ein starkes PSMA‑Signal zeigen, wodurch labelfreie Forminformationen mit gezielter molekularer Bestätigung kombiniert werden. Als die Forschenden dies bei 13 Männern mit fortgeschrittenem Prostatakrebs und 8 gesunden männlichen Spendern anwandten, zeigte die Krebsgruppe deutlich höhere CTC‑Zahlen (Median 12,5 Zellen pro mL) als die Kontrollen (Median 1,5 Zellen pro mL). Auffällig war, dass nur etwa ein Drittel der PSMA‑positiven Zellen EpCAM trug, was nahelegt, dass Tests, die ausschließlich auf EpCAM setzen, in diesen Patienten die Mehrheit der Tumorzellen übersehen würden.
Welche Bedeutung das für Patientinnen und Patienten haben könnte
Indem eine Standardblutentnahme in einen reichhaltigen, automatisierten Scan nach seltenen Krebszellen verwandelt wird, weist diese Plattform den Weg zu praktischeren „Liquid Biopsies“. Die Kombination aus labelfreier Holografie, gezielter Fluoreszenz und Deep Learning erreicht eine niedrige Fehlalarmrate und erfasst gleichzeitig CTCs, die traditionelle markerbasierte Systeme übersehen. Aktuell zeigt sich dies in einer besseren Trennung von Krebspatienten und gesunden Personen in einer Pilotstudie zu Prostatakrebs. Perspektivisch könnte der Ansatz auf viele Tumortypen und Körperflüssigkeiten adaptiert werden und eines Tages ganz ohne fluoreszente Marker auskommen, allein basierend auf dem Aussehen der Zellen im holografischen Raum. Wenn dies in größeren, heterogenen Studien vollständig bestätigt wird, könnten solche Systeme Ärztinnen und Ärzten ermöglichen, das Auf und Ab von Krebs über die Zeit mit einem einfachen Bluttest zu verfolgen, Behandlungen früher anzupassen und lebende Tumorzellen für detaillierte molekulare Analysen zu gewinnen — ganz ohne Skalpell.
Zitation: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Schlüsselwörter: zirkulierende Tumorzellen, Liquid Biopsy, digitale holografische Mikroskopie, Deep‑Learning‑Diagnostik, Prostatakrebs