Clear Sky Science · es
Detección de células tumorales circulantes en pacientes con cáncer mediante holografía en flujo y aprendizaje profundo
Encontrar pistas de cáncer en una simple extracción de sangre
El cáncer a menudo se disemina mucho antes de que un tumor sea visible en una exploración, desprendiendo células errantes hacia el torrente sanguíneo. Estas células “tumorales circulantes” son raras pero contienen pistas poderosas: pueden señalar la presencia del cáncer, seguir cómo responde al tratamiento y apuntar hacia lo que podría ocurrir después. Este artículo describe una nueva tecnología capaz de cribar miles de millones de células sanguíneas para encontrar estas pocas células peligrosas de forma rápida, delicada y con alta precisión, abriendo la posibilidad de pruebas de sangre de rutina que monitoreen el cáncer en tiempo real.
Por qué importan estas células tan raras
Las células tumorales circulantes (CTC) son células cancerosas que se han separado de un tumor primario o metastásico y han entrado en la sangre. Incluso en enfermedad avanzada, un mililitro de sangre puede contener miles de millones de glóbulos rojos y blancos normales pero solo un puñado de CTC, a veces menos de una. Sin embargo, su número y comportamiento están estrechamente ligados a la agresividad del tumor, a si resiste la terapia y a la supervivencia probable del paciente. Los métodos estándar para encontrarlas a menudo dependen de marcadores de superficie como EpCAM, proteïnas externas de muchas células cancerosas epiteliales. Pero conforme los tumores evolucionan y cambian de estado, estos marcadores pueden disminuir, lo que significa que algunas de las células más peligrosas pueden eludir la detección.
Limitaciones de las pruebas actuales
Muchas pruebas sanguíneas existentes para CTC intentan capturar células por sus “etiquetas” moleculares o por rasgos físicos como tamaño y rigidez. Los sistemas basados en marcadores, como los que extraen magnéticamente células que portan EpCAM, pueden pasar por alto células tumorales que han apagado esos marcadores durante un proceso de cambio de forma vinculado a la metástasis. Los filtros basados en tamaño o densidad también pueden fallar, porque algunas células tumorales son similares en tamaño y textura a los leucocitos normales. Los dispositivos que combinan varias técnicas —chips microfluídicos complejos, imanes o fuerzas acústicas— ganan sensibilidad pero suelen aumentar la complejidad, el coste y la pérdida celular. Como resultado, muchas plataformas tienen dificultades para ser a la vez lo suficientemente simples para uso clínico rutinario y lo bastante sensibles para capturar la diversidad completa de las células tumorales.
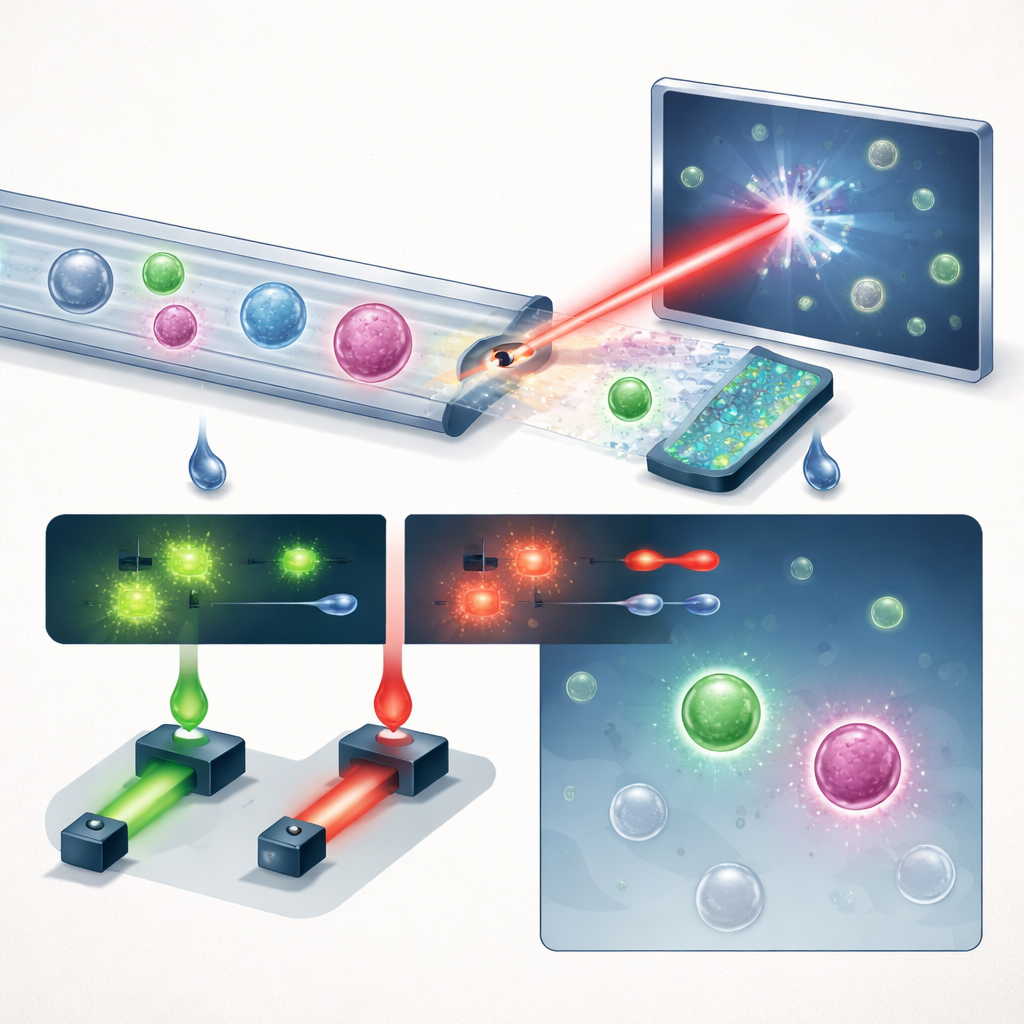
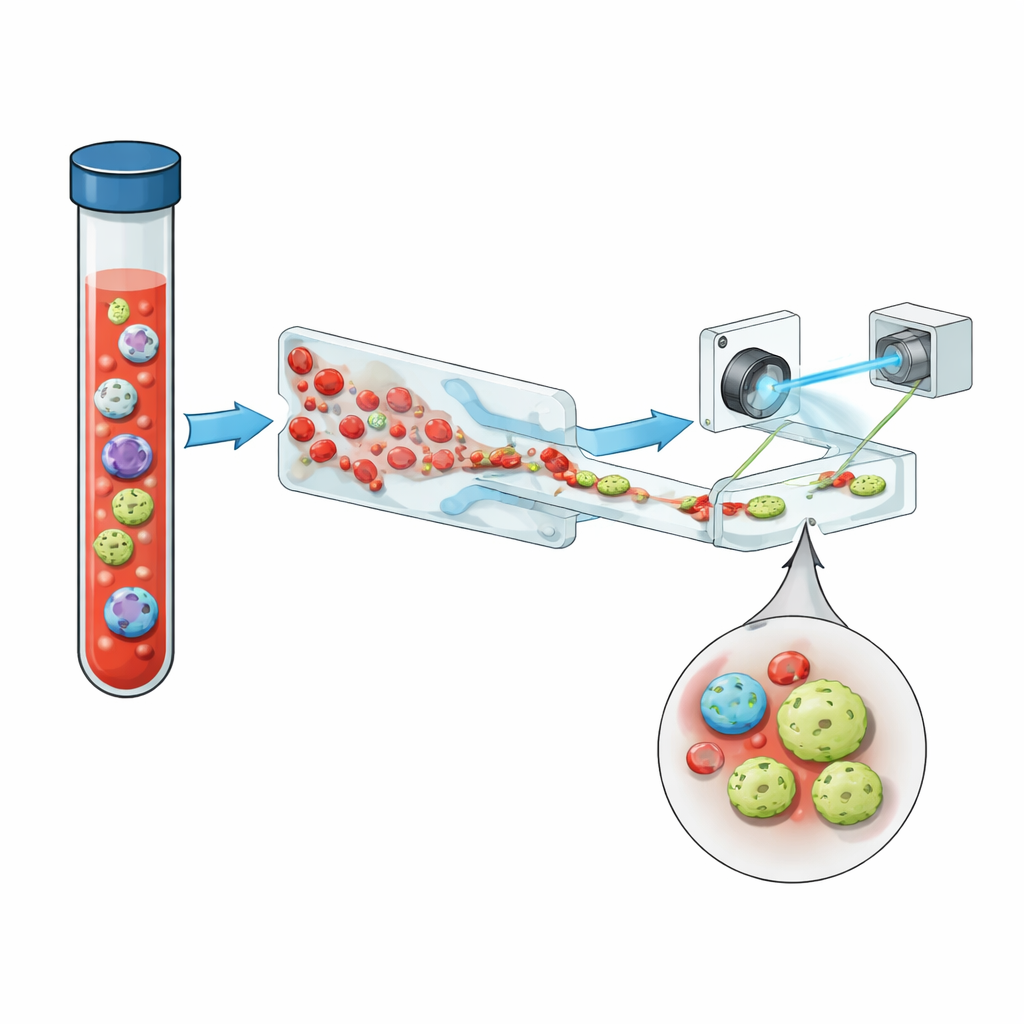
Una nueva forma de ver células en flujo
El equipo presenta un sistema compacto que encadena tres ideas clave: manejo inteligente de fluidos, imagen holográfica y aprendizaje profundo, con una dosis útil de fluorescencia. Primero, sangre entera circula por un chip microfluídico “en sierra” que elimina más del 99,999 % de los glóbulos rojos y casi todos los glóbulos blancos, manteniendo la gran mayoría de las células tumorales. Esto transforma una muestra abarrotada en otra donde las células raras tienen más posibilidades de destacar. El flujo enriquecido pasa luego por un canal recto simple bajo un láser violeta pulsado. En lugar de tomar imágenes planas, el sistema registra hologramas —patrones de interferencia que codifican tanto el brillo como el grosor óptico de cada célula— capturando sutiles estructuras tridimensionales en una sola instantánea.
Entrenar una red neuronal para detectar las que son diferentes
Dado que las CTC reales son escasas, recolectar suficiente ejemplos de pacientes para entrenar un algoritmo no es práctico. Los investigadores enseñaron en su lugar a un modelo de aprendizaje profundo a reconocer todo aquello que no se parece a la sangre ordinaria. Le introdujeron millones de hologramas de donantes sanos, mostrando la variedad completa de glóbulos blancos, rojos y fragmentos, y los equilibraron con imágenes de numerosas líneas celulares cancerosas cultivadas en el laboratorio. Una red neuronal especializada convierte cada holograma en un mapa de calor de posibles ubicaciones tumorales, tratando las células como puntos luminosos en lugar de cajones delimitadores. Para ampliar el entrenamiento sin etiquetado manual infinito, un modelo auxiliar primero marca todas las células en imágenes de poblaciones puras de células cancerosas; el modelo principal utiliza esas “pseudoetiquetas”, además de una función de pérdida ajustada para reflejar lo raras que son las CTC reales, para aprender a ser estricto con las falsas alarmas mientras sigue detectando células inusuales.
Poner el sistema a prueba
En experimentos controlados donde se añadieron números conocidos de células de cáncer de próstata a sangre sana, la plataforma recuperó alrededor del 60 % de esas células en un punto de funcionamiento elegido, manteniendo a la vez menos de una falsa positiva por mililitro —incluso con umbrales de detección permisivos. Para afinar aún más sus decisiones, el sistema también mide dos señales fluorescentes de anticuerpos contra PSMA, un marcador específico de próstata, y EpCAM. Durante las pruebas con pacientes, una célula se contaba como CTC solo si superaba el umbral del aprendizaje profundo holográfico y además mostraba una señal PSMA intensa, combinando información morfológica sin marcadores con confirmación molecular dirigida. Cuando los investigadores aplicaron esto a 13 hombres con cáncer de próstata avanzado y 8 donantes masculinos sanos, el grupo canceroso mostró recuentos de CTC mucho más altos (mediana 12,5 células por mL) que los controles (mediana 1,5 células por mL). De forma llamativa, solo alrededor de un tercio de las células PSMA‑positivas portaban EpCAM, lo que sugiere que las pruebas basadas únicamente en EpCAM perderían la mayoría de las células tumorales en estos pacientes.
Qué podría significar esto para los pacientes
Al convertir una extracción de sangre estándar en un escaneo rico y automatizado para células tumorales raras, esta plataforma apunta hacia biopsias líquidas más prácticas. Su combinación de holografía sin marcaje, fluorescencia dirigida y aprendizaje profundo alcanza una baja tasa de falsos positivos al tiempo que captura CTC que los sistemas tradicionales basados en marcadores pasan por alto. Hoy por hoy, eso implica una mejor separación entre pacientes con cáncer y personas sanas en un estudio piloto de cáncer de próstata. Mirando al futuro, el enfoque podría adaptarse a muchos tipos de tumores y fluidos, y eventualmente funcionar sin etiquetas fluorescentes, confiando únicamente en la apariencia de las células en el espacio holográfico. Si se demuestra plenamente en ensayos mayores y diversos, tales sistemas podrían permitir a los médicos seguir la ascensión y el descenso del cáncer a lo largo del tiempo con una simple prueba sanguínea, ajustar tratamientos antes y recuperar células tumorales vivas para análisis moleculares detallados —todo sin bisturí.
Cita: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Palabras clave: células tumorales circulantes, biopsia líquida, microscopía holográfica digital, diagnóstico por aprendizaje profundo, cáncer de próstata