Clear Sky Science · fr
Détection des cellules tumorales circulantes chez des patients atteints de cancer à l’aide d’holographie en flux et d’apprentissage profond
Détecter des indices de cancer dans une simple prise de sang
Le cancer se propage souvent bien avant qu’une tumeur n’apparaisse sur une image, en relâchant des cellules isolées dans la circulation sanguine. Ces « cellules tumorales circulantes » errantes sont rares mais précieuses : elles peuvent signaler la présence d’un cancer, suivre sa réponse au traitement et donner des indications sur son évolution future. Cet article décrit une nouvelle technologie capable de trier des milliards de cellules sanguines pour retrouver rapidement, délicatement et avec une grande précision ces rares éléments dangereux — ouvrant la voie à des prises de sang de routine permettant de suivre le cancer en temps réel.
Pourquoi ces cellules rares comptent
Les cellules tumorales circulantes (CTC) sont des cellules cancéreuses qui se sont détachées d’une tumeur primaire ou métastatique et sont passées dans le sang. Même dans les maladies avancées, un millilitre de sang peut contenir des milliards de globules rouges et blancs normaux mais seulement une poignée de CTC — parfois moins d’une seule. Pourtant, leur nombre et leur comportement sont étroitement liés à l’agressivité d’une tumeur, à sa résistance aux traitements et à la durée de vie probable d’un patient. Les méthodes standard pour les détecter s’appuient souvent sur des marqueurs de surface tels qu’EpCAM, des protéines présentes à la surface de nombreuses cellules cancéreuses épithéliales. Mais à mesure que les tumeurs évoluent et changent d’état, ces marqueurs peuvent s’effacer, ce qui fait que certaines des cellules les plus dangereuses échappent à la détection.
Limites des tests actuels
De nombreux tests sanguins existants pour les CTC tentent de capturer les cellules par leurs « étiquettes » moléculaires ou par des caractéristiques physiques comme la taille et la rigidité. Les systèmes basés sur des marqueurs, comme ceux qui extraient magnétiquement les cellules portant EpCAM, peuvent manquer des cellules tumorales qui ont coupé l’expression de ces marqueurs lors d’un processus de métamorphose lié aux métastases. Les filtres basés sur la taille ou la densité peuvent aussi échouer, car certaines cellules tumorales ressemblent en taille et en texture aux globules blancs normaux. Les dispositifs combinant plusieurs astuces — puces microfluidiques complexes, aimants ou forces acoustiques — gagnent en sensibilité mais au prix d’une plus grande complexité, d’un coût élevé et de pertes cellulaires. En conséquence, de nombreuses plateformes peinent à être à la fois suffisamment simples pour un usage clinique courant et suffisamment sensibles pour capturer la pleine diversité des cellules tumorales.
Une nouvelle façon d’observer les cellules en flux
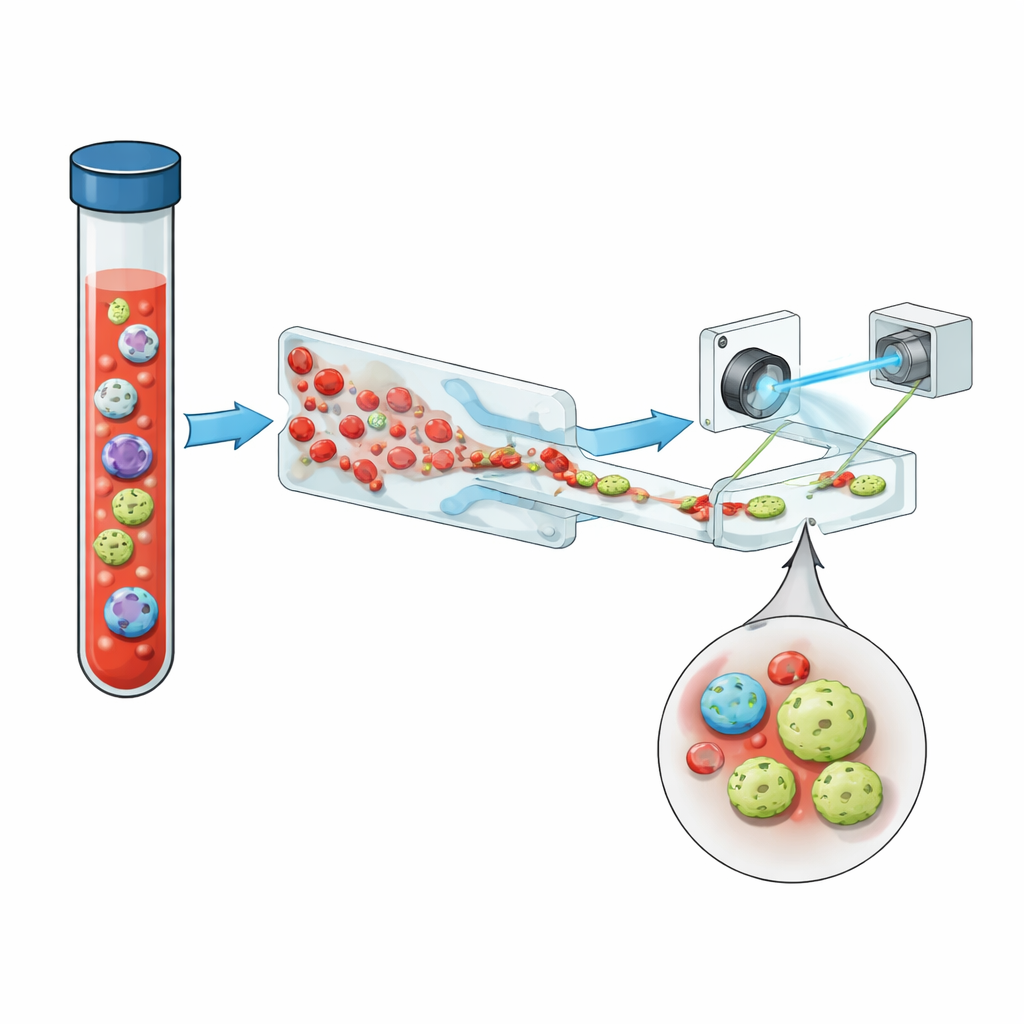
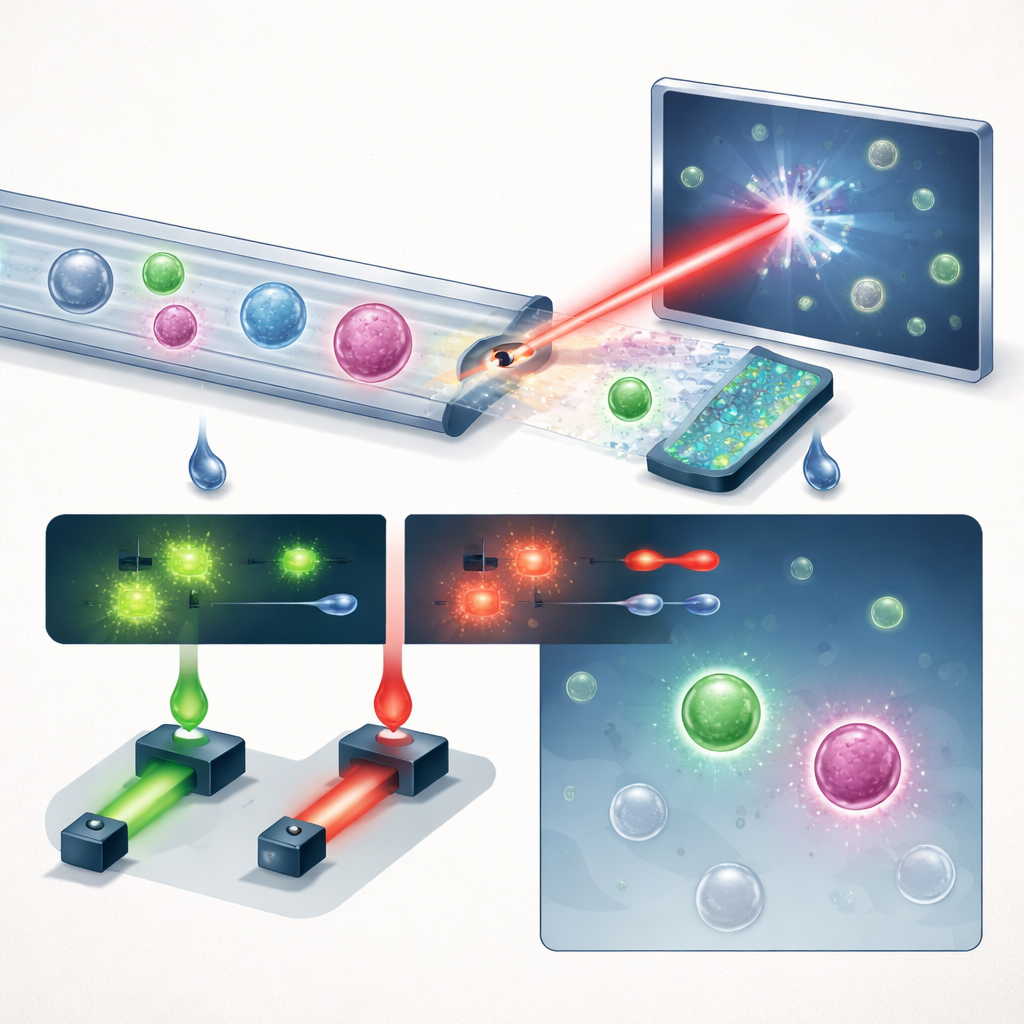
L’équipe présente un système compact qui enchaîne trois idées clés : une gestion des fluides intelligente, l’imagerie holographique et l’apprentissage profond, avec une dose utile de fluorescence. D’abord, le sang total est fait passer dans une puce microfluidique en « dents de scie » qui élimine plus de 99,999 % des globules rouges et presque tous les globules blancs, tout en conservant la grande majorité des cellules tumorales. Cela transforme un échantillon surchargé en un flux où les cellules rares ont davantage de chances de ressortir. Le flux enrichi passe ensuite dans un canal droit et simple sous un laser violet pulsé. Plutôt que de prendre des images plates, le système enregistre des hologrammes — des motifs d’interférence qui codent à la fois l’intensité et l’épaisseur optique de chaque cellule, saisissant une structure tridimensionnelle subtile en une seule prise.
Apprendre à un réseau neuronal à repérer les éléments anormaux
Parce que les CTC véritables sont rares, collecter directement suffisamment d’exemples réels de patients pour entraîner un algorithme est impraticable. Les chercheurs ont donc appris à un modèle d’apprentissage profond à reconnaître tout ce qui ne ressemble pas au sang ordinaire. Ils l’ont alimenté de millions d’hologrammes provenant de donneurs sains, montrant la pleine variété des globules blancs, rouges et des débris, et les ont équilibrés avec des images de nombreuses lignées cellulaires cancéreuses cultivées en laboratoire. Un réseau neuronal spécialisé convertit chaque hologramme en une carte de chaleur des emplacements probables de tumeurs, traitant les cellules comme des points lumineux clés plutôt que comme des boîtes. Pour élargir l’entraînement sans étiquetage manuel infini, un modèle d’aide marque d’abord toutes les cellules dans les images de cellules cancéreuses pures ; le modèle principal utilise alors ces « pseudo-étiquettes », plus une fonction de perte ajustée pour refléter la rareté des CTC réelles, afin d’apprendre à être strict sur les fausses alertes tout en continuant à détecter les cellules inhabituelles.
Évaluer le système
Dans des expériences contrôlées où des nombres connus de cellules de cancer de la prostate étaient ajoutés à du sang sain, la plateforme a retrouvé environ 60 % de ces cellules à un point de fonctionnement choisi, tout en maintenant les faux positifs sous une par millilitre — même à des seuils de détection larges. Pour affiner davantage ses décisions, le système mesure aussi deux signaux fluorescents issus d’anticorps contre le PSMA, un marqueur spécifique de la prostate, et contre EpCAM. Lors des tests patients, une cellule était comptée comme CTC si elle dépassait à la fois le seuil holographique d’apprentissage profond et présentait un signal PSMA fort, combinant l’information de forme sans marquage avec une confirmation moléculaire ciblée. Lorsqu’ils ont appliqué cette méthode à 13 hommes atteints d’un cancer de la prostate avancé et à 8 donneurs masculins sains, le groupe cancer a montré des nombres de CTC nettement plus élevés (médiane 12,5 cellules par mL) que les témoins (médiane 1,5 cellule par mL). Fait remarquable, seulement environ un tiers des cellules PSMA‑positives portaient EpCAM, ce qui suggère que les tests reposant uniquement sur EpCAM manqueraient la majorité des cellules tumorales chez ces patients.
Ce que cela pourrait signifier pour les patients
En transformant une prise de sang standard en un scan riche et automatisé des cellules cancéreuses rares, cette plateforme ouvre la voie à des « biopsies liquides » plus pratiques. Son mélange d’holographie sans marquage, de fluorescence ciblée et d’apprentissage profond atteint un faible taux de faux positifs tout en capturant des CTC que les systèmes traditionnels basés sur des marqueurs négligent. Aujourd’hui, cela se traduit par une meilleure séparation des patients cancéreux et des individus sains dans une étude pilote sur le cancer de la prostate. À l’avenir, l’approche pourrait être adaptée à de nombreux types de tumeurs et de fluides, et pourrait finir par fonctionner sans aucun marqueur fluorescent, en se basant uniquement sur l’apparence des cellules en espace holographique. Si elle est pleinement validée dans des essais plus larges et diversifiés, une telle technologie permettrait aux médecins de suivre l’évolution du cancer au fil du temps avec une simple prise de sang, d’ajuster les traitements plus tôt et de récupérer des cellules tumorales vivantes pour des analyses moléculaires détaillées — le tout sans scalpel.
Citation: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Mots-clés: cellules tumorales circulantes, biopsie liquide, microscopie holographique numérique, diagnostic par apprentissage profond, cancer de la prostate