Clear Sky Science · pl
Wykrywanie krążących komórek nowotworowych u pacjentów onkologicznych za pomocą holografii w przepływie i głębokiego uczenia
Odnajdywanie wskazówek o raku w prostym pobraniu krwi
Nowotwór często rozprzestrzenia się długo przed pojawieniem się guza w badaniu obrazowym, zrzucając luźne komórki do krwiobiegu. Te wędrujące „krążące komórki nowotworowe” są rzadkie, ale dają ważne wskazówki: mogą sygnalizować obecność choroby, śledzić odpowiedź na leczenie oraz dawać wskazówki co do dalszego przebiegu. W artykule opisano nową technologię, która potrafi przesiać miliardy komórek krwi, aby szybko, delikatnie i z dużą dokładnością odnaleźć te kilka niebezpiecznych egzemplarzy — co otwiera perspektywę rutynowych badań krwi monitorujących raka w czasie rzeczywistym.
Dlaczego te rzadkie komórki mają znaczenie
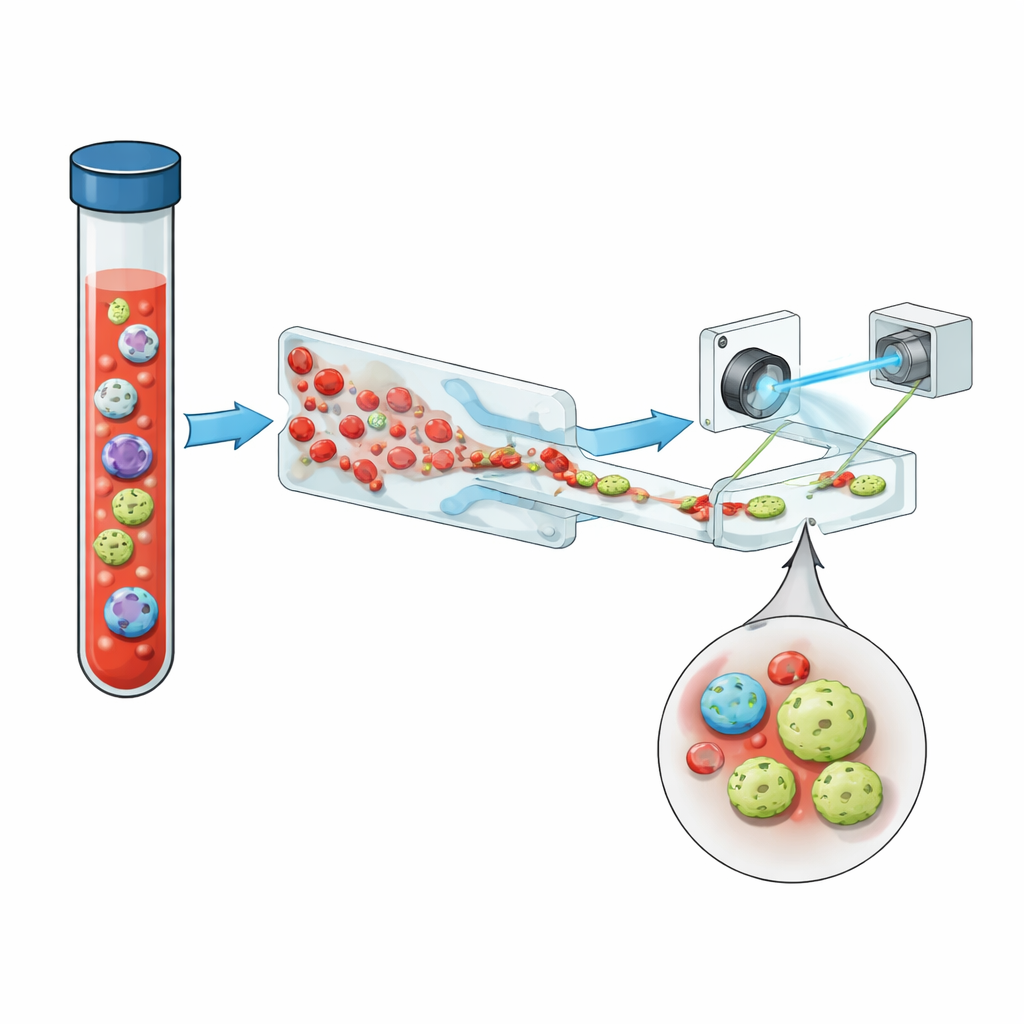
Krążące komórki nowotworowe (CTC) to komórki nowotworowe, które oderwały się od guza pierwotnego lub przerzutowego i przedostały się do krwiobiegu. Nawet w zaawansowanej chorobie mililitr krwi może zawierać miliardy normalnych krwinek czerwonych i białych, a tylko garstkę CTC — czasem mniej niż jedną. Tym niemniej ich liczba i zachowanie są silnie powiązane z agresywnością guza, opornością na terapię i przewidywanym czasem przeżycia pacjenta. Standardowe metody ich wykrywania często opierają się na markerach powierzchniowych, takich jak EpCAM — białka występujące na zewnątrz wielu komórek nowotworów nabłonkowych. Jednak w miarę jak guzy ewoluują i zmieniają swój stan, te markery mogą zanikać, co oznacza, że niektóre z najbardziej niebezpiecznych komórek mogą umknąć wykryciu.
Niedostatki obecnych testów
Wiele istniejących testów krwi na CTC stara się wychwycić komórki po ich molekularnych „metkach” lub cechach fizycznych, takich jak rozmiar i sztywność. Systemy oparte na markerach, na przykład te magnetycznie wyciągające komórki z EpCAM, mogą przeoczyć komórki nowotworowe, które wyłączyły te markery w trakcie procesu zmiany kształtu związanego z tworzeniem przerzutów. Filtry oparte na rozmiarze lub gęstości też mogą zawodzić, ponieważ niektóre komórki nowotworowe mają rozmiar i konsystencję podobne do normalnych białych krwinek. Urządzenia łączące kilka trików — skomplikowane chipy mikroprzepływowe, magnesy czy siły akustyczne — zyskują na czułości, ale często kosztem większej złożoności, kosztów i utraty komórek. W rezultacie wiele platform ma trudność, by być zarówno na tyle prostymi do rutynowego stosowania klinicznego, jak i wystarczająco czułymi, by wychwycić pełną różnorodność komórek nowotworowych.
Nowy sposób obserwacji komórek w przepływie
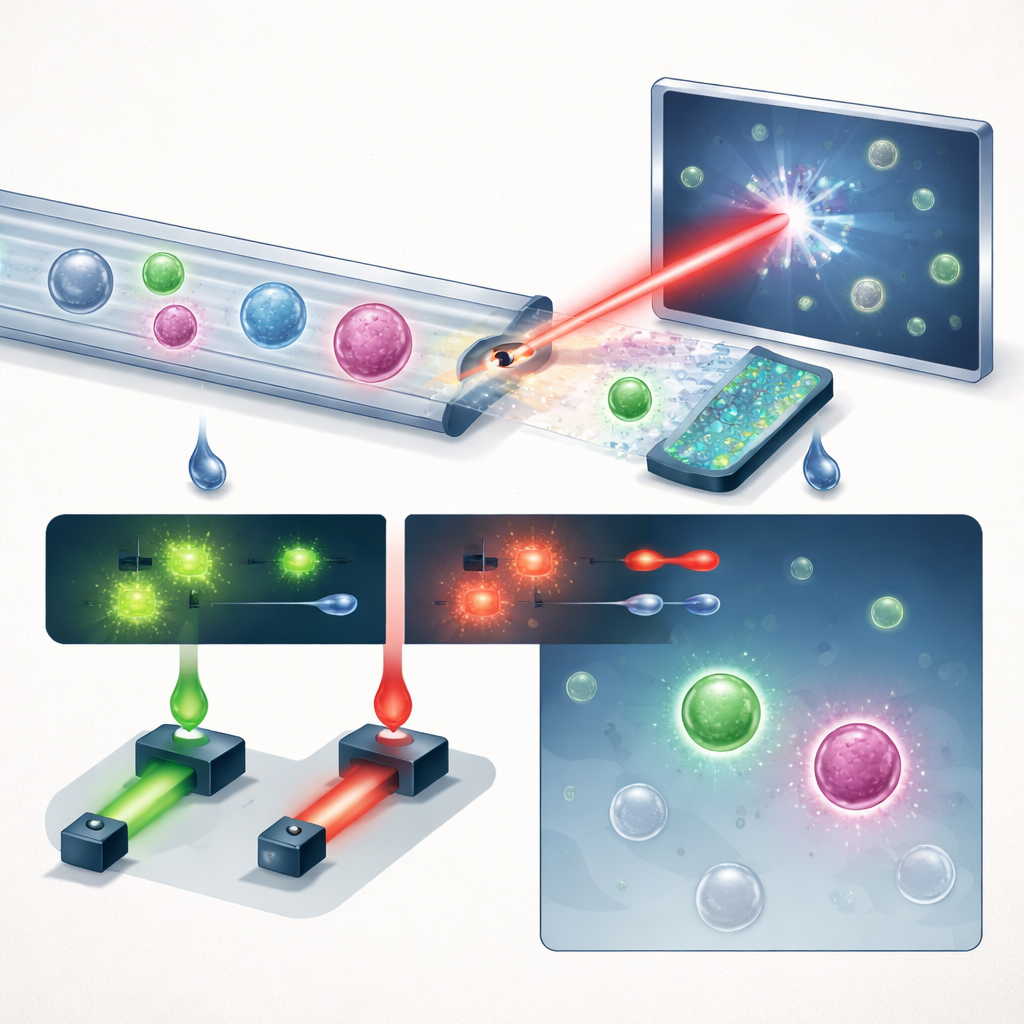
Zespół przedstawia kompaktowy system łączący trzy kluczowe idee: inteligentne zarządzanie płynem, obrazowanie holograficzne i głębokie uczenie, uzupełnione przez fluorescencję. Najpierw całą krew przepuszcza się przez mikroprzepływowy chip o kształcie „ząbkowanej piły”, który usuwa ponad 99,999% erytrocytów i niemal wszystkie leukocyty, zachowując przy tym zdecydowaną większość komórek nowotworowych. To zamienia zatłoczoną próbkę w próbkę, w której rzadkie komórki mają większe szanse się wyróżnić. Wzbogacony strumień następnie przepływa prostym kanałem pod pulsującym fioletowym laserem. Zamiast robić płaskie zdjęcia, system rejestruje hologramy — wzory interferencyjne, które kodują zarówno jasność, jak i grubość optyczną każdej komórki, uchwycając subtelną strukturę trójwymiarową w jednej migawce.
Nauka sieci neuronowej rozpoznawania odmiennych komórek
Ponieważ prawdziwe CTC są rzadkie, bezpośrednie zebranie wystarczającej liczby rzeczywistych próbek pacjentów do treningu algorytmu jest niepraktyczne. Badacze zamiast tego nauczyli model głębokiego uczenia rozpoznawania wszystkiego, co nie wygląda jak zwykła krew. Nakarmili go milionami hologramów od zdrowych dawców, pokazując pełne zróżnicowanie białych i czerwonych krwinek oraz zanieczyszczeń, i wyważyli je obrazami z wielu różnych linii komórkowych nowotworów hodowanych w laboratorium. Specjalistyczna sieć neuronowa konwertuje każdy hologram na mapę cieplną prawdopodobnych lokalizacji komórek nowotworowych, traktując komórki jako świetliste punkty kluczowe zamiast ramek. Aby skalować trening bez nieskończonego ręcznego oznaczania, model pomocniczy najpierw oznacza wszystkie komórki na czystych obrazach komórek nowotworowych; główny model następnie używa tych „pseudo-etykiet” oraz funkcji straty dostrojonej do rzadkości prawdziwych CTC, ucząc się rygorystycznie traktować fałszywe alarmy, a jednocześnie łapać nietypowe komórki.
Testy systemu
W kontrolowanych eksperymentach, gdzie znane liczby komórek raka prostaty były dosypywane do zdrowej krwi, platforma odzyskała około 60% tych komórek przy wybranym punkcie pracy, utrzymując jednocześnie liczbę fałszywych pozytywów poniżej jednego na mililitr — nawet przy liberalnych progach detekcji. Aby jeszcze bardziej wyostrzyć decyzje, system mierzy również dwa sygnały fluorescencyjne z przeciwciał skierowanych przeciw PSMA, markerowi specyficznemu dla prostaty, oraz EpCAM. Podczas badań z pacjentami komórka uznawana za CTC musiała zarówno przekroczyć próg holograficznego modelu głębokiego uczenia, jak i wykazywać silny sygnał PSMA, łącząc informację o kształcie bez znakowania z ukierunkowanym potwierdzeniem molekularnym. Gdy badacze zastosowali to u 13 mężczyzn z zaawansowanym rakiem prostaty i 8 zdrowych dawców płci męskiej, grupa chorych wykazała znacznie wyższe liczby CTC (mediana 12,5 komórek na mL) niż grupa kontrolna (mediana 1,5 komórki na mL). Co istotne, tylko około jedna trzecia komórek pozytywnych na PSMA miała też EpCAM, co sugeruje, że testy polegające wyłącznie na EpCAM przeoczyłyby większość komórek nowotworowych u tych pacjentów.
Co to może znaczyć dla pacjentów
Przekształcając standardowe pobranie krwi w bogate, zautomatyzowane skanowanie rzadkich komórek nowotworowych, ta platforma wskazuje drogę do bardziej praktycznych „biopsji płynnych”. Jej połączenie holografii bez znakowania, ukierunkowanej fluorescencji i głębokiego uczenia osiąga niski odsetek fałszywych pozytywów, jednocześnie wychwytując CTC, które tradycyjne systemy oparte na markerach pomijają. Dziś oznacza to lepsze rozróżnienie pacjentów onkologicznych od zdrowych osób w pilotażowym badaniu raka prostaty. W przyszłości podejście to można by dostosować do wielu typów nowotworów i płynów ustrojowych, a ostatecznie może działać bez żadnych znaczników fluorescencyjnych, polegając wyłącznie na wyglądzie komórek w przestrzeni holograficznej. Jeśli zostanie w pełni potwierdzone w większych, zróżnicowanych badaniach, takie systemy mogłyby pozwolić lekarzom śledzić wzrost i regresję raka w czasie za pomocą prostego badania krwi, szybciej dostosowywać terapie i odzyskiwać żywe komórki nowotworowe do szczegółowej analizy molekularnej — wszystko bez skalpela.
Cytowanie: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Słowa kluczowe: krążące komórki nowotworowe, biopsja płynna, cyfrowa mikroskopia holograficzna, diagnostyka z użyciem głębokiego uczenia, rak prostaty