Clear Sky Science · it
Rilevamento delle cellule tumorali circolanti nei pazienti oncologici mediante olografia in flusso con deep learning
Trovare indizi di cancro con un semplice prelievo di sangue
Il cancro spesso si diffonde molto prima che un tumore sia visibile a una scansione, rilasciando cellule vaganti nel flusso sanguigno. Queste “cellule tumorali circolanti” sono rare ma contengono indizi potenti: possono segnalare la presenza del cancro, monitorare la risposta alle terapie e suggerire come potrebbe evolvere la malattia. Questo articolo descrive una nuova tecnologia in grado di setacciare miliardi di cellule del sangue per trovare in fretta queste poche cellule pericolose, in modo delicato e con elevata accuratezza—aprendo la possibilità di esami ematici di routine che tracciano il cancro in tempo reale.
Perché queste cellule rare sono importanti
Le cellule tumorali circolanti (CTC) sono cellule cancerose che si sono staccate da un tumore primario o metastatico e sono finiti nel flusso sanguigno. Anche nelle fasi avanzate della malattia, un millilitro di sangue può contenere miliardi di globuli rossi e bianchi normali ma solo poche CTC—talvolta meno di una. Eppure il loro numero e il loro comportamento sono strettamente legati all’aggressività del tumore, alla resistenza alle terapie e alla prognosi del paziente. I metodi standard per trovarle spesso si basano su marcatori di superficie come l’EpCAM, proteine presenti sulla membrana di molte cellule tumorali epiteliali. Ma man mano che i tumori evolvono e cambiano stato, questi marcatori possono attenuarsi, facendo sì che alcune delle cellule più pericolose sfuggano alla rilevazione.
Limiti dei test attuali
Molti test ematici esistenti per le CTC cercano di catturare le cellule tramite i loro “cartellini” molecolari o tramite caratteristiche fisiche come dimensione e rigidità. I sistemi basati sui marcatori, come quelli che estraggono magneticamente le cellule che esprimono EpCAM, possono mancare cellule tumorali che hanno spento questi marcatori durante un processo di transizione associato alla metastasi. Filtri basati su dimensioni o densità possono fallire perché alcune cellule tumorali hanno dimensioni e consistenza simili ai normali globuli bianchi. Dispositivi che combinano più stratagemmi—chip microfluidici complessi, magneti o forze acustiche—aumentano la sensibilità ma spesso a costo di maggiore complessità, spesa e perdita di cellule. Di conseguenza, molte piattaforme faticano a essere abbastanza semplici per l’uso clinico di routine e allo stesso tempo sensibili per catturare l’intera diversità delle cellule tumorali.
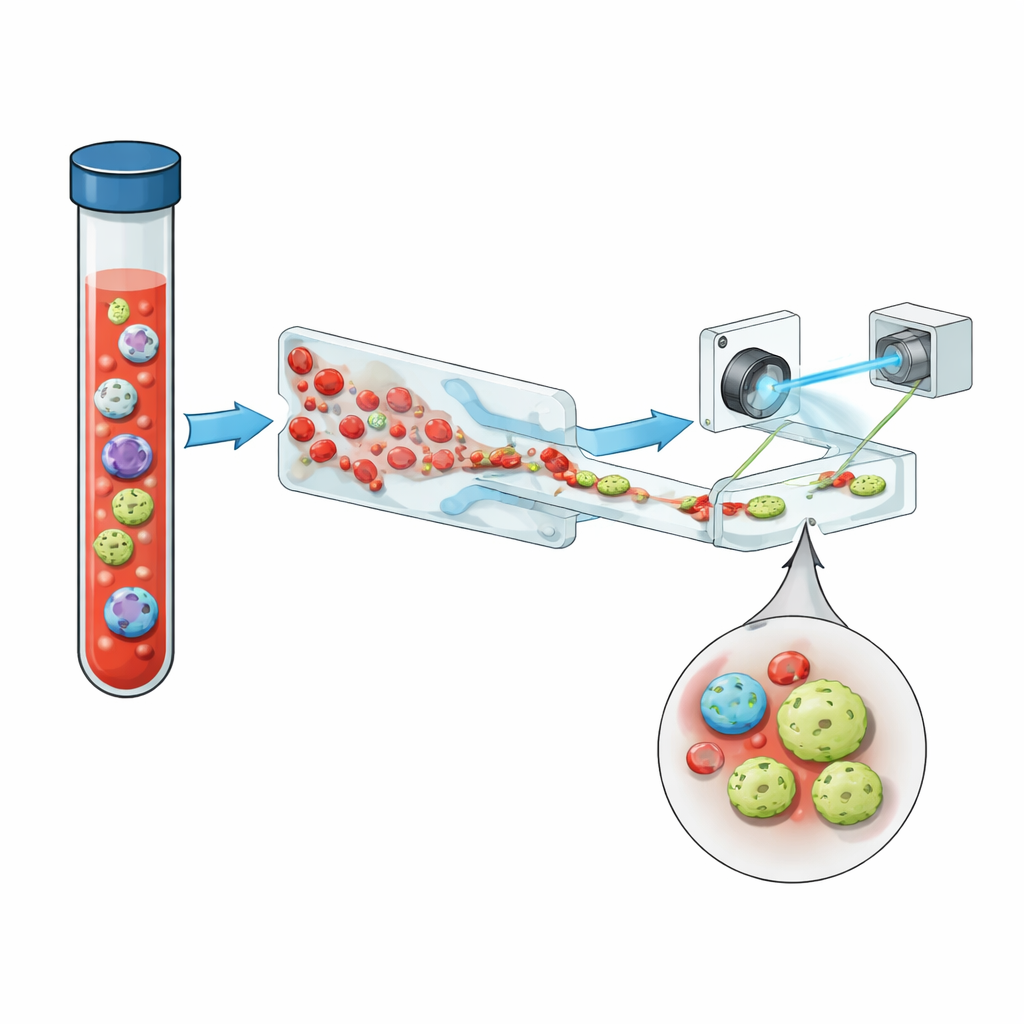
Un nuovo modo di vedere le cellule in flusso
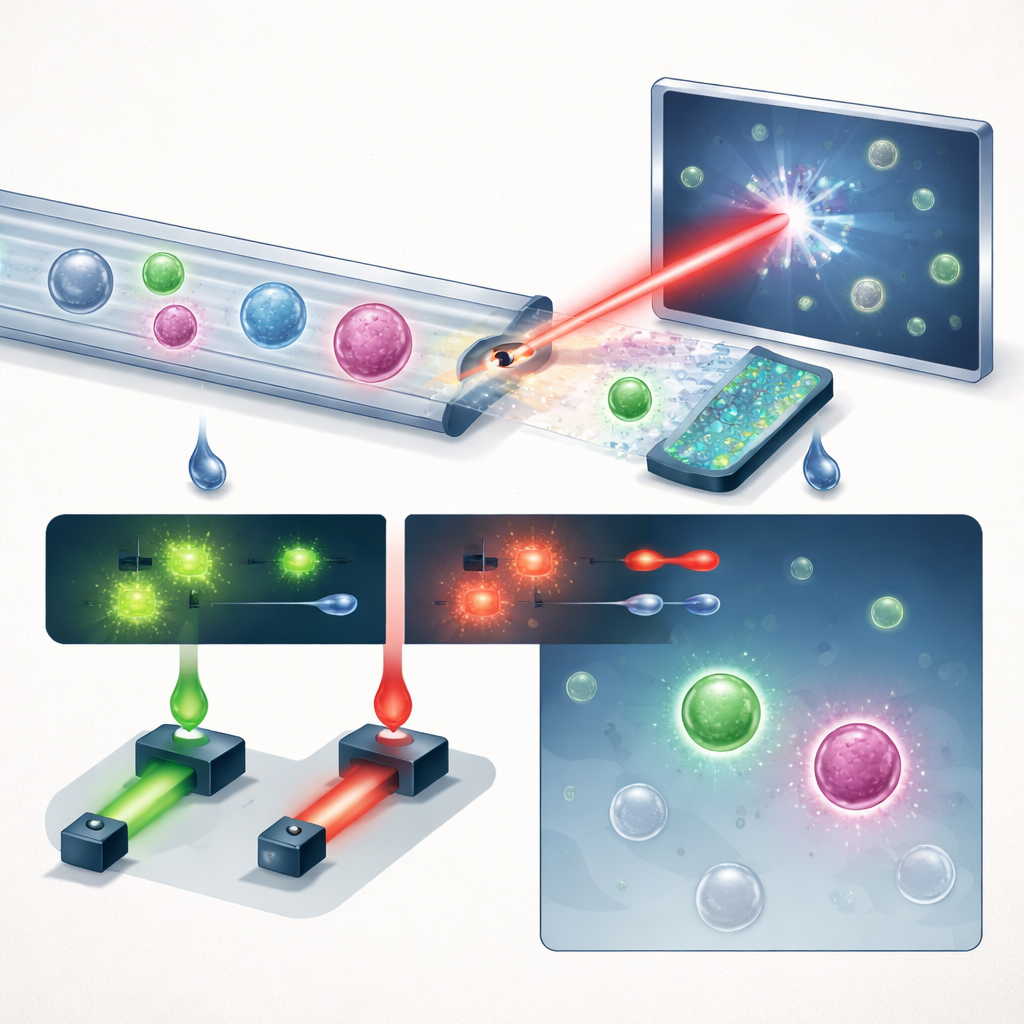
Il team presenta un sistema compatto che unisce tre idee chiave: gestione intelligente dei fluidi, imaging olografico e deep learning, con un utile apporto di fluorescenza. Innanzitutto, il sangue intero viene fatto scorrere attraverso un chip microfluidico a “denti di sega” che rimuove più del 99,999% dei globuli rossi e quasi tutti i globuli bianchi, preservando però la grande maggioranza delle cellule tumorali. Questo trasforma un campione affollato in uno in cui le cellule rare possono emergere più facilmente. Il flusso arricchito passa quindi attraverso un canale rettilineo semplice sotto un laser violetto pulsato. Invece di acquisire immagini piatte, il sistema registra ologrammi—pattern di interferenza che codificano sia la brillantezza sia lo spessore ottico di ogni cellula, catturando sottili strutture tridimensionali in un’unica istantanea.
Insegnare a una rete neurale a riconoscere gli elementi anomali
Poiché le vere CTC sono scarse, raccogliere direttamente abbastanza esempi di pazienti reali per addestrare un algoritmo è poco pratico. I ricercatori hanno quindi insegnato a un modello di deep learning a riconoscere tutto ciò che non somiglia al sangue ordinario. Gli hanno fornito milioni di ologrammi da donatori sani, mostrando tutta la varietà di globuli bianchi, rossi e detriti, e li hanno bilanciati con immagini di molte linee cellulari tumorali cresciute in laboratorio. Una rete neurale specializzata converte ogni ologramma in una mappa di probabilità delle posizioni potenziali di tumore, trattando le cellule come punti chiave luminescenti anziché come riquadri. Per ampliare l’addestramento senza etichettature manuali infinite, un modello di supporto prima segna tutte le cellule nelle immagini di cellule tumorali pure; il modello principale usa quindi queste “pseudo-etichettature”, insieme a una funzione di perdita tarata per riflettere quanto sono rare le vere CTC, per imparare a essere severo con i falsi positivi pur catturando le cellule insolite.
Mettere il sistema alla prova
In esperimenti controllati in cui numeri noti di cellule di cancro alla prostata sono stati aggiunti a sangue sano, la piattaforma ha recuperato circa il 60% di queste cellule a un punto operativo scelto, mantenendo i falsi positivi sotto uno per millilitro—anche con soglie di rilevamento permissive. Per affinare ulteriormente le decisioni, il sistema misura anche due segnali fluorescenti da anticorpi contro PSMA, un marcatore specifico della prostata, ed EpCAM. Durante i test sui pazienti, una cellula veniva conteggiata come CTC solo se superava la soglia del deep learning olografico e mostrava un forte segnale PSMA, combinando informazioni sulla morfologia senza marcatori con una conferma molecolare mirata. Quando i ricercatori hanno applicato questo a 13 uomini con cancro alla prostata avanzato e 8 donatori maschi sani, il gruppo di pazienti ha mostrato conteggi di CTC molto più alti (mediana 12,5 cellule per mL) rispetto ai controlli (mediana 1,5 cellule per mL). In modo notevole, solo circa un terzo delle cellule PSMA-positive esprimeva EpCAM, suggerendo che i test basati esclusivamente su EpCAM perderebbero la maggior parte delle cellule tumorali in questi pazienti.
Cosa potrebbe significare per i pazienti
Trasformando un prelievo di sangue standard in una scansione ricca e automatizzata per cellule tumorali rare, questa piattaforma apre la strada a biopsie liquide più pratiche. La sua combinazione di olografia senza marcatori, fluorescenza mirata e deep learning raggiunge un basso tasso di falsi positivi pur catturando CTC che i sistemi tradizionali basati su marcatori trascurano. Oggi ciò si traduce in una migliore separazione tra pazienti oncologici e individui sani in uno studio pilota sul cancro alla prostata. Guardando al futuro, l’approccio potrebbe essere adattato a molti tipi di tumore e fluidi e potrebbe infine funzionare senza alcuna etichettatura fluorescente, affidandosi unicamente all’aspetto delle cellule nello spazio olografico. Se pienamente dimostrato in studi più ampi e diversificati, tali sistemi potrebbero permettere ai medici di monitorare l’andamento del cancro nel tempo con un semplice esame del sangue, modificare le terapie prima e ripristinare cellule tumorali vive per analisi molecolari dettagliate—il tutto senza scalpello.
Citazione: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Parole chiave: cellule tumorali circolanti, biopsia liquida, microscopia olografica digitale, diagnostica con deep learning, cancro alla prostata