Clear Sky Science · ar
كشف الخلايا الورمية الدائرة في مرضى السرطان باستخدام التصوير الهولوجرافي العميق أثناء التدفق
العثور على دلائل السرطان من عينة دم بسيطة
غالبًا ما ينتشر السرطان قبل أن يظهر ورم على الفحص، عبر انقفاء خلايا متناثرة في مجرى الدم. هذه «الخلايا الورمية الدائرة» نادرة لكنها دلائل قوية: إذ يمكن أن تشير إلى وجود السرطان، وتتابع استجابته للعلاج، وتلمّح إلى ما قد يحدث بعد ذلك. تصف هذه الورقة تقنية جديدة يمكنها غربلة مليارات خلايا الدم للعثور على هذه الخلايا الخطرة القليلة بسرعة وبنعومة وبدقة عالية — مما يفتح إمكانية إجراء اختبارات دم روتينية ترصد السرطان في الوقت الحقيقي.
لماذا تهم هذه الخلايا النادرة
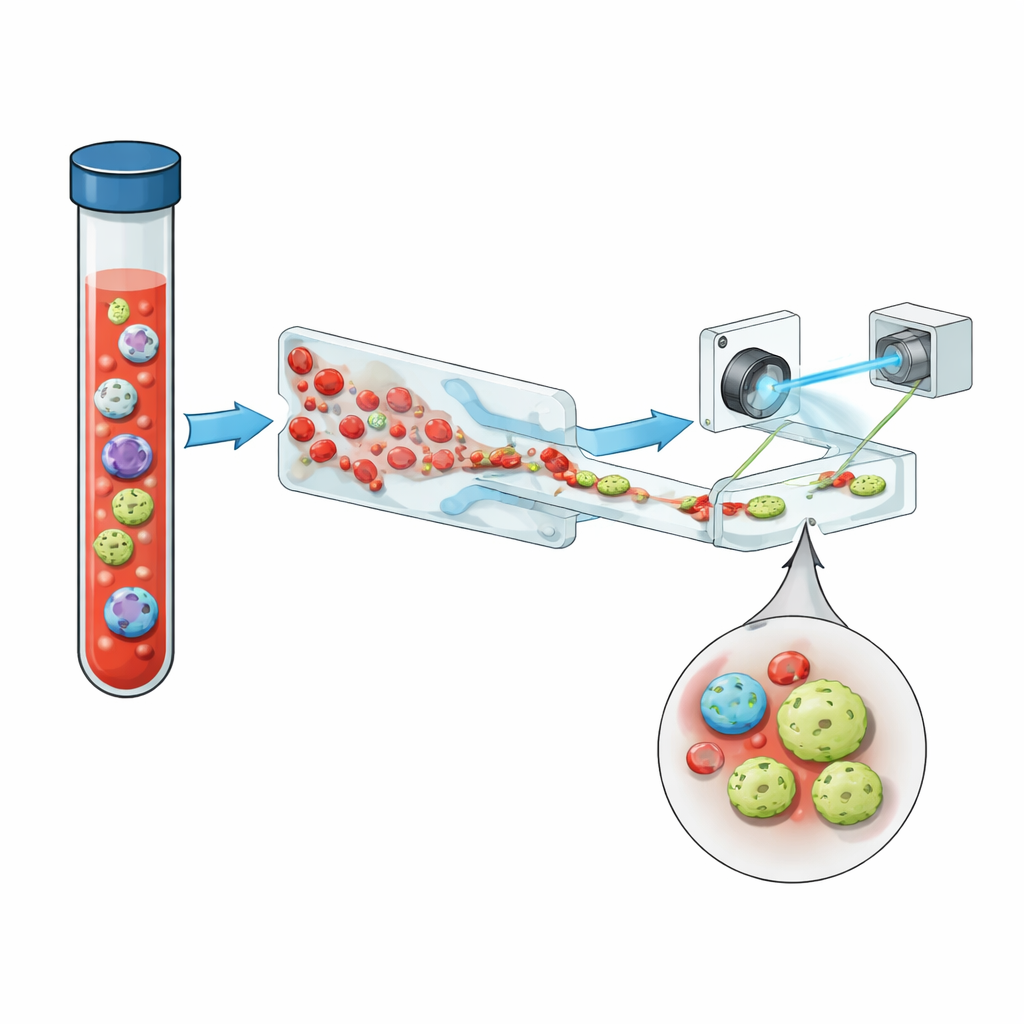
الخلايا الورمية الدائرة (CTCs) هي خلايا سرطانية انفصلت عن ورم أولي أو نقلي ودخلت مجرى الدم. حتى في المراحل المتقدمة من المرض، قد يحتوي الملليلتر الواحد من الدم على مليارات الخلايا الحمراء والبيضاء العادية لكن فقط عدد قليل من الخلايا الورمية — وأحيانًا أقل من واحد. ومع ذلك يرتبط عددها وسلوكها ارتباطًا وثيقًا بشدة الورم، وبمقاومته للعلاج، وبمدى بقاء المريض. الطرق التقليدية لاكتشافها غالبًا ما تعتمد على علامات سطحية مثل EpCAM، وهي بروتينات على سطح العديد من خلايا السرطان الظهارية. لكن مع تطور الأورام وتغير حالتها، قد تتلاشى هذه العلامات، مما يعني أن بعض أخطر الخلايا قد تهرب من الكشف.
نقائص الاختبارات الحالية
تحاول العديد من اختبارات الدم الحالية للـCTCs الإمساك بالخلايا عن طريق «أوسمة» جزيئية أو بصفات فيزيائية مثل الحجم والصلابة. الأنظمة المعتمدة على العلامات، مثل تلك التي تسحب مغناطيسيًا الخلايا الحاملة لـEpCAM، قد تفوّت خلايا ورمية أوقفت التعبير عن هذه العلامات أثناء عملية تغيير الشكل المرتبطة بالنقائل. قد تفشل الفلاتر المعتمدة على الحجم أو الكثافة أيضًا، لأن بعض الخلايا الورمية تشبه في الحجم والملمس خلايا الدم البيضاء الطبيعية. الأجهزة التي تجمع عدة تقنيات — شرائح ميكروفلويدية معقدة، مغنطات، أو قوى صوتية — تكسب حساسية أكبر لكنها غالبًا ما تأتي على حساب التعقيد والتكلفة وفقدان الخلايا. ونتيجة لذلك، تكافح كثير من المنصات لتكون بسيطة بما يكفي للاستخدام السريري الروتيني وحساسة بما يكفي لالتقاط التنوع الكامل للخلايا الورمية.
طريقة جديدة لرؤية الخلايا أثناء التدفق
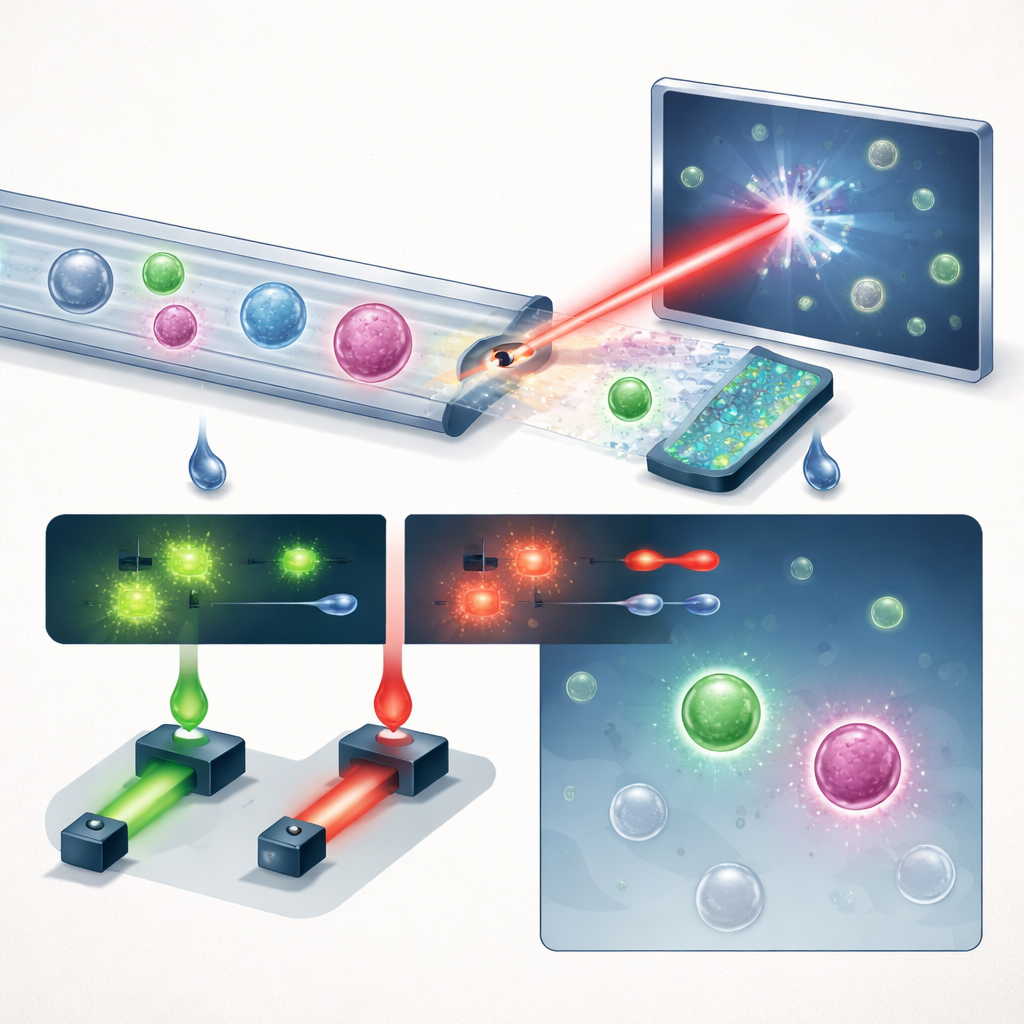
يقدّم الفريق نظامًا مدمجًا يربط بين ثلاث أفكار رئيسية: معالجة سائلة ذكية، تصوير هولوجرافي، وتعلّم عميق، مع جرعة مساعدة من التألق المفلوري. أولًا، يمرّ الدم الكامل عبر شريحة ميكروفلويدية «مسننة» تزيل أكثر من 99.999% من خلايا الدم الحمراء ومعظم خلايا الدم البيضاء، مع الحفاظ على الغالبية العظمى من الخلايا الورمية. هذا يحول عينة مكتظة إلى عينة تقل فيها المنافسة، فتبرز الخلايا النادرة. يتدفق المزيج المنقّى بعد ذلك عبر قناة مستقيمة بسيطة تحت ليزر بنفسجي نابض. بدلًا من التقاط صور مسطحة، يسجل النظام هولوجرامات — أنماط تداخل تشفّر كلًا من السطوع والسماكة البصرية لكل خلية، وتلتقط البنية الثلاثية الأبعاد الدقيقة في لقطة واحدة.
تعليم شبكة عصبية لتمييز العناصر الشاذة
نظرًا لندرة الـCTCs الحقيقية، فإن جمع أمثلة مرضية كافية لتدريب خوارزمية أمر غير عملي. بدلاً من ذلك علّم الباحثون نموذجًا للتعلّم العميق على التعرف على أي شيء لا يشبه الدم العادي. زوّدوه بملايين الهولوجرامات من متبرعين أصحاء، التي تُظهر التنوع الكامل لخلايا الدم البيضاء والحمراء والحطام، وموازنوها بصور من العديد من خطوط الخلايا السرطانية المزروعة في المختبر. يحول شبكة عصبية متخصصة كل هولوجرام إلى خريطة حرارية لمواقع محتملة للأورام، معاملة الخلايا كنقاط مضيئة بدلًا من صناديق. ولتوسيع التدريب دون وسم يدوي لا نهائي، يؤشر نموذج مساعد أولًا كل الخلايا في صور الخلايا السرطانية النقية؛ ثم يستخدم النموذج الرئيسي تلك «الوسوم الزائفة»، بالإضافة إلى دالة خسارة مضبوطة لتعكس ندرة الـCTCs الحقيقية، ليتعلّم أن يكون صارمًا تجاه الإيجابيات الكاذبة مع الحفاظ على القدرة على كشف الخلايا الشاذة.
اختبار النظام
في تجارب محكمة حيث أُضيف أعداد معروفة من خلايا سرطان البروستاتا إلى دم صحي، استعاد النظام نحو 60% من هذه الخلايا عند نقطة تشغيل مختارة، مع الحفاظ على إيجابيات كاذبة أقل من واحدة لكل ملليلتر — حتى عند عتبات كشف متساهلة. ولتعزيز قراراته، يقيس النظام أيضًا إشارتين فلوريّتين من أجسام مضادة ضد PSMA، وهو مؤشر خاص بالبروستاتا، وEpCAM. أثناء اختبارات المرضى، كان يجب أن يجتاز الخلية حتى تُحتسب كـCTC عتبة التعلّم العميق الهولوجرافي وأن تظهر إشارة PSMA قوية، جامعًا بين معلومات الشكل الخالية من الأوسمة وتأكيد جزيئي مستهدف. عندما طبّق الباحثون هذا على 13 رجلاً مصابًا بسرطان البروستاتا المتقدم و8 متبرعين ذكور أصحاء، أظهرت مجموعة السرطان معدلات أعلى بكثير من خلايا CTC (الوسيط 12.5 خلية لكل مل) مقارنةً بالضوابط (الوسيط 1.5 خلية لكل مل). اللافت أن حوالي ثلث الخلايا الموجبة لـPSMA فقط حملت EpCAM، مما يشير إلى أن الاختبارات المعتمدة حصريًا على EpCAM ستفوّت أغلبية الخلايا الورمية في هؤلاء المرضى.
ماذا قد يعني هذا للمرضى
من خلال تحويل سحب دم قياسي إلى فحص آلي غني للخلايا الورمية النادرة، يشير هذا النظام إلى إمكانية «خزعات سائلة» أكثر عملية. مزيجه من الهولوجرافيا الخالية من الأوسمة، والتألق المستهدف، والتعلّم العميق يحقق معدل إيجابيات كاذبة منخفضًا مع التقاط خلايا CTC التي تتجاهلها أنظمة الاعتماد على العلامات التقليدية. اليوم، يعني ذلك فصلًا أفضل بين مرضى السرطان والأفراد الأصحّاء في دراسة تجريبية لسرطان البروستاتا. مستقبلًا، قد تُكيّف هذه المقاربة لأنواع أورام وسوائل متعددة، وقد تعمل في نهاية المطاف دون أي أوسمة فلورية، معتمدة فقط على مظهر الخلايا في الفضاء الهولوجرافي. إذا ثبتت فعاليتها في تجارب أكبر ومتنوعة، قد تسمح مثل هذه الأنظمة للأطباء بتتبع صعود وهبوط السرطان عبر الزمن بواسطة اختبار دم بسيط، تعديل العلاجات بسرعة أكبر، واستعادة خلايا ورمية حية للتحليل الجزيئي المفصّل — كل ذلك دون مشرط.
الاستشهاد: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
الكلمات المفتاحية: الخلايا الورمية الدائرة, الخزعة السائلة, الميكروسكوب الهولوجرافي الرقمي, التشخيص بالتعلّم العميق, سرطان البروستاتا