Clear Sky Science · he
גילוי תאי גידול ממאירים בהישרדות במחזור הדם במטופלי סרטן באמצעות הולוגרפיה זרימתית בלמידת עומק
למצוא רמזים לסרטן במבחן דם פשוט
הסרטן לעיתים מופץ הרבה לפני שמאותר גוש בסריקה, על ידי שחרור תאים בודדים לזרם הדם. תאים נודדים אלה, שנקראים "תאי גידול במחזור הדם" (CTCs), נדירים אך מספקים רמזים רבי‑עוצמה: הם יכולים לאותת על נוכחות הסרטן, לעקוב אחר תגובת הגידול לטיפול ולהצביע על מה שעשוי לקרות בהמשך. מאמר זה מתאר טכנולוגיה חדשה שיכולה לסרוק מיליארדי תאי דם כדי למצוא את האוספים המסוכנים הללו במהירות, בעדינות ובדיוק גבוה — ומעלה את האפשרות לבדיקות דם שגרתיות שיעקבו אחר הסרטן בזמן אמת.
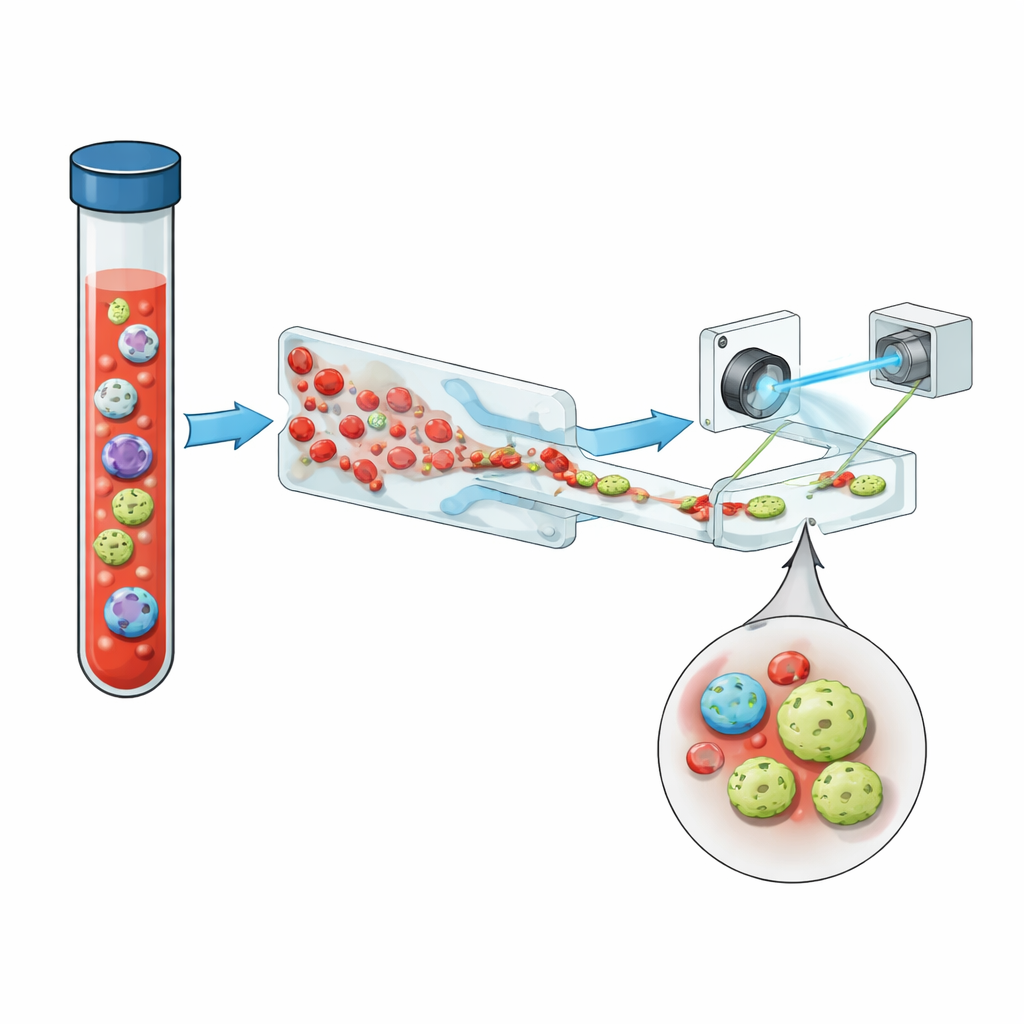
מדוע תאים נדירים אלה חשובים
תאי גידול במחזור הדם (CTCs) הם תאי סרטן שניתקו ממקור ראשוני או ממטסטזות והחדרו לזרם הדם. גם במחלה מתקדמת, מיליליטר דם יכול להכיל מיליארדי תאי דם אדומים ולבנים רגילים אך רק קומץ CTCs — לעיתים פחות מאחד. עם זאת, כמותם והתנהגותם קשורים בקשר הדוק לאגרסיביות הגידול, לעמידותו לטיפול ולמשך החיים הצפוי של המטופל. שיטות מקובלות לזיהוין מסתמכות לעתים על סמני פני שטח כמו EpCAM, חלבונים על פני תאים אפיתליאלים רבים. אך כשהגידול משתנה ומתפתח, סמנים אלה עלולים לדעוך, כך שחלק מהתאים המסוכנים ביותר עשויים להימלט מזיהוי.
החסרונות של בדיקות קיימות
רבות מהבדיקות הקיימות ל‑CTCs מנסות לתפוס תאים לפי "תגי־שם" מולקולריים או לפי תכונות פיזיות כמו גודל וקשיחות. מערכות מבוססות סמנים, כגון אלה שמושכות מגנטית תאים הנושאים EpCAM, עלולות לפספס תאי גידול שכיבו סמנים אלה במהלך תהליך שינוי צורה הקשור למטסטזות. מסננים על בסיס גודל או צפיפות גם יכולים להיכשל, כי חלק מתאי הגידול דומים בגודלם ובתחושתם לתאי דם לבנים רגילים. מכשירים שמצברים מספר שיטות — שבבים מיקרו‑נוזליים מורכבים, מגנטים או כוחות אקוסטיים — מרוויחים ברגישות אך לעתים במחיר של מורכבות גבוהה יותר, עלות גדולה יותר ואובדן תאים. כתוצאה מכך, רבות מהפלטפורמות מתקשות להיות גם פשוטות מספיק לשימוש קליני שגרתי וגם רגישות מספיק כדי ללכוד את מגוון תאי הגידול במלואו.
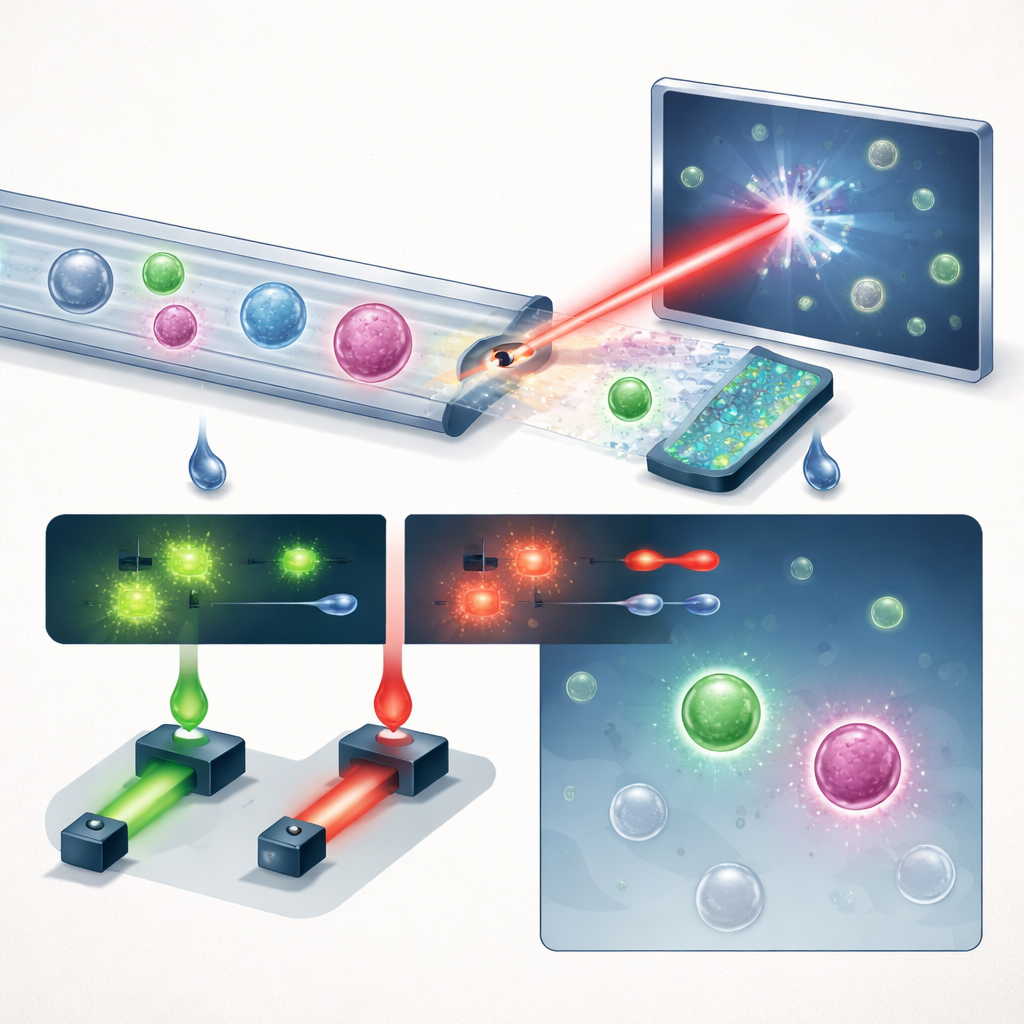
דרך חדשה לראות תאים בזרימה
הצוות מציג מערכת קומפקטית שמחברת שלוש רעיונות מרכזיים: טיפול נוזלים חכם, דימות הולוגרפי ולמידת עומק, עם תוספת מועילה של פלואורוסנצence. תחילה, דם שלם עובר דרך שבב מיקרו‑נוזליים בצורת "מסור" שמסיר יותר מ‑99.999% מתאי הדם האדומים וכמעט את כל תאי הדם הלבנים, תוך שמירה על רוב תאי הגידול. כך מדגם צפוף הופך לאזור שבו תאים נדירים בולטים יותר. הזרם המועשר עובר אחר כך בערוץ ישר ופשוט תחת לייזר ורוד מהבהב. במקום לצלם תמונות שטוחות, המערכת מקליטה הולגרמות — דפוסים התערבותיים שמקודדים גם את הבהירות וגם את העמידות האופטית של כל תא, ותופסים מבנה תלת‑ממדי עדין בלכידה אחת.
להדריך רשת נוירונים לזהות את הזרות
מכיוון שתאי CTC אמיתיים נדירים, איסוף מספיק דוגמאות מטופלים לאימון אלגוריתם אינו מעשי. החוקרים לימדו במקום זאת מודל למידת עומק לזהות כל דבר שאינו נראה כמו דם רגיל. הם הזינו לו מיליוני הולגרמות מתורמים בריאים, המציגות את המגוון המלא של תאי דם אדומים ולבנים ופסולת, ואיזנו אותן עם תמונות ממספר רב של שורות תאים סרטניות שגודלו במעבדה. רשת נוירונית מתמחה ממירה כל הולגרמה למפת חום של מיקומי גידול אפשריים, וטורחת להציג תאים כנקודות מאירות במקום כמלבנים. כדי להרחיב את האימון ללא תיוג ידני אינסופי, מודל עזר מסמן תחילה את כל התאים בתמונות של תאים סרטניים טהורים; המודל הראשי משתמש אז ב"תיוגי־שקר" אלה, ובפונקציית אובדן המותאמת לשכיחות הנמוכה של CTCs אמיתיים, ללמוד להיות קפדני ביחס לאזעקות שווא ובאותו זמן לתפוס תאים יוצאי דופן.
בחינה של המערכת במבחן
בניסויים מבוקרים שבהם הוסיפו מספרים ידועים של תאי סרטן הערמונית לדם בריא, הפלטפורמה השיבה כ‑60% מהתאים בנקודת הפעלה נבחרת, תוך שמירה על שגיאות חיוביות נמוכות מפחות מאחת למיליליטר — גם בספי זיהוי ליברליים. כדי לדייק עוד יותר את ההחלטות, המערכת גם מודדת שני אותות פלואורוסנציה מחיסונים כנגד PSMA, סמן ספציפי לערמונית, ו‑EpCAM. במבחנים על מטופלים, תא נספר כ‑CTC רק אם עמד גם בסף הלמידה העמוקה של ההולוגרפיה וגם הראה אות PSMA חזק, ובכך שילב מידע צורה חופשי‑תיוג עם אישור מולקולרי ממוקד. כאשר החלו להשתמש בזה על 13 גברים עם סרטן ערמונית מתקדם ו‑8 תורמים גברים בריאים, קבוצת החולים הראתה ספירות CTC גבוהות בהרבה (חציון 12.5 תאים למיליליטר) מהקבוצת ביקורת (חציון 1.5 תאים למיליליטר). באופן בולט, רק כשליש מהתאים החיוביים ל‑PSMA נשאו EpCAM, מה שמרמז שמבחנים המבוססים רק על EpCAM היו מפספסים את מרבית תאי הגידול במטופלים אלה.
מה זה עשוי להעניק למטופלים
על‑ידי הפיכת נתיחת דם שגרתית לסריקה עשירה ומאוטומטת אחר תאי סרטן נדירים, הפלטפורמה מצביעה לכיוון של "ביופסיות נוזליות" יישומיות יותר. תערובת ההולוגרפיה החופשית תיוג, הפלואורוסנציה הממוקדת ולמידת העומק מגיעה לשיעור שגיאות חיוביות נמוך תוך לכידת CTCs שמערכות מסורתיות המבוססות סמנים משאירות מאחור. כיום, זה אומר הבחנה טובה יותר בין חולי סרטן לפרטים בריאים במחקר פיילוט על סרטן הערמונית. בעתיד, הגישה עשויה להיות מותאמת לסוגי גידולים ונוזלים רבים, ואולי תעבוד בסופו של דבר ללא כל תיוג פלואורוסנטי, בהסתמך לחלוטין על המראה ההולוגרפי של התאים. אם תוצלח באופן מלא בניסויים רחבים ומגוונים, מערכות כאלה יכולות לאפשר לרופאים לעקוב אחרי עלייתו ושקיעתו של הסרטן לאורך זמן בבדיקת דם פשוטה, להתאים טיפולים במהירות רבה יותר ולהשיב תאים גידוליים חיים לניתוח מולקולרי מפורט — וכל זאת ללא סכין מנתחת.
ציטוט: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
מילות מפתח: תאי גידול במחזור הדם, ביופסיה נוזלית, מיקרוסקופיה הולוגרפית דיגיטלית, אבחון בלמידת עומק, סרטן הערמונית