Clear Sky Science · nl
Detectie van circulerende tumorcellen bij kankerpatiënten met behulp van in-flow deep learning-holografie
Kankeropsporing met een eenvoudige bloedafname
Kanker verspreidt zich vaak lang voordat een tumor op een scan zichtbaar wordt, door losse cellen af te stoten in de bloedbaan. Deze rondzwervende “circulerende tumorcellen” zijn zeldzaam maar belangrijke aanwijzingen: ze kunnen de aanwezigheid van kanker signaleren, laten zien hoe de ziekte reageert op behandeling en een indicatie geven van wat er kan gebeuren. Dit artikel beschrijft een nieuwe technologie die miljarden bloedcellen kan doorzoeken om deze paar gevaarlijke afwijkingen snel, zacht en met hoge nauwkeurigheid te vinden—wat de mogelijkheid opent van routinematige bloedtesten die kanker in real time volgen.
Waarom deze zeldzame cellen ertoe doen
Circulerende tumorcellen (CTC’s) zijn kankercellen die losgeraakt zijn van een primaire of metastatische tumor en in de bloedbaan terechtkomen. Zelfs bij gevorderde ziekte kan een milliliter bloed miljarden normale rode en witte bloedcellen bevatten maar slechts een handvol CTC’s—soms minder dan één. Toch hangen hun aantal en gedrag nauw samen met hoe agressief een tumor is, of hij therapieresistentie ontwikkelt en hoe lang een patiënt waarschijnlijk leeft. Standaardmethoden om ze te vinden vertrouwen vaak op oppervlakte-eiwitten zoals EpCAM, die op veel epitheliale kankercellen voorkomen. Maar naarmate tumoren evolueren en van toestand veranderen, kunnen deze markers verdwijnen, waardoor sommige van de gevaarlijkste cellen onopgemerkt blijven.
Gebreken van huidige tests
Veel bestaande bloedtesten voor CTC’s proberen cellen te vangen aan de hand van moleculaire “naamplaatjes” of op basis van fysieke eigenschappen zoals grootte en stijfheid. Marker-gebaseerde systemen, zoals die cellen met EpCAM magnetisch verwijderen, kunnen tumorcellen missen die deze markers hebben uitgeschakeld tijdens een vormveranderingsproces dat samenhangt met metastase. Filters op grootte of dichtheid kunnen ook falen, omdat sommige tumorcellen vergelijkbaar zijn in grootte en gevoel met normale witte bloedcellen. Apparaten die meerdere trucs combineren—complexe microfluidische chips, magneten of akoestische krachten—vergroten de gevoeligheid maar vaak ten koste van hogere complexiteit, kosten en celverlies. Daardoor worstelen veel platforms om zowel eenvoudig genoeg te zijn voor routinematig klinisch gebruik als gevoelig genoeg om de volledige diversiteit van tumorcellen te vangen.
Een nieuwe manier om cellen in stroming te zien
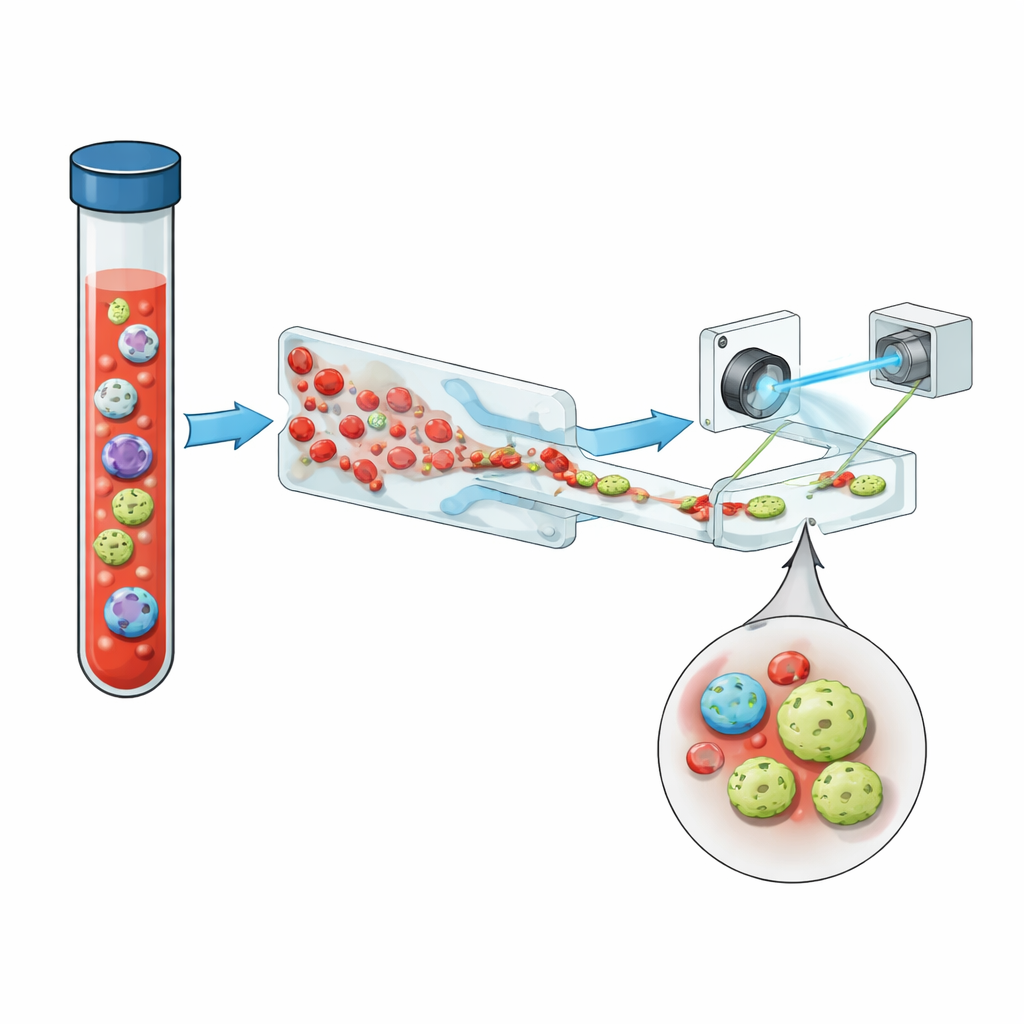
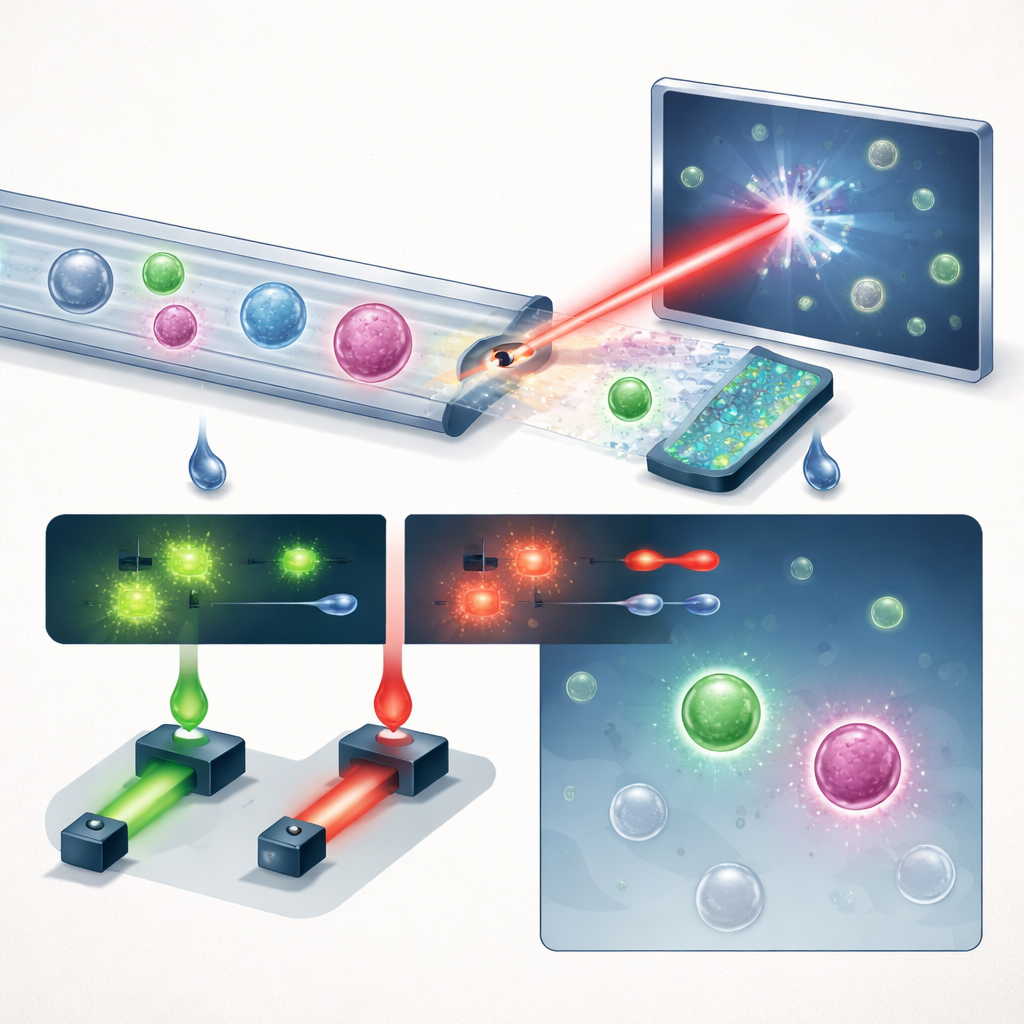
Het team introduceert een compact systeem dat drie kernideeën achter elkaar schakelt: slimme vloeistofverwerking, holografische beeldvorming en deep learning, met een nuttige toevoeging van fluorescentie. Eerst wordt volledig bloed door een “zaagtand”-microfluidisch chip geleid die meer dan 99,999% van de rode bloedcellen en vrijwel alle witte bloedcellen verwijdert, terwijl de overgrote meerderheid van de tumorcellen behouden blijft. Dit verandert een drukke monster in een waarin zeldzame cellen meer kans hebben op opvallen. De verrijkte stroom stroomt vervolgens door een eenvoudige rechte kanaal onder een gepulste violette laser. In plaats van platte foto’s te maken, registreert het systeem hologrammen—interferentiepatronen die zowel de helderheid als de optische dikte van elke cel coderen, waardoor subtiele driedimensionale structuren in één enkele opname worden vastgelegd.
Een neuraal netwerk leren de afwijkende cellen te herkennen
Aangezien echte CTC’s schaars zijn, is het praktisch onmogelijk om rechtstreeks genoeg echte patiëntvoorbeelden te verzamelen om een algoritme te trainen. De onderzoekers leerden het deep learning-model daarom te herkennen wat niet lijkt op gewoon bloed. Ze voedden het met miljoenen hologrammen van gezonde donoren, die de volledige variëteit aan witte en rode bloedcellen en debris tonen, en balanceerden die met beelden van vele verschillende kankercellijnen gekweekt in het laboratorium. Een gespecialiseerd neuraal netwerk zet elk hologram om in een heatmap van waarschijnlijke tumorlocaties, waarbij cellen worden behandeld als oplichtende kernpunten in plaats van als rechthoeken. Om de training op te schalen zonder eindeloze handmatige labeling, markeert een hulpsysteem eerst alle cellen in zuivere kankercelbeelden; het hoofdmodel gebruikt die “pseudo-labels”, plus een verliesfunctie afgestemd op hoe zeldzaam echte CTC’s zijn, om streng te leren omgaan met false alarms terwijl het toch ongebruikelijke cellen opvangt.
Het systeem op de proef stellen
In gecontroleerde experimenten waarbij bekende aantallen prostaatkankercellen aan gezond bloed werden toegevoegd, herstelde het platform ongeveer 60% van deze cellen bij een gekozen bedrijfsinstelling, terwijl het aantal false positives onder één per milliliter bleef—even bij vrijgegeven detectiedrempels. Om de beslissingen verder te verscherpen, meet het systeem ook twee fluorescentiesignalen van antilichamen tegen PSMA, een prostaat-specifieke marker, en EpCAM. Tijdens patiënttesten moest een cel als CTC worden geteld zowel de holografische deep learning-drempel passeren als een sterk PSMA-signaal tonen, waarmee labelvrije vorminformatie wordt gecombineerd met gerichte moleculaire bevestiging. Toen de onderzoekers dit toepasten op 13 mannen met gevorderde prostaatkanker en 8 gezonde mannelijke donoren, toonde de kankergroep veel hogere CTC-aantallen (mediaan 12,5 cellen per mL) dan de controles (mediaan 1,5 cellen per mL). Opvallend was dat slechts ongeveer een derde van de PSMA-positieve cellen EpCAM droeg, wat suggereert dat tests die uitsluitend op EpCAM vertrouwen de meerderheid van de tumorcellen bij deze patiënten zouden missen.
Wat dit voor patiënten kan betekenen
Door een standaard bloedafname te veranderen in een rijke, geautomatiseerde scan voor zeldzame kankercellen, wijst dit platform op meer praktische “vloeibare biopsieën.” De combinatie van labelvrije holografie, gerichte fluorescentie en deep learning bereikt een laag false-positive-tarief terwijl het CTC’s vangt die traditionele marker-gebaseerde systemen over het hoofd zien. Vandaag betekent dat een betere scheiding van kankerpatiënten en gezonde individuen in een pilootstudie voor prostaatkanker. Vooruitkijkend kan de aanpak worden aangepast aan veel tumorsoorten en vloeistoffen, en uiteindelijk mogelijk werken zonder enige fluorescentielabels, uitsluitend afhankelijk van hoe cellen eruitzien in holografische ruimte. Als dit volledig wordt bewezen in grotere, diverse trials, zouden dergelijke systemen artsen kunnen toestaan om de opkomst en afname van kanker in de loop van de tijd met een eenvoudige bloedtest te volgen, behandelingen eerder aan te passen en levende tumorcellen te winnen voor gedetailleerde moleculaire analyse—al dat zonder scalpel.
Bronvermelding: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Trefwoorden: circulerende tumorcellen, vloeibare biopsie, digitale holografische microscopie, deep learning diagnostiek, prostaatkanker