Clear Sky Science · ja
フロー内ディープラーニングホログラフィを用いたがん患者の循環腫瘍細胞検出
採血で得られるがんの手がかりを見つける
がんはしばしばスキャンで腫瘍が見つかるずっと前に広がり、血流中に迷い出た細胞を放出します。これらの遊走する「循環腫瘍細胞(CTC)」は稀ですが重要な手がかりであり、がんの存在を示したり、治療への反応を追跡したり、今後の経過を予測したりします。本論文は、数十億の血球の中からこの数個の危険な細胞を迅速かつ穏やかに、かつ高精度で見つけ出せる新しい技術を述べており、リアルタイムでがんを追跡する日常的な血液検査の可能性を高めます。
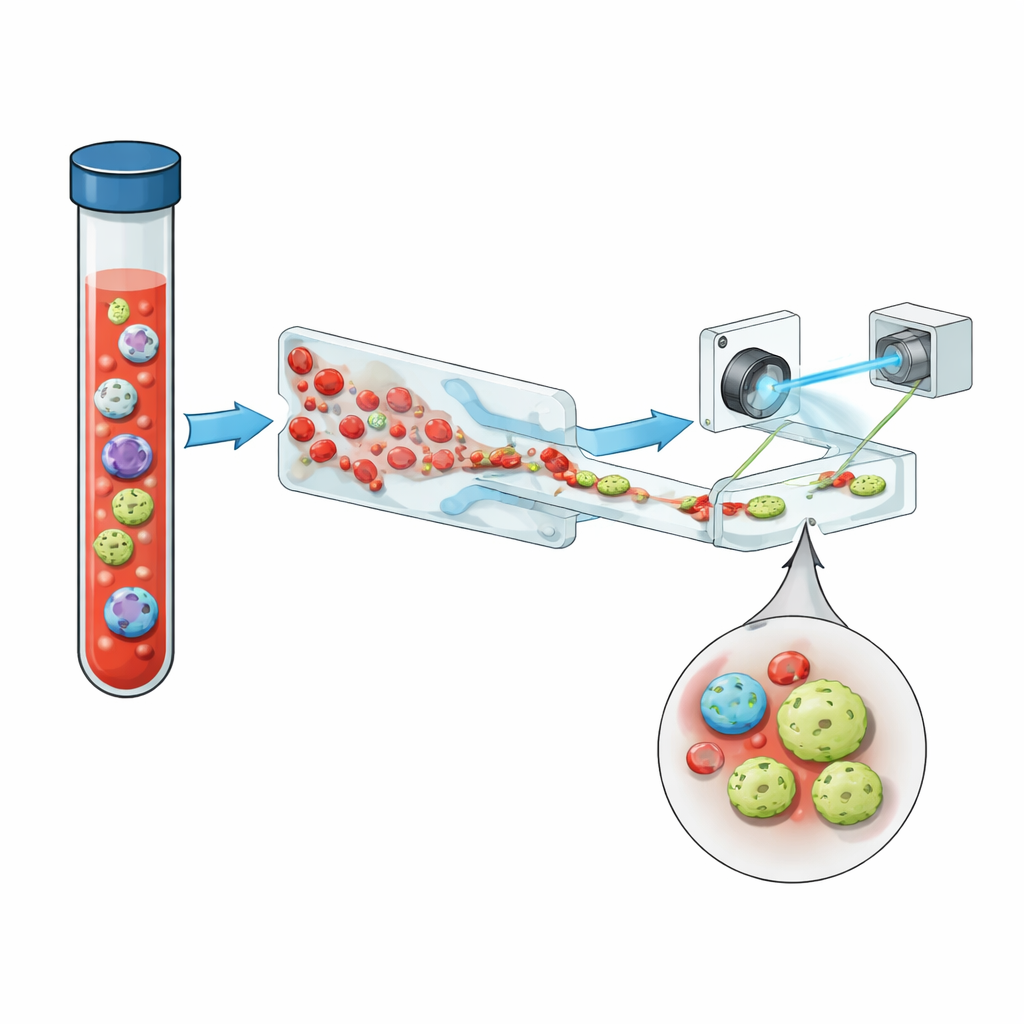
なぜこれらの稀な細胞が重要なのか
循環腫瘍細胞(CTC)は、原発または転移性腫瘍から離れて血流に入ったがん細胞です。進行した病態でも、1ミリリットルの血液中には何億個もの正常な赤血球や白血球が存在する一方で、CTCは数個しか含まれないことがあり、場合によっては1個未満です。それでもCTCの数や挙動は、腫瘍の悪性度、治療への耐性、患者の生存期間と密接に関連します。標準的な検出法は多くの場合EpCAMのような表面マーカーに依存していますが、腫瘍が進化して状態を変えるとこれらのマーカーが薄れ、最も危険な細胞の一部が見逃されることがあります。
現行検査の欠点
既存の多くのCTC血液検査は、分子の“名札”やサイズや剛性といった物理的特性によって細胞を捕まえようとします。EpCAMを持つ細胞を磁気的に取り出すようなマーカーベースのシステムは、転移に関連する形態変化の過程でこれらのマーカーを消失した腫瘍細胞を見逃す可能性があります。サイズや密度に基づくフィルターも、一部の腫瘍細胞が正常な白血球と大きさや感触が似ているため、失敗することがあります。複数の手法を組み合わせた装置—複雑なマイクロ流体チップ、磁石、音響力など—は感度を高めますが、しばしば複雑さ、コスト、細胞ロスの増加を招きます。その結果、多くのプラットフォームは日常臨床で使えるほどシンプルであることと、腫瘍細胞の多様性を完全に捕捉するほど感度が高いことを両立できていません。
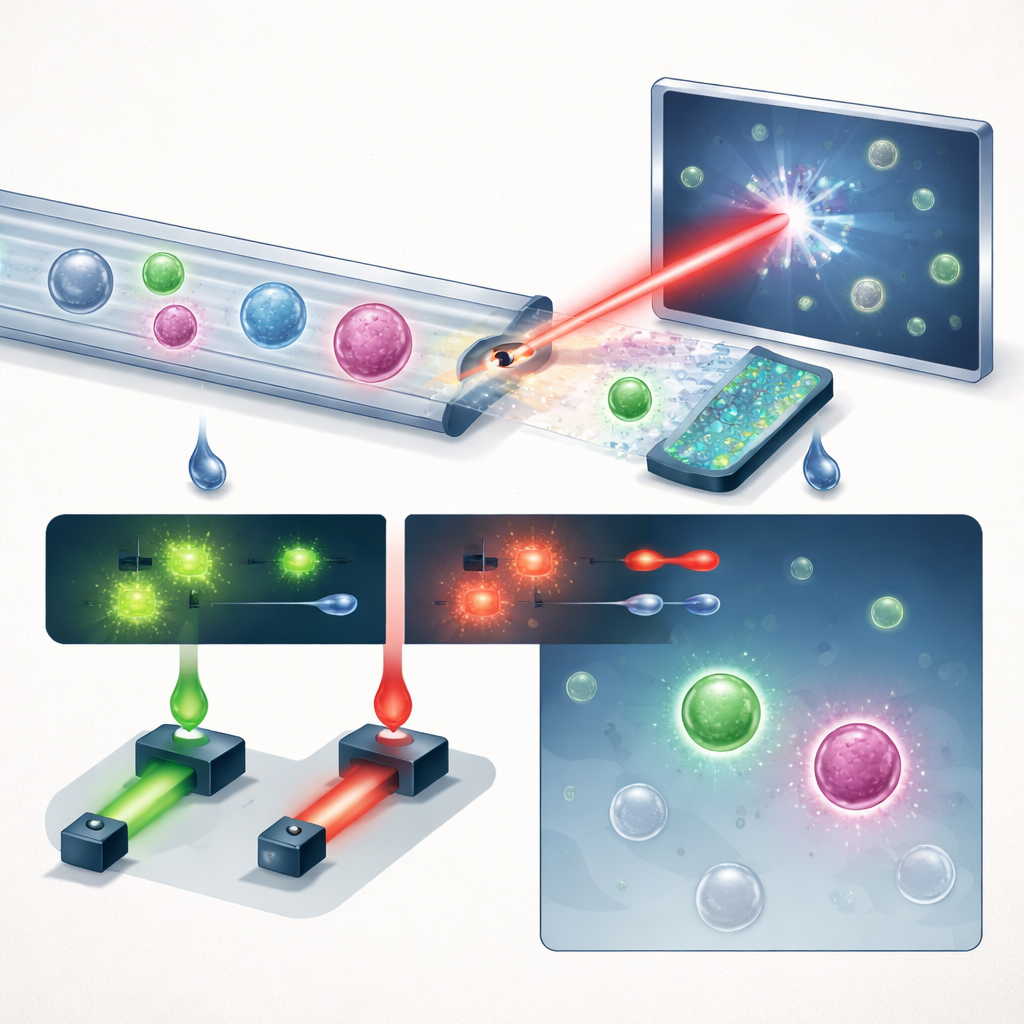
フロー中の細胞を新しい方法で見る
研究チームは、スマートな流体処理、ホログラフィ画像化、ディープラーニングという三つの主要なアイデアを結びつけ、蛍光検出を組み合わせたコンパクトなシステムを紹介します。まず、全血を“のこぎり歯”型のマイクロ流体チップに通し、赤血球の99.999%以上とほぼすべての白血球を除去しつつ、腫瘍細胞の大部分を保持します。これにより混雑したサンプルが希少細胞を見つけやすい状態に変わります。濃縮された流れはパルス状の紫色レーザー下の単純な直線チャネルを流れます。平面的な写真を撮る代わりに、システムはホログラム—各細胞の明るさと光学的厚さを符号化する干渉パターン—を記録し、単一のスナップショットで微細な三次元構造を捉えます。
異質な細胞を見分けるニューラルネットワークの教育
真のCTCは稀であるため、アルゴリズムを訓練するのに十分な実患者由来のサンプルを直接収集するのは現実的ではありません。研究者らは代わりに、通常の血液に見えないものを認識するようディープラーニングモデルを訓練しました。彼らは健康な献血者から得た何百万ものホログラムを与え、白血球や赤血球、デブリの全バラエティを示し、これを多数の培養されたがん細胞株の画像とバランスさせました。特殊化したニューラルネットワークは各ホログラムを、ボックスではなく光るキーポイントとして細胞を扱う、腫瘍のありそうな位置のヒートマップに変換します。果てしない手動ラベリングを避けるために、補助モデルがまず純粋ながん細胞画像中のすべての細胞をマークし、主モデルはそれらの“疑似ラベル”と、実際のCTCが稀であることを反映した損失関数を用いて、誤報を厳しく抑えつつ異常な細胞を見逃さないよう学習します。
システムの試験
既知数の前立腺がん細胞を健康な血液にスパイクインした制御実験では、プラットフォームは選択した動作点で約60%の回収率を示し、検出閾値を緩めても偽陽性はミリリットル当たり1未満に保たれました。判定精度をさらに高めるために、システムはPSMA(前立腺特異的マーカー)とEpCAMに対する抗体からの二つの蛍光シグナルも測定します。患者試験では、ある細胞をCTCとカウントするにはホログラフィディープラーニングの閾値をクリアするとともに強いPSMAシグナルを示す必要があり、ラベルフリーの形状情報と標的分子の確認を組み合わせています。研究者らがこれを進行した前立腺がんの13人の男性と8人の健常男性ドナーに適用したところ、がん群は対照群よりもはるかに高いCTC数(中央値12.5個/mL)を示し、対照は中央値1.5個/mLでした。注目すべきは、PSMA陽性の細胞のうちEpCAMを持つものは約3分の1に過ぎず、EpCAMのみに依存する検査ではこれら患者の腫瘍細胞の大部分を見逃してしまう可能性が示唆された点です。
患者にとっての意義
標準的な採血を希少ながん細胞を探す豊富で自動化されたスキャンに変えることで、このプラットフォームはより実用的な“リキッドバイオプシー”への道を示します。ラベルフリーのホログラフィ、標的蛍光、ディープラーニングの組み合わせにより、偽陽性率を低く保ちながら従来のマーカーベースのシステムが見逃すCTCを捕らえます。現在は、パイロットの前立腺がん研究においてがん患者と健常者をより良く分けることを意味します。将来に目を向ければ、このアプローチは多くの腫瘍タイプや体液に適応でき、最終的には蛍光ラベルをまったく使わずホログラフィ上の見た目だけで動作する可能性もあります。より大規模で多様な試験で十分に検証されれば、この種のシステムは単純な採血でがんの増減を時間経過として追跡し、治療を早期に調整し、外科的切除なしで生きた腫瘍細胞を回収して詳細な分子解析を行えるようになるかもしれません。
引用: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
キーワード: 循環腫瘍細胞, リキッドバイオプシー, デジタルホログラフィ顕微鏡, ディープラーニング診断, 前立腺がん