Clear Sky Science · pt
Detecção de células tumorais circulantes em pacientes com câncer usando holografia por fluxo e aprendizado profundo
Encontrando pistas do câncer em uma simples coleta de sangue
O câncer frequentemente se espalha muito antes de um tumor aparecer em um exame por imagem, liberando células perdidas na corrente sanguínea. Essas “células tumorais circulantes” são raras, mas trazem pistas poderosas: podem indicar a presença do câncer, monitorar sua resposta ao tratamento e antecipar possíveis desfechos. Este artigo descreve uma nova tecnologia capaz de vasculhar bilhões de células sanguíneas para encontrar essas poucas células perigosas de forma rápida, suave e com alta precisão — abrindo a perspectiva de exames de sangue rotineiros que acompanhem o câncer em tempo real.
Por que essas células raras importam
Células tumorais circulantes (CTCs) são células cancerígenas que se desprenderam de um tumor primário ou metastático e entraram na corrente sanguínea. Mesmo em doença avançada, um mililitro de sangue pode conter bilhões de glóbulos vermelhos e brancos normais, mas apenas algumas CTCs — às vezes menos de uma. Ainda assim, seu número e comportamento estão intimamente ligados à agressividade do tumor, à resistência ao tratamento e à sobrevida provável do paciente. Métodos padrão para encontrá‑las frequentemente dependem de marcadores de superfície como EpCAM, proteínas na membrana externa de muitas células epiteliais tumorais. Mas à medida que os tumores evoluem e mudam de estado, esses marcadores podem desaparecer, o que faz com que algumas das células mais perigosas escapem da detecção.
Limitações dos testes atuais
Muitos testes sanguíneos existentes para CTCs tentam capturar células por “etiquetas” moleculares ou por características físicas como tamanho e rigidez. Sistemas baseados em marcadores, como os que retiram magneticamente células que expressam EpCAM, podem deixar passar células tumorais que desligaram esses marcadores durante um processo de mudança de forma associado à metastase. Filtros por tamanho ou densidade também podem falhar, porque algumas células tumorais têm tamanho e propriedades físicas semelhantes aos glóbulos brancos normais. Dispositivos que combinam várias estratégias — chips microfluídicos complexos, ímãs ou forças acústicas — ganham sensibilidade, mas frequentemente ao custo de maior complexidade, custo e perda celular. Como resultado, muitas plataformas têm dificuldade em ser ao mesmo tempo simples o suficiente para uso clínico rotineiro e sensíveis o bastante para capturar a diversidade completa das células tumorais.
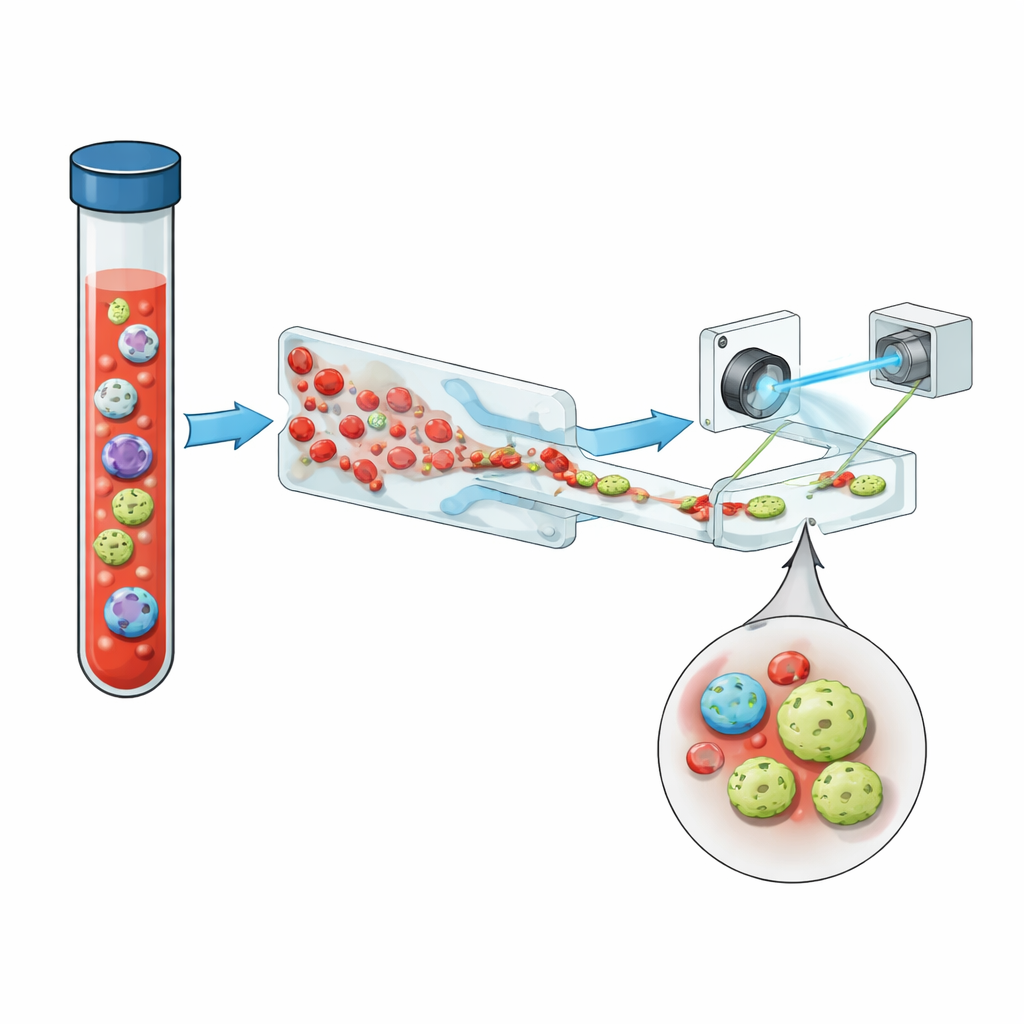
Uma nova forma de ver células em fluxo
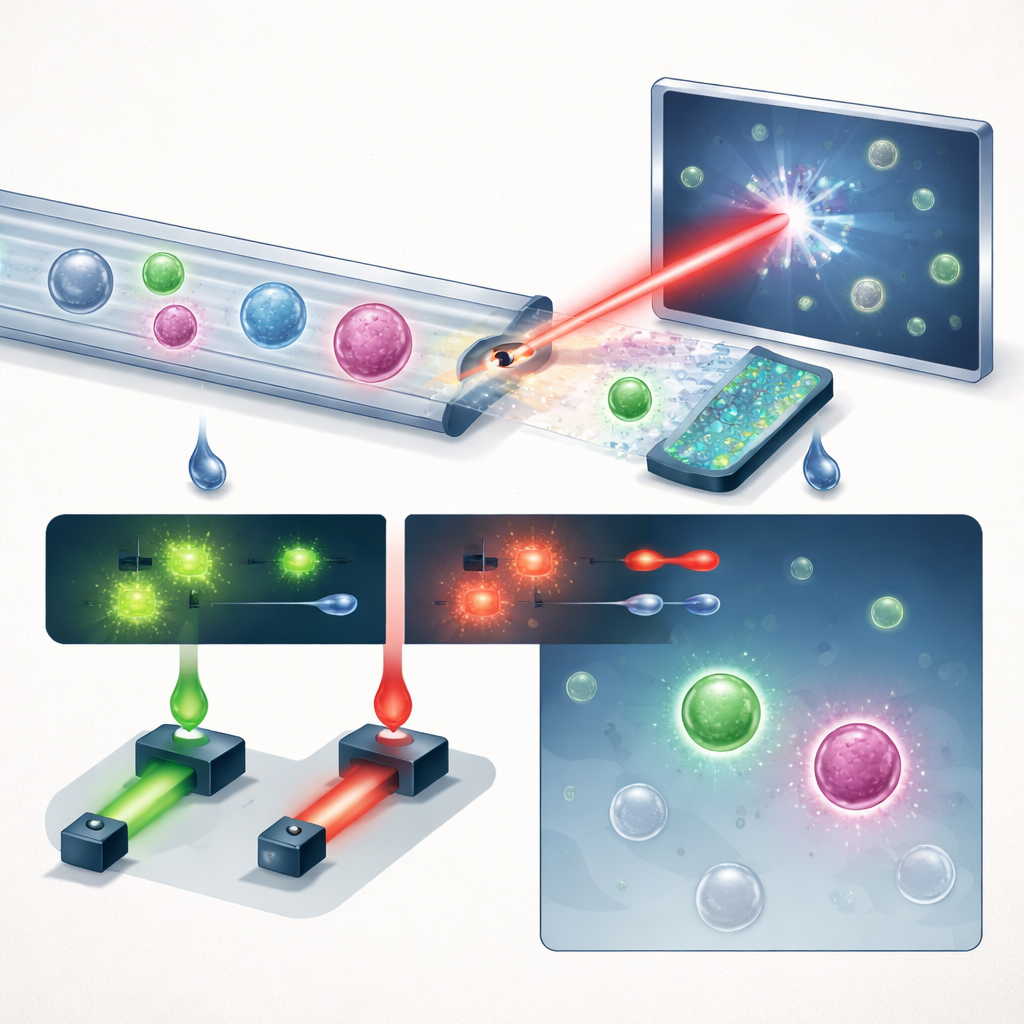
A equipe apresenta um sistema compacto que combina três ideias-chave: manipulação inteligente de fluidos, imageamento holográfico e aprendizado profundo, com uma dose útil de fluorescência. Primeiro, o sangue total é passado por um chip microfluídico em formato “serrilhado” que remove mais de 99,999% dos glóbulos vermelhos e quase todos os glóbulos brancos, preservando a grande maioria das células tumorais. Isso transforma uma amostra lotada em uma onde células raras têm mais chance de se destacar. O fluxo enriquecido então passa por um canal reto sob um laser violeta pulsado. Em vez de tirar imagens planas, o sistema grava hologramas — padrões de interferência que codificam tanto o brilho quanto a espessura óptica de cada célula, capturando sutis estruturas tridimensionais em um único instantâneo.
Ensinando uma rede neural a identificar as diferentes
Como CTCs verdadeiras são escassas, coletar diretamente exemplos reais de pacientes em quantidade suficiente para treinar um algoritmo é impraticável. Os pesquisadores, em vez disso, ensinaram um modelo de aprendizado profundo a reconhecer tudo o que não se parece com sangue comum. Eles alimentaram o modelo com milhões de hologramas de doadores saudáveis, mostrando toda a variedade de glóbulos brancos, vermelhos e detritos, e os equilibraram com imagens de várias linhagens de células cancerígenas cultivadas em laboratório. Uma rede neural especializada converte cada holograma em um mapa de calor de prováveis locais tumorais, tratando células como pontos-chave brilhantes em vez de caixas delimitadoras. Para escalar o treinamento sem rotulagem manual interminável, um modelo auxiliar primeiro marca todas as células em imagens puras de células cancerosas; o modelo principal então usa esses “pseudo‑rótulos”, além de uma função de perda ajustada para refletir quão raras são as CTCs reais, aprendendo a ser rigoroso sobre alarmes falsos ao mesmo tempo em que ainda captura células incomuns.
Testando o sistema
Em experimentos controlados nos quais números conhecidos de células de câncer de próstata foram acrescentados ao sangue saudável, a plataforma recuperou cerca de 60% dessas células em um ponto operacional escolhido, mantendo os falsos positivos abaixo de um por mililitro — mesmo com limiares de detecção liberais. Para afinar ainda mais suas decisões, o sistema também mede dois sinais fluorescentes de anticorpos contra PSMA, um marcador específico de próstata, e EpCAM. Durante os testes com pacientes, uma célula era contada como CTC se passasse tanto pelo limiar do aprendizado profundo holográfico quanto exibisse um forte sinal de PSMA, combinando informação morfológica sem rótulo com confirmação molecular direcionada. Quando os pesquisadores aplicaram isso a 13 homens com câncer de próstata avançado e 8 doadores saudáveis do sexo masculino, o grupo com câncer apresentou contagens de CTCs muito maiores (mediana de 12,5 células por mL) do que os controles (mediana de 1,5 células por mL). Notavelmente, apenas cerca de um terço das células positivas para PSMA carregava EpCAM, sugerindo que testes baseados exclusivamente em EpCAM perderiam a maioria das células tumorais nesses pacientes.
O que isso pode significar para os pacientes
Ao transformar uma coleta de sangue padrão em uma varredura automatizada e rica por células tumorais raras, esta plataforma aponta para biópsias líquidas mais práticas. Sua combinação de holografia sem rótulo, fluorescência direcionada e aprendizado profundo alcança baixa taxa de falsos positivos ao mesmo tempo em que captura CTCs que sistemas tradicionais baseados em marcadores ignoram. Hoje, isso significa melhor separação entre pacientes com câncer e indivíduos saudáveis em um estudo piloto de câncer de próstata. No futuro, a abordagem poderia ser adaptada a muitos tipos de tumor e fluidos, e pode eventualmente funcionar sem quaisquer marcadores fluorescentes, confiando puramente na aparência das células no espaço holográfico. Se totalmente comprovada em ensaios maiores e diversos, tais sistemas poderiam permitir que médicos monitorem a ascensão e queda do câncer ao longo do tempo com um simples exame de sangue, ajustem tratamentos mais cedo e recuperem células tumorais vivas para análise molecular detalhada — tudo sem bisturi.
Citação: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Palavras-chave: células tumorais circulantes, biópsia líquida, microscopia holográfica digital, diagnóstico por aprendizado profundo, câncer de próstata