Clear Sky Science · ru
Обнаружение циркулирующих опухолевых клеток у пациентов с онкологией с помощью потоковой голографии и глубинного обучения
Искать признаки рака в обычном анализе крови
Рак часто распространяется задолго до того, как опухоль становится видимой на снимке, отторгая отдельные клетки в кровоток. Эти скитающиеся «циркулирующие опухолевые клетки» редки, но дают важную информацию: они могут сигнализировать о наличии рака, показывать реакцию на лечение и предсказывать дальнейшее течение болезни. В этой статье описана новая технология, которая может быстро, бережно и с высокой точностью просеивать миллиарды клеток крови в поисках этих единичных опасных фрагментов — открывая перспективу рутинных анализов крови для мониторинга рака в реальном времени.
Почему эти редкие клетки важны
Циркулирующие опухолевые клетки (ЦОК) — это раковые клетки, оторвавшиеся от первичной или метастатической опухоли и попавшие в кровоток. Даже при развитом заболевании в миллилитре крови может содержаться миллиарды обычных эритроцитов и лейкоцитов, но лишь несколько ЦОК — иногда меньше одной. Тем не менее их количество и поведение тесно связаны с агрессивностью опухоли, устойчивостью к терапии и прогнозом пациента. Стандартные методы их поиска часто опираются на поверхностные маркеры, такие как EpCAM — белки на оболочке многих эпителиальных раковых клеток. Но по мере эволюции опухоли эти маркеры могут исчезать, и тогда часть наиболее опасных клеток ускользает от обнаружения.
Недостатки существующих тестов
Многие современные тесты на ЦОК пытаются поймать клетки по молекулярным «бейджам» или по физическим характеристикам, таким как размер и жесткость. Системы, основанные на маркерах, например те, что магнитно извлекают клетки с EpCAM, могут пропускать клетки, выключившие эти маркеры в процессе, связанном с метастазированием. Фильтры по размеру или плотности тоже дают сбои, поскольку некоторые опухолевые клетки по размеру и ощущению похожи на обычные лейкоциты. Устройства, комбинирующие несколько подходов — сложные микрофлюидные чипы, магниты или акустические силы — повышают чувствительность, но обычно за счет большей сложности, стоимости и потерь клеток. В результате многие платформы не могут одновременно быть достаточно простыми для рутинного клинического использования и достаточно чувствительными, чтобы охватить всё разнообразие опухолевых клеток.
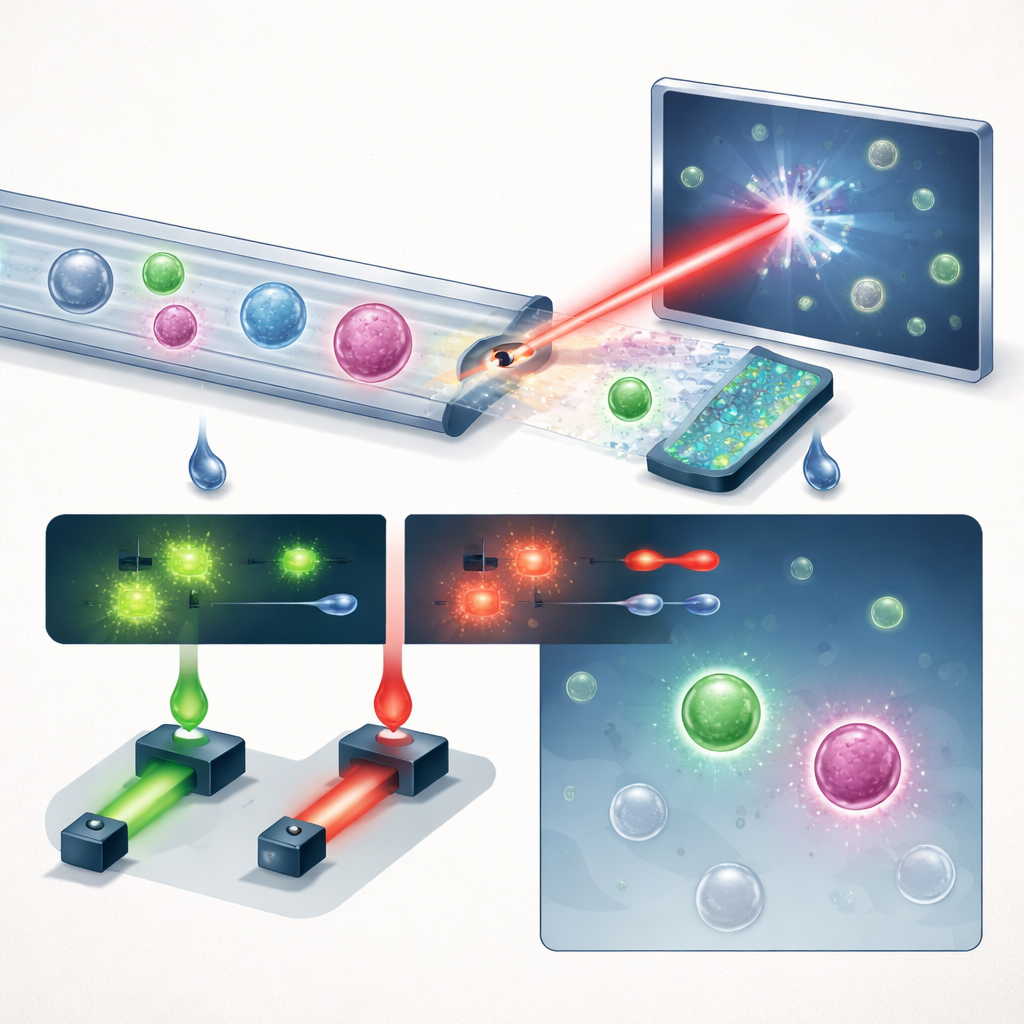
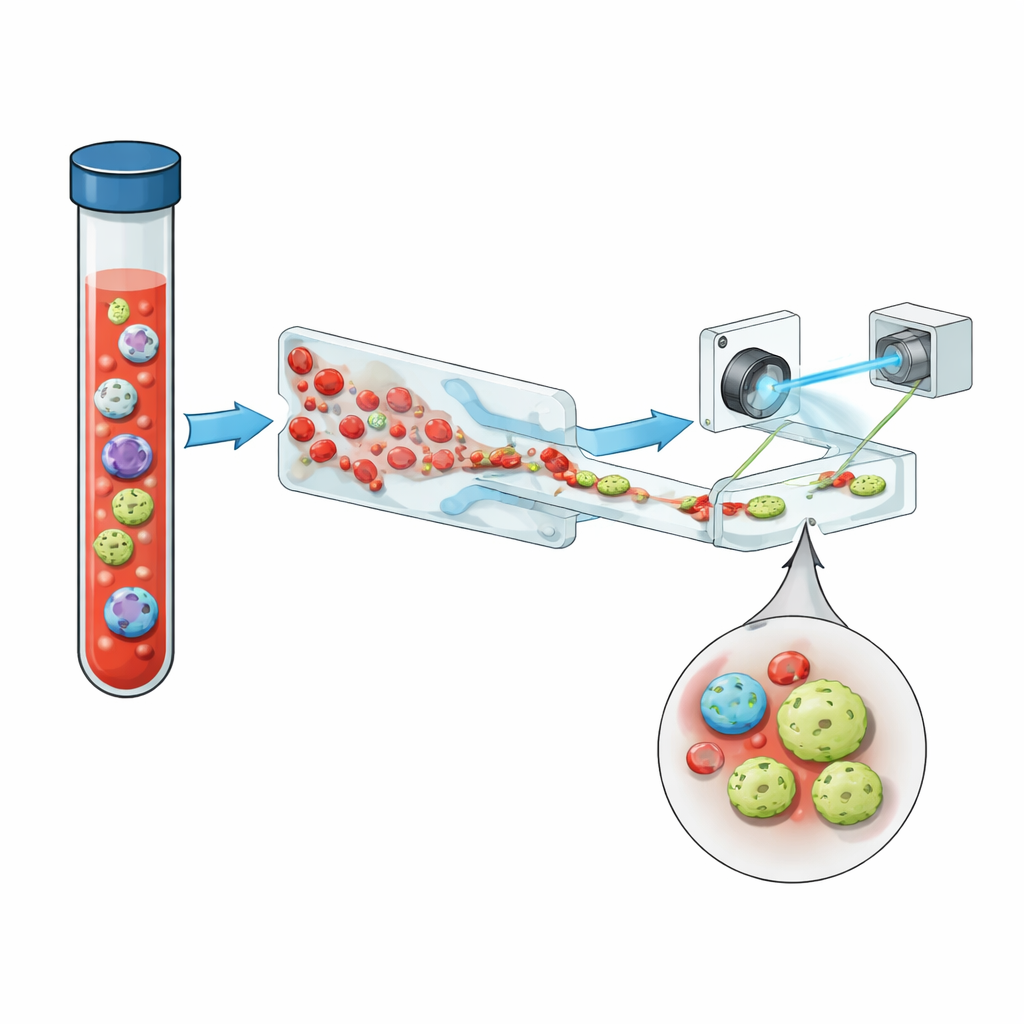
Новый способ «видеть» клетки в потоке
Авторы представляют компактную систему, объединяющую три ключевые идеи: интеллектуальную работу с жидкостью, голографическую съемку и глубокое обучение, с полезной дозой флуоресценции. Сначала цельную кровь пропускают через микрофлюидный чип «зубчатой» формы, который удаляет более 99,999% эритроцитов и практически все лейкоциты, сохраняя при этом подавляющее большинство опухолевых клеток. Это превращает плотный образец в такой, где редкие клетки легче заметить. Обогащённый поток затем проходит по простому прямому каналу под импульсным фиолетовым лазером. Вместо плоских снимков система записывает голограммы — интерференционные картины, кодирующие и яркость, и оптическую толщину каждой клетки, фиксируя тонкую трёхмерную структуру в одном кадре.
Обучение нейросети отмечать «чужеродные» клетки
Поскольку подлинные ЦОК встречаются редко, напрямую собрать достаточно реальных примеров пациентов для обучения алгоритма проблематично. Исследователи вместо этого научили модель глубокого обучения распознавать всё, что не выглядит как обычная кровь. Они снабдили модель миллионами голограмм от здоровых доноров, демонстрирующих всё разнообразие лейкоцитов, эритроцитов и мусора, и сбалансировали эти данные изображениями из множества разных линий раковых клеток, выращенных в лаборатории. Специализированная нейросеть преобразует каждую голограмму в тепловую карту вероятных локализаций опухолевых клеток, рассматривая клетки как светящиеся ключевые точки, а не как ограничивающие рамки. Чтобы масштабировать обучение без бесконечной ручной разметки, вспомогательная модель сначала отмечает все клетки на чистых изображениях раковых клеток; основная модель затем использует эти «псевдометки», а также функцию потерь, настроенную с учётом редкости реальных ЦОК, чтобы научиться строго относиться к ложным срабатываниям и одновременно улавливать необычные клетки.
Проверка системы
В контролируемых экспериментах, где в здоровую кровь добавляли известное количество клеток рака предстательной железы, платформа извлекала около 60% этих клеток при выбранной рабочей точке, сохраняя при этом менее одного ложноположительного события на миллилитр — даже при либеральных порогах обнаружения. Чтобы дополнительно уточнить решения, система также измеряет два флуоресцентных сигнала от антител к PSMA, маркеру, специфичному для предстательной железы, и к EpCAM. При тестировании пациентов клетка считалась ЦОК только если она одновременно проходила порог голографического глубокого обучения и демонстрировала сильный сигнал PSMA, сочетая безмаркёрную форму с целевой молекулярной верификацией. Когда исследователи применили метод к 13 мужчинам с прогрессирующим раком предстательной железы и 8 здоровым донорам-мужчинам, в группе рака наблюдалось существенно больше ЦОК (медиана 12,5 клеток на мл) чем в контроле (медиана 1,5 клеток на мл). Примечательно, что лишь около трети PSMA-положительных клеток имели EpCAM, что указывает на то, что тесты, опирающиеся только на EpCAM, пропустили бы большинство опухолевых клеток у этих пациентов.
Что это может значить для пациентов
Преобразуя стандартный забор крови в богатое, автоматизированное сканирование на редкие раковые клетки, эта платформа указывает путь к более практичным «жидкостным биопсиям». Её сочетание безмаркёрной голографии, таргетной флуоресценции и глубокого обучения обеспечивает низкий уровень ложноположительных результатов, одновременно улавливая ЦОК, которые традиционные системы, основанные на маркерах, пропускают. Сегодня это означает лучшую дифференциацию пациентов с раком и здоровых участников в пилотном исследовании рака предстательной железы. В перспективе подход может быть адаптирован к разным типам опухолей и биологическим жидкостям и в конечном итоге работать без каких‑либо флуоресцентных меток, опираясь исключительно на внешний вид клеток в голографическом пространстве. Если метод подтвердят в более крупных и разнообразных испытаниях, такие системы позволят врачам отслеживать прогресс или регресс рака во времени с помощью простого анализа крови, быстрее корректировать лечение и получать живые опухолевые клетки для детального молекулярного анализа — без скальпеля.
Цитирование: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Ключевые слова: циркулирующие опухолевые клетки, жидкостная биопсия, цифровая голографическая микроскопия, диагностика с помощью глубокого обучения, рак предстательной железы