Clear Sky Science · sv
Detektion av cirkulerande tumörceller hos cancerpatienter med in-flow djupinlärningsholografi
Att hitta cancerledtrådar i ett enkelt blodprov
Cancer sprider sig ofta långt innan en tumör syns på en skanning, genom att skicka ut enstaka celler i blodomloppet. Dessa kringströvande "cirkulerande tumörceller" är sällsynta men viktiga ledtrådar: de kan signalera att cancer finns, följa hur den svarar på behandling och ge en fingervisning om vad som kan ske härnäst. Denna studie beskriver en ny teknik som snabbt, varsamt och med hög noggrannhet kan sålla igenom miljarder blodceller för att hitta dessa få farliga avvikare—vilket öppnar för rutinmässiga blodtester som kan övervaka cancer i realtid.
Varför dessa sällsynta celler är viktiga
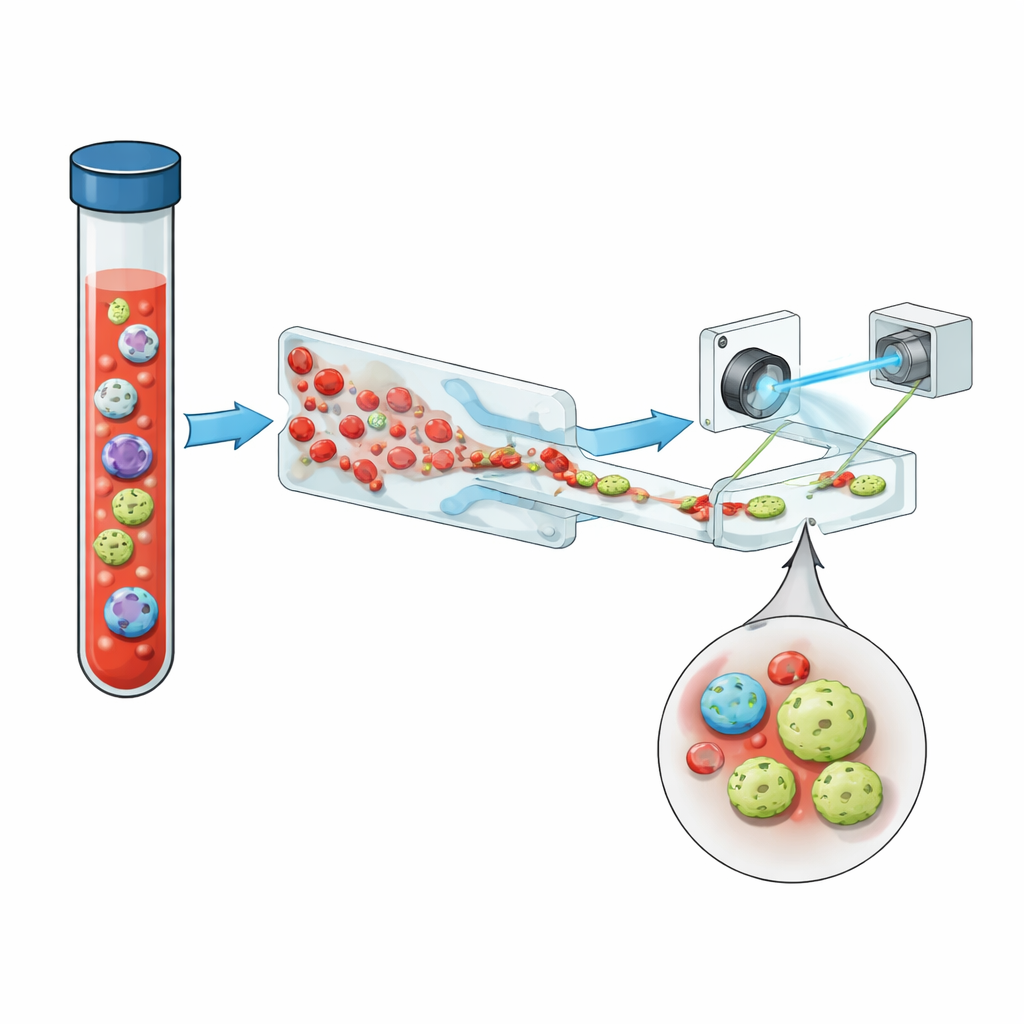
Cirkulerande tumörceller (CTC) är cancerceller som brutit sig loss från en primär eller metastatisk tumör och hamnat i blodomloppet. Även vid avancerad sjukdom kan en milliliter blod innehålla miljarder normala röda och vita blodkroppar men bara ett fåtal CTC—ibland färre än en. Ändå är deras antal och beteende nära kopplat till hur aggressiv en tumör är, om den är resistent mot behandling och hur lång tid patienten sannolikt har kvar. Standardmetoder för att hitta dem förlitar sig ofta på ytmarkörer som EpCAM, proteiner på ytan av många epiteliala cancerceller. Men när tumörer utvecklas och ändrar tillstånd kan dessa markörer försvinna, vilket innebär att några av de farligaste cellerna kan undgå upptäckt.
Brister i nuvarande tester
Många befintliga blodtester för CTC försöker fånga celler via deras molekylära "namnskyltar" eller via fysiska egenskaper som storlek och styvhet. Markörbaserade system, såsom de som magnetiskt drar ut EpCAM-bärande celler, kan missa tumörceller som stängt av dessa markörer under en formförändrande process kopplad till metastasering. Storleks- eller densitetsbaserade filter kan också misslyckas, eftersom vissa tumörceller är lika stora och liknar vita blodkroppar i känsla. Enheter som kombinerar flera trick—komplexa mikrofluidiska chip, magneter eller akustiska krafter—ökar känsligheten men ofta på bekostnad av större komplexitet, högre kostnad och cellförluster. Som en följd har många plattformar svårt att vara både tillräckligt enkla för rutinmässig klinisk användning och känsliga nog att fånga tumörcellernas hela mångfald.
Ett nytt sätt att se celler i flöde
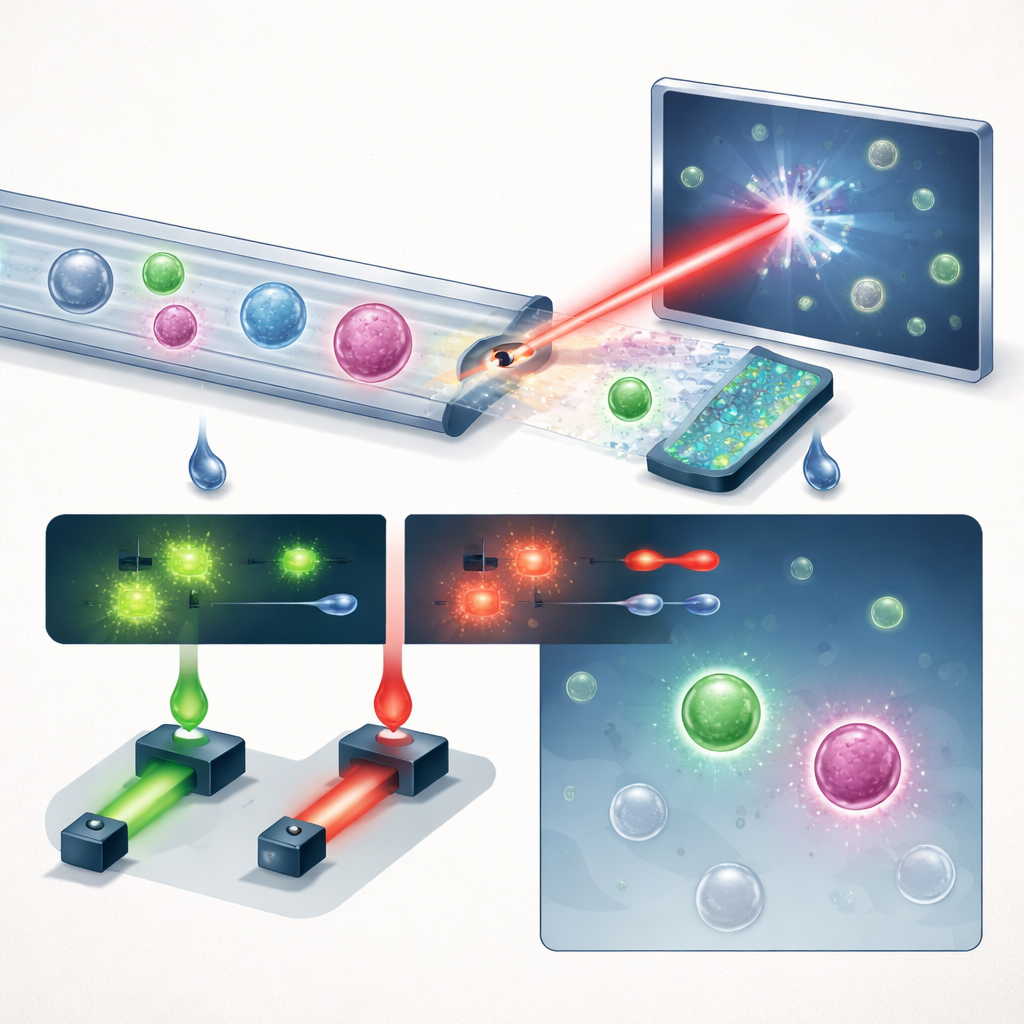
Forskargruppen presenterar ett kompakt system som kedjar ihop tre nyckelidéer: smart vätskahantering, holografisk avbildning och djupinlärning, med en hjälpsam dos fluorescens. Först leds helblod genom ett "sågtands"-mikrofluidiskt chip som tar bort mer än 99,999 % av röda blodkroppar och nästan alla vita blodkroppar, samtidigt som majoriteten av tumörcellerna bevaras. Det förvandlar ett trångt prov till ett där sällsynta celler har bättre chans att sticka ut. Den berikade strömmen rinner sedan genom en enkel rak kanal under en pulserande violett laser. Istället för att ta plana bilder registrerar systemet hologram—interferensmönster som kodar både ljusstyrka och optisk tjocklek hos varje cell, vilket fångar subtil tredimensionell struktur i en enda ögonblicksbild.
Att lära ett neuralt nätverk att upptäcka de udda
Eftersom verkliga CTC är sällsynta är det opraktiskt att samla tillräckligt många riktiga patientexempel för att träna en algoritm direkt. Forskarna lärde istället en djupinlärningsmodell att känna igen allt som inte ser ut som vanligt blod. De matade den med miljontals hologram från friska givare, som visade hela variationen av vita och röda blodkroppar och skräp, och balanserade dem med bilder från många olika cancercellinjer odlade i laboratoriet. Ett specialiserat neuralt nätverk omvandlar varje hologram till en värmekarta över troliga tumörlokaler, och behandlar celler som lysande punkter snarare än rutor. För att skala upp träningen utan ändlösa manuella märkningar markerar en hjälparmodell först alla celler i rena cancercellbilder; huvudmodellen använder sedan dessa "pseudoetiketter", plus en förlustfunktion anpassad för att återspegla hur sällsynta verkliga CTC är, för att lära sig vara strikt mot falska larm samtidigt som den fortfarande fångar ovanliga celler.
Att testa systemet
I kontrollerade experiment där kända antal prostataceller tillsattes i hälsosamt blod återvann plattformen cirka 60 % av dessa celler vid en vald driftpunkt, samtidigt som falska positiva hölls under en per milliliter—even vid långtgående detektionsgränser. För att ytterligare skärpa besluten mäter systemet också två fluorescerande signaler från antikroppar mot PSMA, en prostataselektiv markör, och EpCAM. Under patienttester krävdes att en cell räknades som CTC både passade holografi-djupinlärningens tröskel och visade en stark PSMA-signal, vilket kombinerar märkningsfri forminformation med riktad molekylär bekräftelse. När forskarna tillämpade detta på 13 män med avancerad prostatacancer och 8 friska manliga givare visade cancerguppen mycket högre CTC-tal (median 12,5 celler per ml) än kontrollerna (median 1,5 celler per ml). Slående nog bar bara omkring en tredjedel av PSMA-positiva celler EpCAM, vilket tyder på att tester som enbart förlitar sig på EpCAM skulle missa majoriteten av tumörcellerna hos dessa patienter.
Vad detta kan betyda för patienterna
Genom att förvandla ett standardblodprov till en rik, automatiserad sökning efter sällsynta cancerceller pekar denna plattform mot mer praktiska "flytande biopsier." Dess blandning av märkningsfri holografi, riktad fluorescens och djupinlärning når en låg frekvens av falska positiva samtidigt som den fångar CTC som traditionella markörbaserade system förbiser. I dag innebär det bättre separation av cancerpatienter från friska individer i en pilotstudie om prostatacancer. Framöver skulle metoden kunna anpassas till många tumörtyper och vätskor, och kanske så småningom fungera utan några fluorescerande markörer alls, genom att förlita sig enbart på hur celler ser ut i holografiskt utrymme. Om den fullt ut bekräftas i större, mångsidiga prövningar skulle sådana system kunna låta läkare följa cancerns uppgång och nedgång över tid med ett enkelt blodprov, justera behandlingar snabbare och återvinna levande tumörceller för detaljerad molekylär analys—allt utan skalpell.
Citering: Mallery, K., Bristow, N.R., Heller, N. et al. Circulating tumor cell detection in cancer patients using in-flow deep learning holography. npj Biosensing 3, 23 (2026). https://doi.org/10.1038/s44328-026-00084-z
Nyckelord: cirkulerande tumörceller, flytande biopsi, digital holografisk mikroskopi, djupinlärningsdiagnostik, prostatacancer