Clear Sky Science · tr
CD8+ T hücresi farklılaşma durumlarında STAT5 paraloglarının asimetri ve yedekliliği
Gelecekteki immün tedaviler açısından bunun önemi
Günümüzde en umut verici kanser ve otoimmün tedavilerin çoğu, özellikle CD8+ “katil” T hücreleri olmak üzere kendi bağışıklık hücrelerimizi daha agresif dövüşmeye veya sakinleşmeye teşvik ederek çalışır. Bu hücrelerdeki önemli moleküler anahtar STAT5 adlı bir proteindir ve aslında iki neredeyse ikiz versiyonu vardır. Bu çalışma, terapötik açıdan büyük sonuçları olabilecek aldatıcı derecede basit bir soruyu soruyor: bu ikizler gerçekten yer değiştirebilir mi, yoksa biri sessizce yöneten taraf mı?
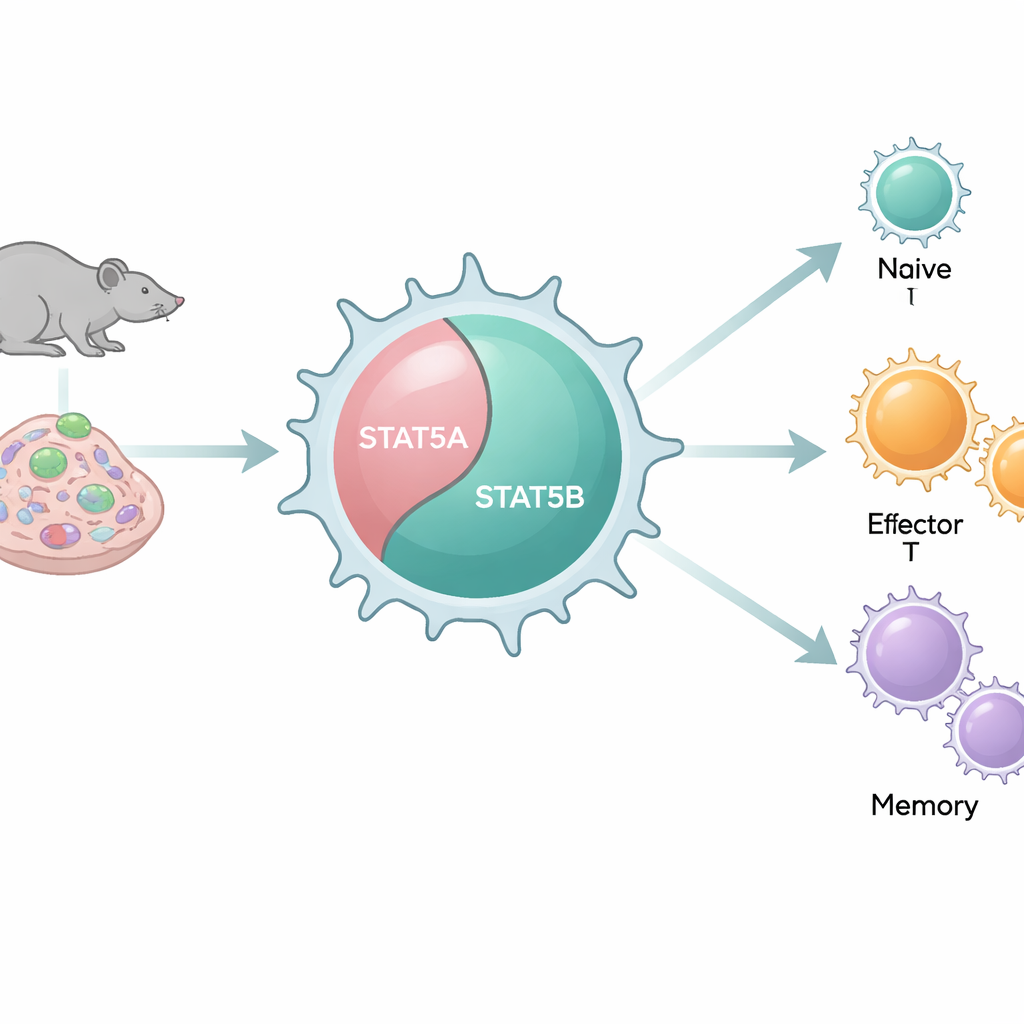
Benzer iki anahtar ama farklı davranışlar
Genomlarımızda STAT5’in iki yakın akraba kopyası yani paralogu bulunur: STAT5A ve STAT5B. Moleküler düzeyde birbirine çok benzediği ve birçok aynı DNA dizisine bağlandığı için genellikle yedek parçalar gibi ele alınmıştır. Buna karşın STAT5B’de zararlı mutasyonları olan hastalarda ciddi bağışıklık sorunları görülürken, benzer STAT5A kusurları nadirdir. Yazarlar, STAT5A’yı, STAT5B’yi veya her ikisini çeşitli kombinasyonlarla sistematik olarak ortadan kaldıran bir dizi fare modeli kullanarak, her paralogun canlı organizmalarda ve hücrelerde CD8+ T hücrelerinin sayısını ve davranışını nasıl şekillendirdiğini incelediler.
Katil T hücrelerinin dengesini korumada STAT5B’nin kilit rolü
Toplam STAT5 düzeyi azaltıldığında, CD8+ T hücreleri lenf düğümlerinde, dalakta ve kemik iliğinde keskin şekilde azaldı ve yardımcı (CD4+) ile katil (CD8+) T hücreleri arasındaki oranlar kaydı. Karışık kemik iliği nakilleri, bunun büyük ölçüde hücrelerin çevresindeki değişikliklerden ziyade T hücrelerinin kendi içindeki bir sorundan kaynaklandığını gösterdi. Kayıp, STAT5B yok olduğunda en şiddetliydi ve yalnızca tek bir STAT5A kopyasına güvenen fareler en kötü durumda kaldı. Aynı zamanda kalan CD8+ T hücreleri dinlenmiş, naive durumdan daha deneyimli efektör ve bellek durumlarına kaydı; fakat paradoksal olarak belirli enzimler ve reseptörler gibi anahtar öldürme araçlarıyla tam donanımlı hale gelemediler. Bu bulgu, STAT5’i katil T hücrelerinin hem sayısının hem de kalitesinin koruyucusu olarak ortaya koyuyor ve STAT5B’nin en fazla ağırlığı taşıdığını gösteriyor.
Kapağın altında eşitsiz ortaklar
Daha derine inildiğinde, ekip her paralogdan ne kadar bulunduğunu ve hangisi eksik olduğunda genlerin nasıl yanıt verdiğini ölçtü. CD8+ T hücrelerinde STAT5B, toplam STAT5 proteini ve mesajının yaklaşık üçte ikisini oluşturuyordu. STAT5B kaybı, yolun ana fosforilasyon aktivasyonunu STAT5A kaybından daha fazla azalttı. Araştırmacılar naive, efektör ve bellek CD8+ T hücrelerinden IL-7 ve IL-15 olmak üzere iki sitokinle uyarıldığında RNA dizilemesi yaptıklarında, sadece STAT5A eksik olduğunda olduğundan çok daha fazla genin düzensizleştiğini buldular. Bu genlerin birçoğu hayatta kalma, metabolizma ve bellek oluşumunu kontrol ediyor; bu da STAT5B’yi katil T hücrelerinde sitokin tepkilerinin ana itici gücü olarak vurguluyor.
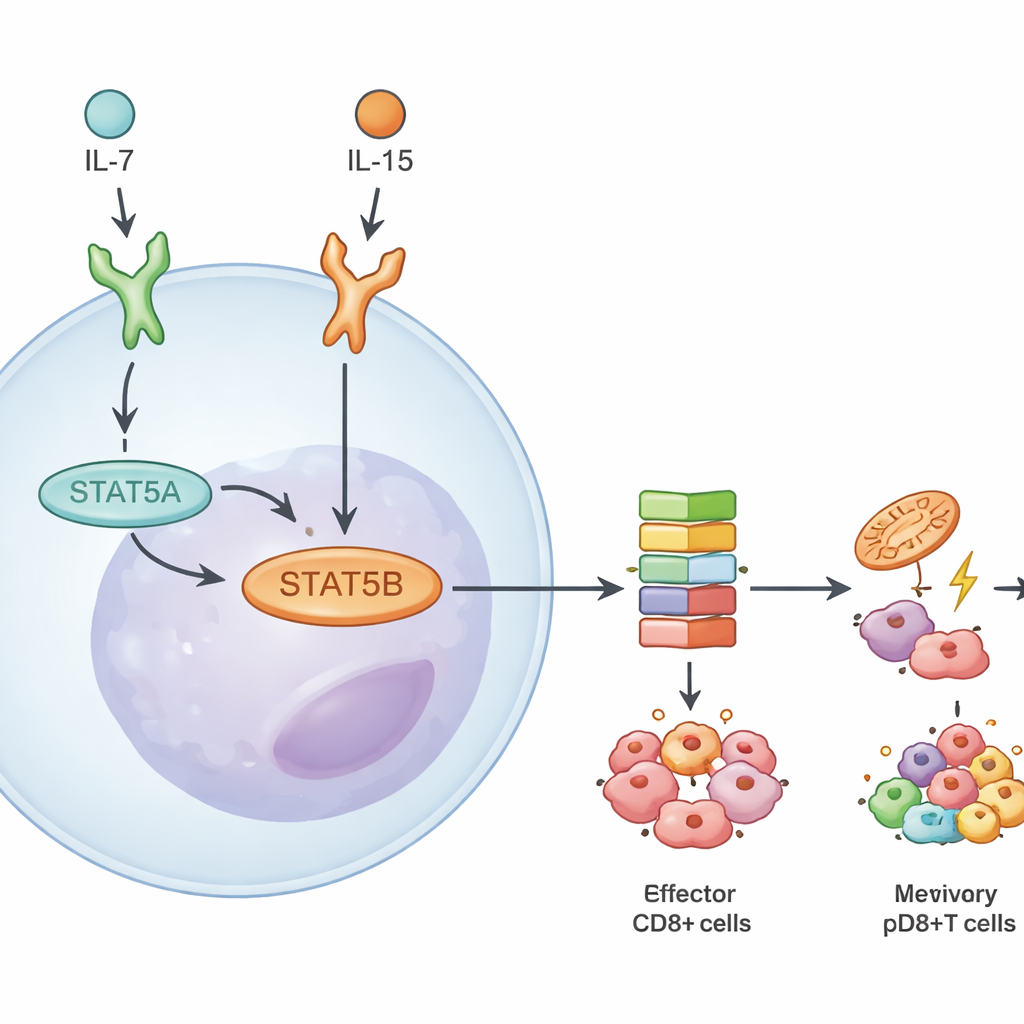
Paylaşılan DNA hedefleri ama bağlama özgü etkiler
STAT5B’nin baskınlığına rağmen, iki paralogun genomun büyük kısmında aynı bölgeleri işgal ettiği görüldü. Bağlanma haritaları kullanıldığında, yüksek etkili DNA bölgelerinin çoğunun hem STAT5A hem de STAT5B tarafından bağlandığı gözlendi. Eksik hücrelere sürekli etkin bir STAT5A formu yeniden verildiğinde, büyük ölçüde STAT5B tarafından da erişilebilen genleri güçlendirdi; bu, gerçekten STAT5A-özel hedeflerin nadir ve görece zayıf olduğunu öne sürüyor. Farklılıklar bunun yerine STAT5B’nin ne kadar güçlü ve hangi durumlarda hareket ettiğinden kaynaklandı. Tepkiler hangi sitokinin sinyal verdiğine (IL-7 vs IL-15), T hücresinin naive mi yoksa bellek mi olduğuna ve CD4+ ya da CD8+ soyuna ait olup olmadığına göre değişti. Örneğin IL-15, özellikle bellek CD8+ T hücrelerinde IL-7’den daha geniş STAT5B odaklı gen programlarını tetikledi.
Hastalıkta STAT5 aktivitesini izlemek için bir gen imzası
Bu yolun özünü yakalamak için araştırmacılar farklı sitokinler ve CD8+ T hücresi durumları arasında ortaya çıkan 85 genlik bir “çekirdek STAT5 imzası” çıkardılar. Bu imzayı virüsle enfekte farelerden alınan tek hücre RNA verisine yerleştirdiklerinde, erken efektör veya erken tükenmişlik gösteren CD8+ T hücrelerinin belirgin bir kümesini aydınlattı; bunlar güçlü, taze sitokin uyarımı yaşayan hücrelerdi. İmza tam tükenmiş veya dinlenmiş hücrelerde çok daha az aktiftı; bu da onun bağışıklık yanıtları sırasında yoğun STAT5 sinyalleşmesini —ve belki de anormal STAT5B aktivitesiyle sürüklenen kanserlerde— bioinformatik bir işaretçi olarak kullanılabileceğini düşündürüyor.
Hastalar ve tedaviler için bunun anlamı
Uzman olmayan bir okuyucu için alınacak sonuç şudur: STAT5A ve STAT5B aynı kontrol panelindeki iki kol gibidir, ama biri—STAT5B—daha uzun ve daha sık çekilen koldur. Her ikisi de katil T hücrelerinin nasıl hayatta kaldığına, dinlendiğine ve hatırladığına katkı sağlarken, STAT5B sayılarına ve kritik gen programlarına özgün ve güçlü bir etki yapar. Bu asimetrinin açıklığa kavuşturulması ve STAT5 aktivitesine dayalı bir gen imzası sunulması, sitokin ilaçlarını ayarlamak, T hücrelerini mühendislik ile geliştirmek veya hasta genom verilerini yorumlamak gibi daha hassas immünoterapi tasarımları için kavramsal bir harita sağlar; böylece katil T hücrelerinin gücünden faydalanılırken bağışıklık sistemi hastalığa kaydırılmamış olur.
Atıf: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Anahtar kelimeler: STAT5B, CD8 T hücreleri, sitozin sinyallemesi, immünoterapi, T hücresi farklılaşması