Clear Sky Science · es
Asimetría y redundancia de los paralogos STAT5 a lo largo de los estados de diferenciación de las células T CD8+
Por qué importa para futuras terapias inmunes
Muchas de las terapias contra el cáncer y las enfermedades autoinmunes más prometedoras de hoy funcionan estimulando a nuestras propias células inmunitarias, en especial a las células T CD8+ “asesinas”, para que actúen con más intensidad o se contengan. Un interruptor molecular clave en estas células es una proteína llamada STAT5, que en realidad existe en dos versiones casi gemelas. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones terapéuticas: ¿son estos gemelos realmente intercambiables o uno de ellos dirige el proceso en silencio?
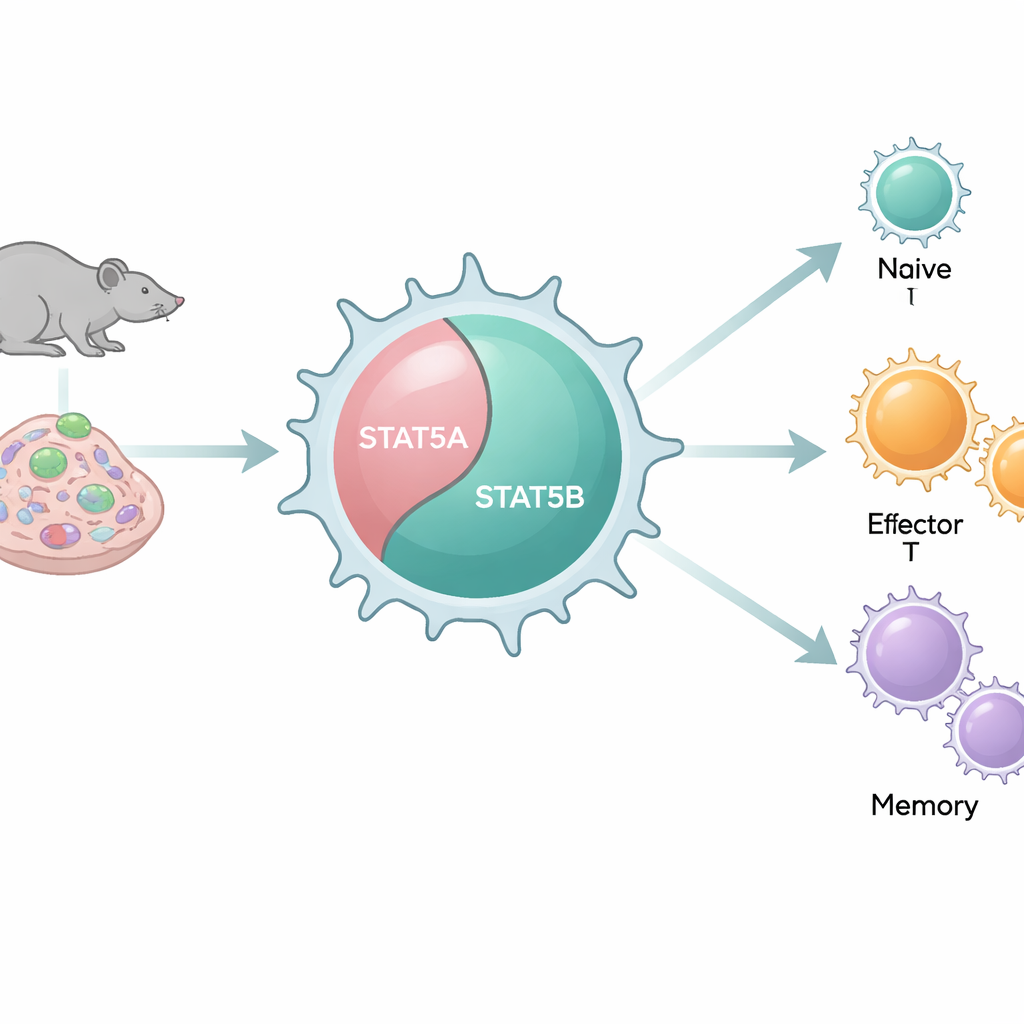
Dos interruptores similares que se comportan de forma diferente
Nuestros genomas contienen dos copias estrechamente relacionadas, o paralogos, de STAT5: STAT5A y STAT5B. Debido a que se parecen mucho a nivel molecular y se unen a muchos de los mismos tramos de ADN, a menudo se han considerado partes redundantes. Sin embargo, los pacientes con mutaciones dañinas en STAT5B desarrollan problemas inmunitarios graves, mientras que defectos comparables en STAT5A son raros. Usando una batería de modelos murinos que eliminan sistemáticamente STAT5A, STAT5B o ambos en distintas combinaciones, los autores exploran cómo cada paralogo moldea el número y el comportamiento de las células T CD8+ en organismos y en células.
Papel clave de STAT5B para mantener el equilibrio de las células T asesinas
Cuando los niveles totales de STAT5 se redujeron, las células T CD8+ disminuyeron drásticamente en los ganglios linfáticos, el bazo y la médula ósea, lo que provocó proporciones alteradas entre células T colaboradoras (CD4+) y células T asesinas (CD8+). Trasplantes de médula ósea mixta mostraron que esto se debe en gran medida a un problema intrínseco de las propias células T, y no solo a cambios en su entorno. La pérdida fue más severa cuando faltaba STAT5B, y los ratones que dependían de una única copia de STAT5A tuvieron el peor desempeño. Al mismo tiempo, las células T CD8+ restantes se desplazaron desde un estado de reposo y naïve hacia estados más experimentados, efectores y de memoria, pero paradójicamente no pudieron equiparse por completo con herramientas clave de matanza, como ciertas enzimas y receptores. Esto revela a STAT5 como guardián tanto de la cantidad como de la calidad de las células T asesinas, con STAT5B llevando el mayor peso.
Socios desiguales bajo el capó
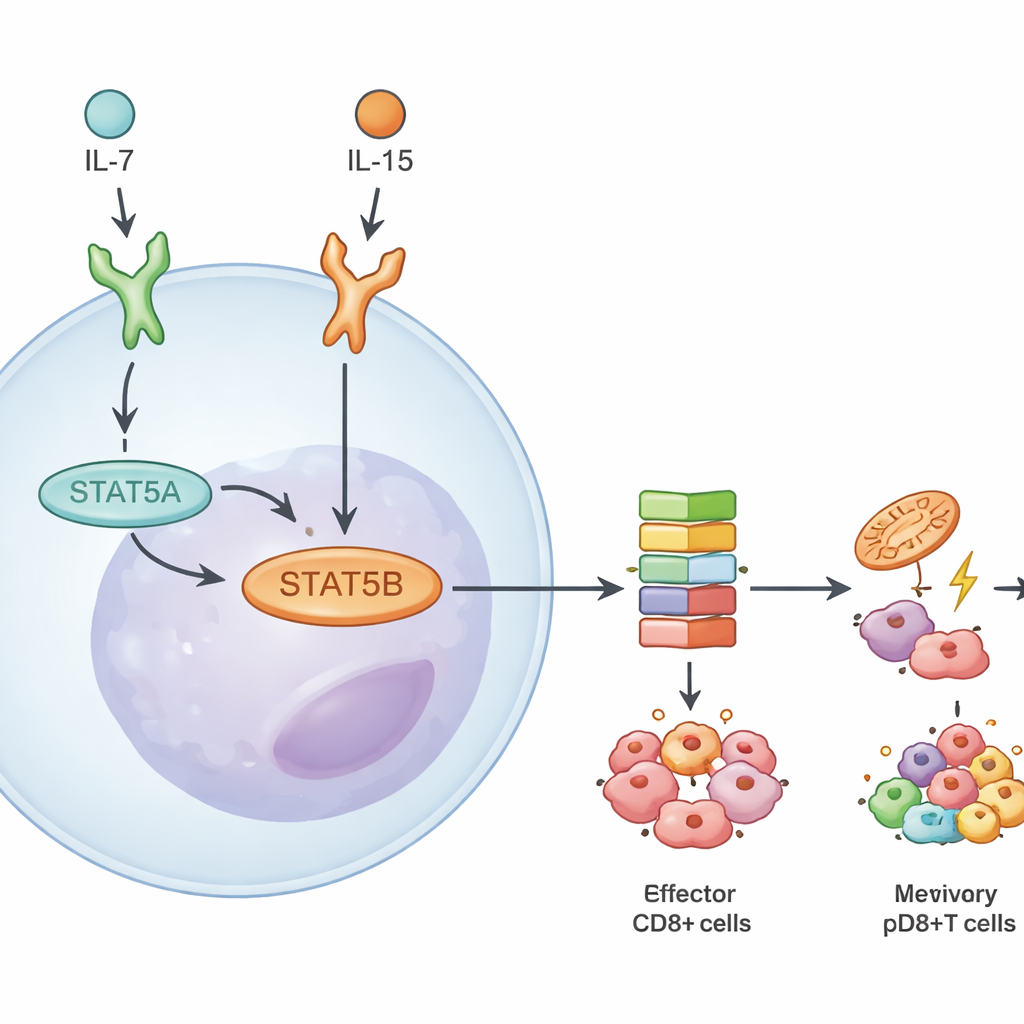
Indagando más, el equipo midió cuánto de cada paralogo está presente y cómo responden los genes cuando falta uno u otro. En las células T CD8+, STAT5B constituía aproximadamente dos tercios de la proteína y del ARN mensajero total de STAT5. La pérdida de STAT5B redujo la activación del paso clave de fosforilación de la vía más que la pérdida de STAT5A. Cuando los investigadores secuenciaron el ARN de células T CD8+ naïve, efectoras y de memoria estimuladas por dos citoquinas, IL-7 e IL-15, encontraron muchos más genes desregulados en ausencia de STAT5B que cuando solo faltaba STAT5A. Muchos de estos genes controlan la supervivencia, el metabolismo y la formación de memoria, lo que subraya a STAT5B como el principal impulsor de las respuestas a citoquinas en las células T asesinas.
Objetivos de ADN compartidos pero acciones específicas según el contexto
A pesar del dominio de STAT5B, ambos paralogos ocuparon gran parte del mismo territorio genómico. Usando mapas de unión, los autores observaron que la mayoría de los sitios de ADN de alto impacto estaban unidos por STAT5A y STAT5B. Cuando reintrodujeron una forma siempre activa de STAT5A en células deficientes, esta aumentó en gran medida los genes que también eran accesibles para STAT5B, lo que sugiere que los verdaderos objetivos exclusivos de STAT5A son raros y relativamente débiles. En cambio, las diferencias surgieron según la intensidad y las situaciones en que actúa STAT5B. Las respuestas variaron según la citoquina que señalaba (IL-7 frente a IL-15), si la célula T era naïve o de memoria y si pertenecía a la línea CD4+ o CD8+. IL-15, por ejemplo, desencadenó programas génicos impulsados por STAT5B más amplios que IL-7, especialmente en las células T CD8+ de memoria.
Una firma génica para rastrear la actividad de STAT5 en la enfermedad
Para capturar la esencia de esta vía, los investigadores destilaron una “firma central de STAT5” de 85 genes que apareció a través de diferentes citoquinas y estados de las células T CD8+. Cuando sobrepusieron esta firma a datos de ARN unicelular de ratones infectados por un virus, iluminó un clúster distinto de células T CD8+ de efector temprano o de agotamiento temprano, las mismas células que experimentan una estimulación citocínica intensa y reciente. La firma fue mucho menos activa en células plenamente agotadas o en reposo, lo que sugiere que puede actuar como un faro bioinformático para la señalización intensa de STAT5 durante las respuestas inmunitarias y, quizás, en cánceres impulsados por actividad aberrante de STAT5B.
Qué significa esto para pacientes y terapias
Para un lector no especialista, la idea principal es que STAT5A y STAT5B son como dos palancas en el mismo panel de control, pero una palanca, STAT5B, es más larga y se acciona con más frecuencia. Ambas contribuyen a cómo las células T asesinas sobreviven, descansan y recuerdan, pero STAT5B ejerce una influencia singularmente fuerte sobre su número y sobre programas génicos críticos. Al aclarar esta asimetría y ofrecer una firma basada en genes de la actividad de STAT5, el estudio proporciona un mapa conceptual para diseñar inmunoterapias más precisas—ya sea afinando fármacos citocínicos, diseñando células T o interpretando datos genómicos de pacientes—que aprovechen el poder de las células T asesinas sin desequilibrar el sistema inmunitario hasta causar enfermedad.
Cita: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Palabras clave: STAT5B, Células T CD8, señalización por citoquinas, inmunoterapia, diferenciación de células T