Clear Sky Science · nl
Asymmetrie en redundantie van STAT5-paralogen gedurende differentiatietoestanden van CD8+ T-cellen
Waarom dit belangrijk is voor toekomstige immuuntherapieën
Veel van de meest veelbelovende behandelingen voor kanker en auto-immuunziekten van vandaag stimuleren of remmen onze eigen afweercellen—vooral CD8+ "killer" T-cellen—zodat ze harder vechten of juist bijstellen. Een sleutelschakelaar op moleculair niveau in deze cellen is een eiwit genaamd STAT5, dat in twee vrijwel identieke versies voorkomt. Deze studie stelt een misleidend eenvoudige vraag met grote therapeutische implicaties: zijn deze tweelingen echt uitwisselbaar, of voert de één stiekem de boventoon?
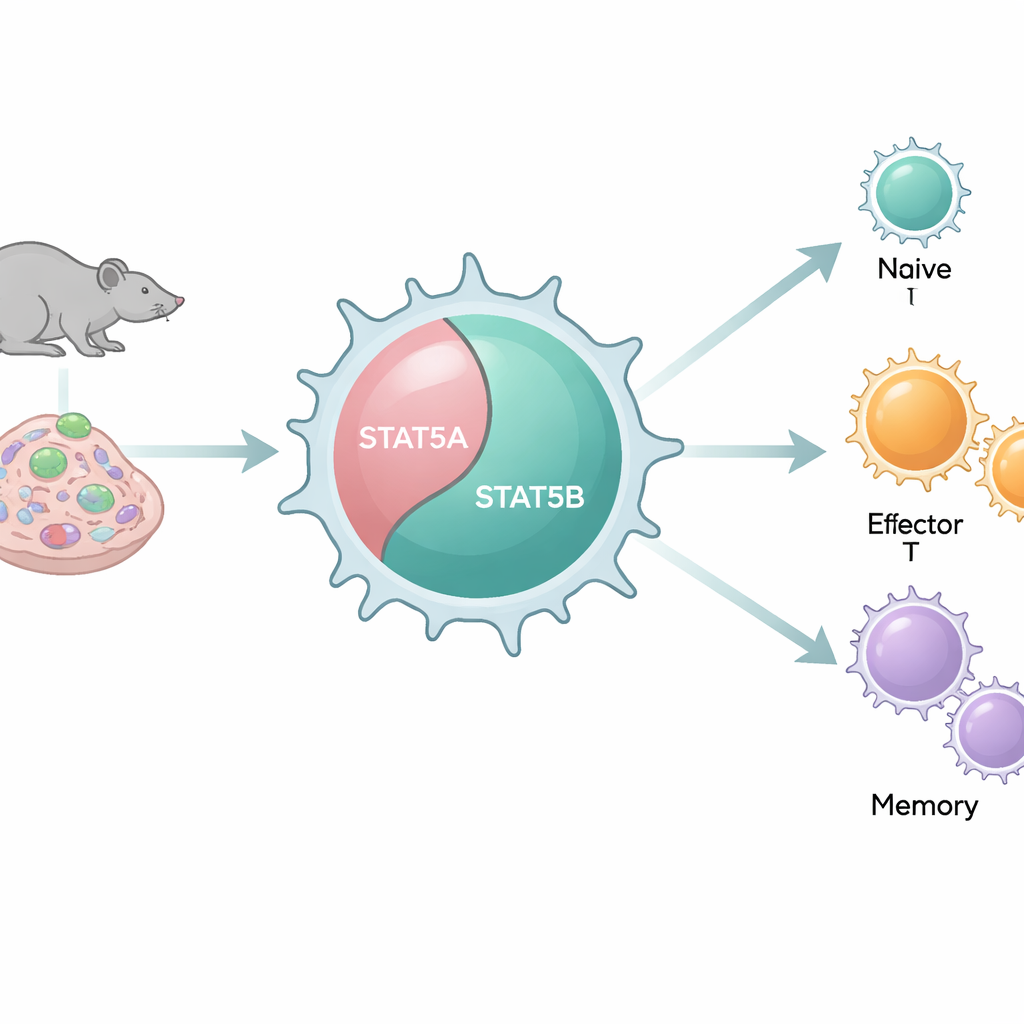
Twee vergelijkbare schakelaars met verschillend gedrag
Ons genoom bevat twee nauw verwante kopieën, of paralogen, van STAT5: STAT5A en STAT5B. Omdat ze op moleculair niveau zo op elkaar lijken en veel van dezelfde DNA-regio’s binden, werden ze vaak als redundante onderdelen beschouwd. Toch ontwikkelen patiënten met schadelijke STAT5B-mutaties ernstige immuunproblemen, terwijl vergelijkbare STAT5A-defecten zeldzaam zijn. Met een reeks muismodellen die systematisch STAT5A, STAT5B of beide in verschillende combinaties verwijderen, onderzoeken de auteurs hoe elke paralog aantallen en gedrag van CD8+ T-cellen in levende organismen en cellen beïnvloedt.
Belangrijke rol van STAT5B bij het in balans houden van killer T-cellen
Wanneer de totale STAT5-niveaus werden verlaagd, daalden CD8+ T-cellen sterk in lymfeklieren, milt en beenmerg, wat leidde tot verstoorde verhoudingen tussen helper- (CD4+) en killer- (CD8+) T-cellen. Gemengde beenmergtransplantaties toonden aan dat dit grotendeels te wijten is aan een probleem binnen de T-cellen zelf, en niet alleen aan veranderingen in hun omgeving. Het verlies was het ernstigst wanneer STAT5B ontbrak, en muizen die op één kopie STAT5A moesten vertrouwen, deden het het slechtst. Tegelijkertijd verschoof de overgebleven CD8+ T-celpopulatie van een rustende, naïeve toestand naar meer ervaren effector- en geheugenstaten, maar kon paradoxaal genoeg zichzelf niet volledig bewapenen met belangrijke dodelijke gereedschappen zoals specifieke enzymen en receptoren. Dit toont STAT5 als een bewaker van zowel het aantal als de kwaliteit van killer T-cellen, waarbij STAT5B het grootste gewicht draagt.
Ongelijke partners onder de motorkap
Dieper gravend maten de onderzoekers hoeveel van elke paralog aanwezig is en hoe genen reageren wanneer één van beide ontbreekt. In CD8+ T-cellen bestond STAT5B uit ongeveer twee derde van het totale STAT5-eiwit en -transcript. Verlies van STAT5B verminderde de activatie van de sleutel-fosforylatiestap in de route meer dan verlies van STAT5A. Toen de onderzoekers RNA-sequencing uitvoerden op naïeve, effector- en geheugen-CD8+ T-cellen die werden gestimuleerd door twee cytokines, IL-7 en IL-15, vonden ze veel meer verkeerd gereguleerde genen bij afwezigheid van STAT5B dan wanneer alleen STAT5A ontbrak. Veel van deze genen regelen overleving, metabolisme en geheugenvorming, wat STAT5B onderstreept als de belangrijkste bestuurder van cytokine-responsen in killer T-cellen.
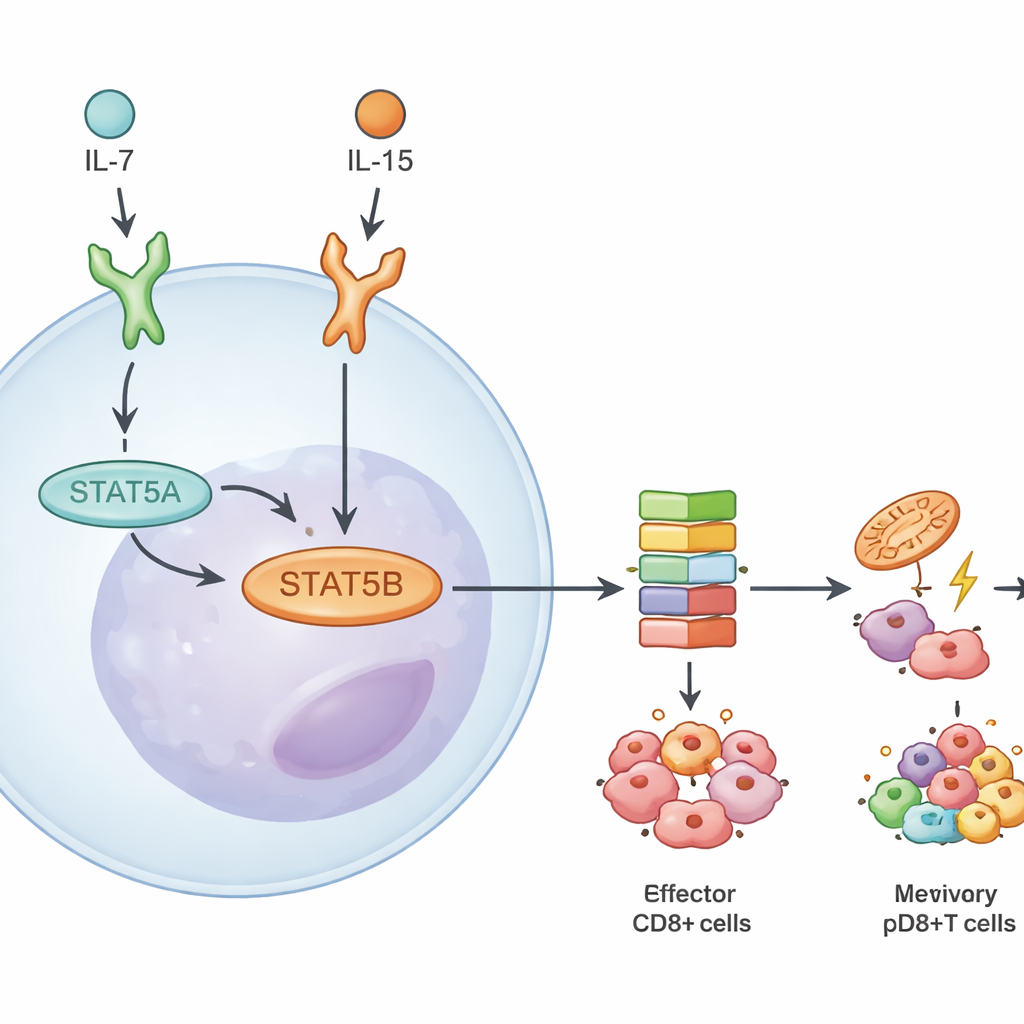
Gedeelde DNA-doelen maar contextspecifieke acties
Ondanks de dominantie van STAT5B, bleken de twee paralogen veel van hetzelfde genomische terrein te bezetten. Met behulp van bindingskaarten zagen de auteurs dat de meeste hoog-impact DNA-locaties door zowel STAT5A als STAT5B werden gebonden. Toen zij een altijd-actieve vorm van STAT5A terugbrachten in deficiente cellen, verhoogde dat grotendeels genen die ook bereikbaar waren voor STAT5B, wat suggereert dat echte STAT5A-only doelen zeldzaam en relatief zwak zijn. In plaats daarvan ontstonden verschillen uit hoe sterk en in welke situaties STAT5B werkt. Reacties verschilden afhankelijk van welk cytokine signaleerde (IL-7 versus IL-15), of de T-cel naïef of geheugen was, en of deze tot de CD4+- of CD8+-lijn behoorde. IL-15 activeerde bijvoorbeeld bredere door STAT5B gedreven genprogramma’s dan IL-7, vooral in geheugen CD8+ T-cellen.
Een gencanvas om STAT5-activiteit bij ziekte te volgen
Om de essentie van deze route vast te leggen destilleerden de onderzoekers een 85-genen tellend „core STAT5-signatuur” die opviel over verschillende cytokines en CD8+ T-celtoestanden. Wanneer zij deze signatuur projecteerden op single-cell RNA-gegevens van virus-geïnfecteerde muizen, lichtte een duidelijke cluster van vroege effector- of vroeg uitgeputte CD8+ T-cellen op—juist de cellen die sterke, verse cytokinesignalen ervaren. De signatuur was veel minder actief in volledig uitgeputte of rustende cellen, wat suggereert dat het kan dienen als een bioinformatisch baken voor intense STAT5-signalisatie tijdens immuunreacties en mogelijk in kankers die worden aangedreven door aberrante STAT5B-activiteit.
Wat dit betekent voor patiënten en therapieën
Voor niet-specialisten is de kernboodschap dat STAT5A en STAT5B als twee hendels op hetzelfde bedieningspaneel zijn, maar één hendel—STAT5B—is langer en wordt vaker gebruikt. Beide dragen bij aan hoe killer T-cellen overleven, rusten en onthouden, maar STAT5B heeft een uniek sterke invloed op hun aantallen en op kritieke genprogramma’s. Door deze asymmetrie te verduidelijken en door een gengebaseerde signatuur van STAT5-activiteit te bieden, levert de studie een conceptuele kaart voor het ontwerpen van meer precieze immunotherapieën—of het nu gaat om het afstemmen van cytokine-geneesmiddelen, het engineer’n van T-cellen of het interpreteren van patiëntengenoomgegevens—die de kracht van killer T-cellen benutten zonder het immuunsysteem naar ziekte te duwen.
Bronvermelding: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Trefwoorden: STAT5B, CD8 T-cellen, cytokinesignalering, immunotherapie, T-celdifferentiatie