Clear Sky Science · de
Asymmetrie und Redundanz der STAT5-Paraloge in verschiedenen Differenzierungszuständen von CD8+-T-Zellen
Warum das für künftige Immuntherapien wichtig ist
Viele der vielversprechendsten Krebstherapien und Behandlungen bei Autoimmunerkrankungen greifen darauf zurück, die eigenen Immunzellen – vor allem CD8+-„Killer“-T-Zellen – dazu zu bringen, stärker anzugreifen oder sich zurückzuhalten. Ein zentraler molekularer Schalter in diesen Zellen ist das Protein STAT5, das in zwei nahezu identischen Varianten vorkommt. Die Studie stellt eine auf den ersten Blick einfache, aber therapeutisch weitreichende Frage: Sind diese Zwillinge tatsächlich austauschbar, oder übernimmt einer von beiden insgeheim die Hauptrolle?
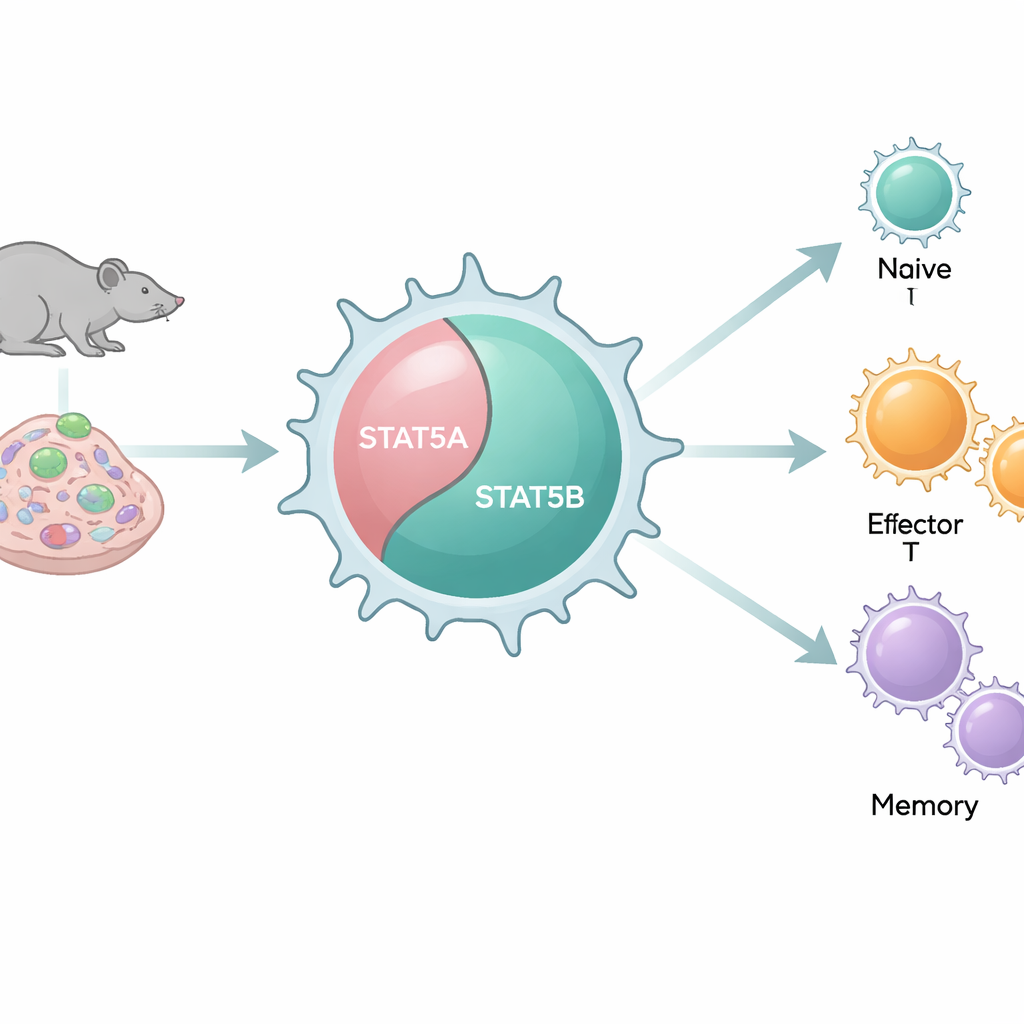
Zwei ähnliche Schalter mit unterschiedlichem Verhalten
Unser Genom enthält zwei eng verwandte Kopien, sogenannte Paraloge, von STAT5: STAT5A und STAT5B. Da sie molekular sehr ähnlich sind und viele der gleichen DNA-Abschnitte binden, galten sie häufig als redundante Bausteine. Patient:innen mit schädigenden STAT5B-Mutationen entwickeln jedoch schwere Immunstörungen, während vergleichbare Defekte in STAT5A selten sind. Mithilfe verschiedener Mausmodelle, die systematisch STAT5A, STAT5B oder beide in unterschiedlichen Kombinationen entfernen, untersuchen die Autor:innen, wie jeder Paraloge die Anzahl und das Verhalten von CD8+-T-Zellen in lebenden Organismen und in Zellen beeinflusst.
Zentrale Rolle von STAT5B für das Gleichgewicht der Killer-T-Zellen
Wurden die gesamten STAT5-Werte reduziert, gingen die CD8+-T-Zellen in Lymphknoten, Milz und Knochenmark stark zurück, was zu verschobenen Verhältnissen von Helfer- (CD4+) zu Killer- (CD8+) T-Zellen führte. Gemischte Knochenmarkstransplantationen zeigten, dass dies größtenteils an einem Problem innerhalb der T-Zellen selbst liegt und nicht nur an Veränderungen ihrer Umgebung. Der Verlust war am gravierendsten, wenn STAT5B fehlte; Mäuse, die nur eine Kopie von STAT5A hatten, schnitten am schlechtesten ab. Gleichzeitig wandelten sich die verbleibenden CD8+-T-Zellen von einem ruhenden, naiven Zustand hin zu erfahreneren Effektor- und Gedächtniszellen, konnten sich paradox jedoch nicht vollständig mit wichtigen Effektormolekülen wie bestimmten Enzymen und Rezeptoren ausrüsten. Das zeigt STAT5 als Wächter sowohl der Anzahl als auch der Qualität von Killer-T-Zellen, wobei STAT5B das größte Gewicht trägt.
Ungleiche Partner im Inneren
Beim genaueren Hinsehen maßen die Forschenden, wie viel von jedem Paralogen vorhanden ist und wie Gene reagieren, wenn einer von beiden fehlt. In CD8+-T-Zellen machte STAT5B etwa zwei Drittel des gesamten STAT5-Proteins und der zugehörigen Boten-RNA aus. Der Verlust von STAT5B verringerte die Aktivierung des zentralen Phosphorylierungs-Schritts der Signalkaskade stärker als der Verlust von STAT5A. Als die Forschenden RNA aus naiven, Effektor- und Gedächtnis-CD8+-T-Zellen sequenzierten, die durch die Zytokine IL-7 und IL-15 stimuliert wurden, fanden sie deutlich mehr fehlregulierte Gene bei Abwesenheit von STAT5B als bei fehlendem STAT5A. Viele dieser Gene steuern Überleben, Stoffwechsel und Gedächtnisbildung, was STAT5B als Haupttreiber zytokinvermittelter Antworten in Killer-T-Zellen unterstreicht.
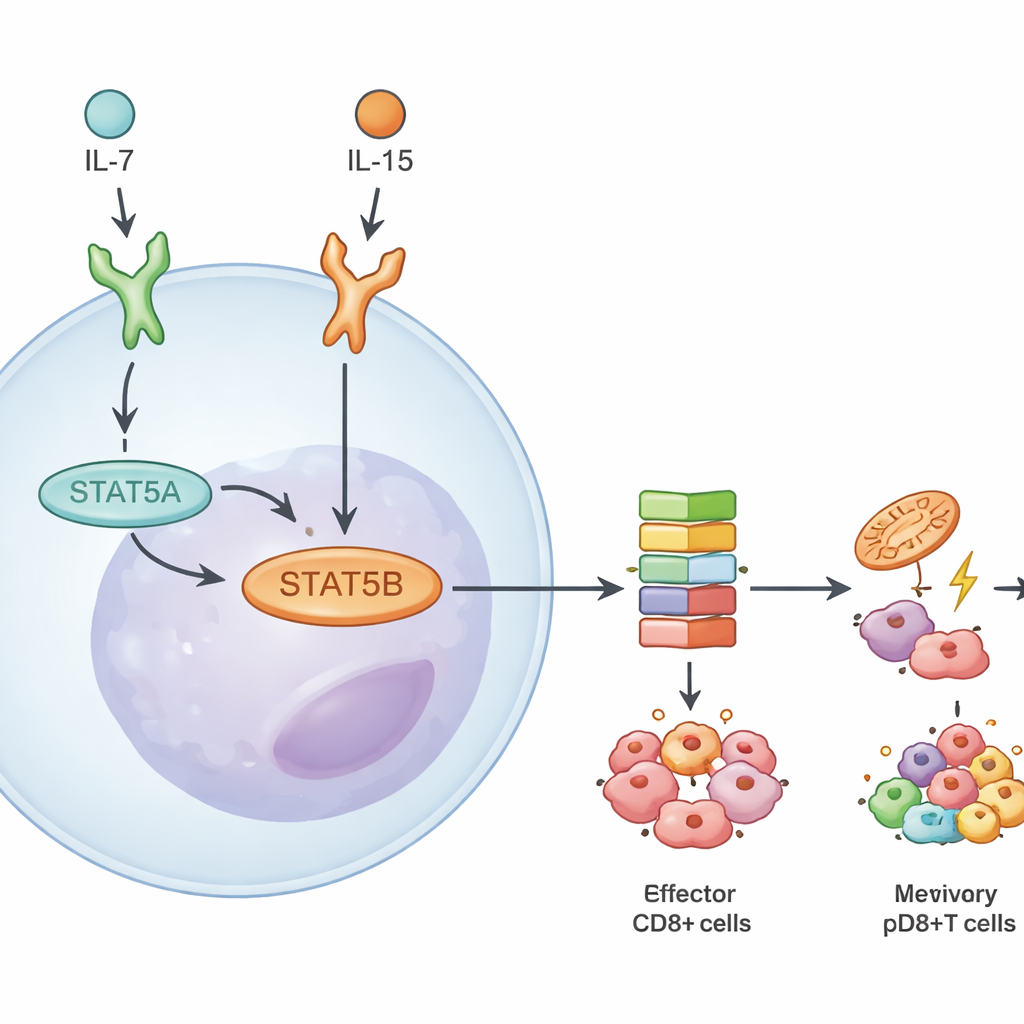
Gemeinsame DNA-Ziele, aber kontextspezifisches Wirken
Trotz der Dominanz von STAT5B besetzten die beiden Paraloge viele der gleichen genomischen Regionen. Mithilfe von Bindungskarten stellten die Autor:innen fest, dass die meisten hochwirksamen DNA-Stellen sowohl von STAT5A als auch von STAT5B gebunden wurden. Als sie eine dauerhaft aktive Form von STAT5A in defiziente Zellen zurückbrachten, hob dies größtenteils Gene an, die ebenfalls von STAT5B erreichbar waren, was darauf hindeutet, dass echte STAT5A-exklusive Zielgene selten und relativ schwach sind. Unterschiede ergaben sich stattdessen daraus, wie stark und in welchen Situationen STAT5B wirkt. Die Antworten variierten je nach dem auslösenden Zytokin (IL-7 versus IL-15), dem Zustand der T-Zelle (naiv oder Gedächtnis) und der Zugehörigkeit zur CD4+- oder CD8+-Linie. IL-15 zum Beispiel löste breitere, von STAT5B getriebene Genprogramme aus als IL-7, insbesondere in Gedächtnis-CD8+-T-Zellen.
Ein Gen-Signatur, um STAT5-Aktivität bei Erkrankungen zu verfolgen
Um das Wesentliche dieses Signalwegs zu erfassen, erarbeiteten die Forschenden eine 85-gene umfassende „Kern-STAT5-Signatur“, die bei verschiedenen Zytokinen und CD8+-T-Zell-Zuständen auftrat. Legten sie diese Signatur auf Einzelzell-RNA-Daten von virusinfizierten Mäusen, leuchtete ein ausgeprägter Cluster früher Effektor- oder früh erschöpfter CD8+-T-Zellen auf — genau die Zellen, die eine starke, frische Zytokin-Stimulation erfahren. Die Signatur war bei vollständig erschöpften oder ruhenden Zellen deutlich weniger aktiv, was darauf hindeutet, dass sie als bioinformatischer Leuchtturm für intensive STAT5-Signalgebung während Immunantworten und möglicherweise bei Krebserkrankungen mit aberranter STAT5B-Aktivität dienen kann.
Was das für Patient:innen und Therapien bedeutet
Für Nichtfachleute lautet die Kernaussage: STAT5A und STAT5B sind wie zwei Hebel am selben Bedienpult, aber ein Hebel, STAT5B, ist länger und wird häufiger gezogen. Beide beeinflussen, wie Killer-T-Zellen überleben, ruhen und Gedächtnis bilden, doch STAT5B hat einen einzigartig starken Einfluss auf ihre Zahl und auf kritische Genprogramme. Indem die Studie diese Asymmetrie klärt und eine genbasierte Signatur der STAT5-Aktivität liefert, bietet sie eine konzeptionelle Landkarte für die Entwicklung präziserer Immuntherapien — sei es durch Feinabstimmung von Zytokinwirkstoffen, durch gentechnische Gestaltung von T-Zellen oder bei der Interpretation genomischer Patient:innendaten — die die Kraft der Killer-T-Zellen nutzen, ohne das Immunsystem in Krankheit zu kippen.
Zitation: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Schlüsselwörter: STAT5B, CD8 T-Zellen, Zytokin-Signalgebung, Immuntherapie, T-Zell-Differenzierung