Clear Sky Science · it
Asimmetria e ridondanza dei paraloghi STAT5 negli stati di differenziamento dei linfociti T CD8+
Perché è importante per le future terapie immunitarie
Molti dei trattamenti più promettenti contro il cancro e le malattie autoimmuni agiscono modulando le nostre cellule immunitarie, in particolare i linfociti T CD8+ “killer”, per farle combattere di più o attenuarne l’attività. Un interruttore molecolare chiave in queste cellule è una proteina chiamata STAT5, che in realtà è presente in due versioni quasi gemelle. Questo studio pone una domanda apparentemente semplice ma con grandi implicazioni terapeutiche: questi gemelli sono davvero intercambiabili o uno di loro dirige silenziosamente l’azione?
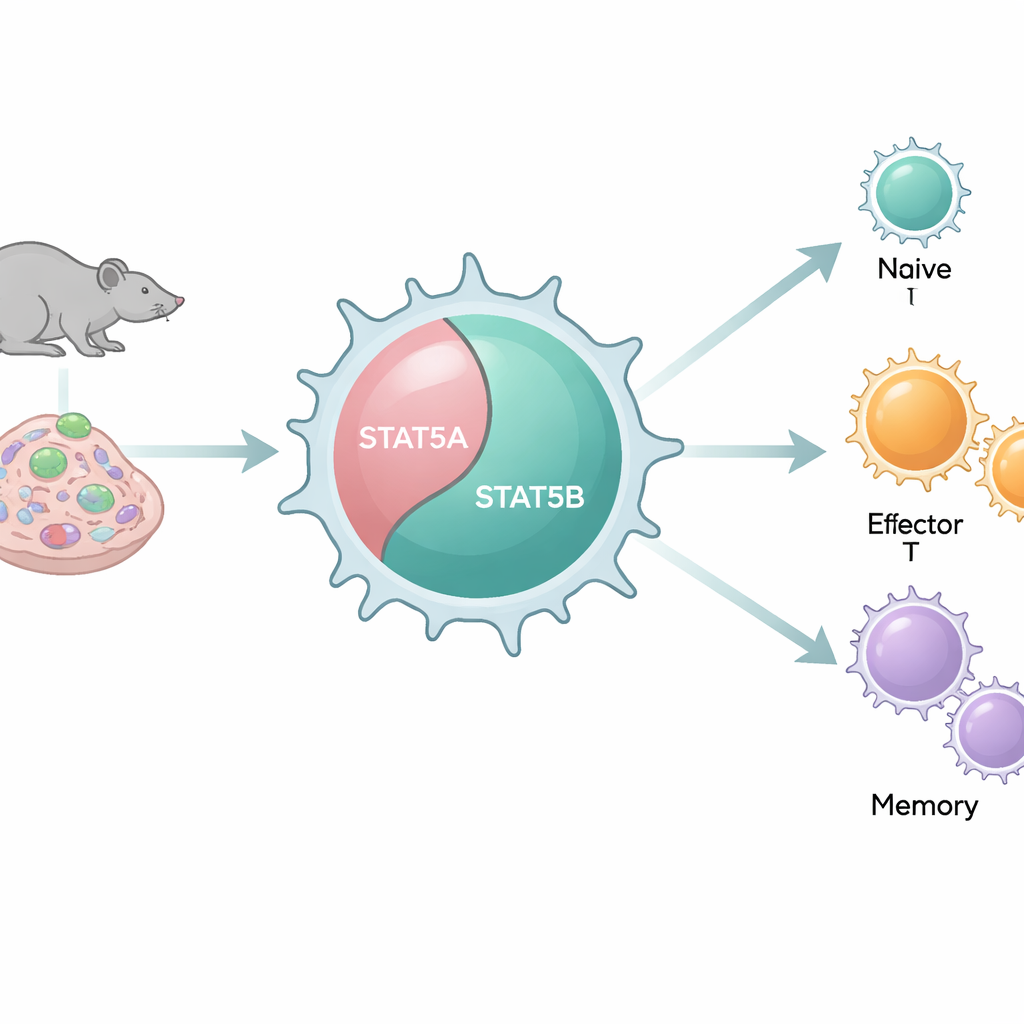
Due interruttori simili che si comportano in modo diverso
I nostri genomi contengono due copie strettamente correlate, o paraloghi, di STAT5: STAT5A e STAT5B. Poiché assomigliano molto a livello molecolare e si legano a molte delle stesse sequenze di DNA, sono spesso stati considerati parti ridondanti. Tuttavia i pazienti con mutazioni dannose in STAT5B sviluppano gravi problemi immunitari, mentre difetti comparabili in STAT5A sono rari. Usando una serie di modelli murini che rimuovono sistematicamente STAT5A, STAT5B o entrambi in varie combinazioni, gli autori hanno investigato come ciascun paralogo influenzi il numero e il comportamento dei linfociti T CD8+ negli organismi viventi e nelle cellule.
Ruolo chiave di STAT5B nel mantenere l’equilibrio dei linfociti killer
Quando i livelli totali di STAT5 venivano ridotti, i linfociti T CD8+ calavano drasticamente nei linfonodi, nella milza e nel midollo osseo, portando a rapporti sbilanciati tra cellule helper (CD4+) e killer (CD8+). Trapianti di midollo osseo misti hanno dimostrato che ciò è dovuto in gran parte a un problema intrinseco alle cellule T stesse, non solo a cambiamenti del loro ambiente. La perdita era più grave quando mancava STAT5B, e i topi che potevano contare su una sola copia di STAT5A mostravano i peggiori risultati. Allo stesso tempo, i rimanenti linfociti T CD8+ si spostavano da uno stato riposato e naive verso stati più esperti di effettori e memoria, ma paradossalmente non riuscivano a dotarsi pienamente degli strumenti chiave per uccidere, come specifici enzimi e recettori. Questo rivela STAT5 come custode sia del numero sia della qualità dei linfociti killer, con STAT5B che porta il peso maggiore.
Partner diseguali sotto il cofano
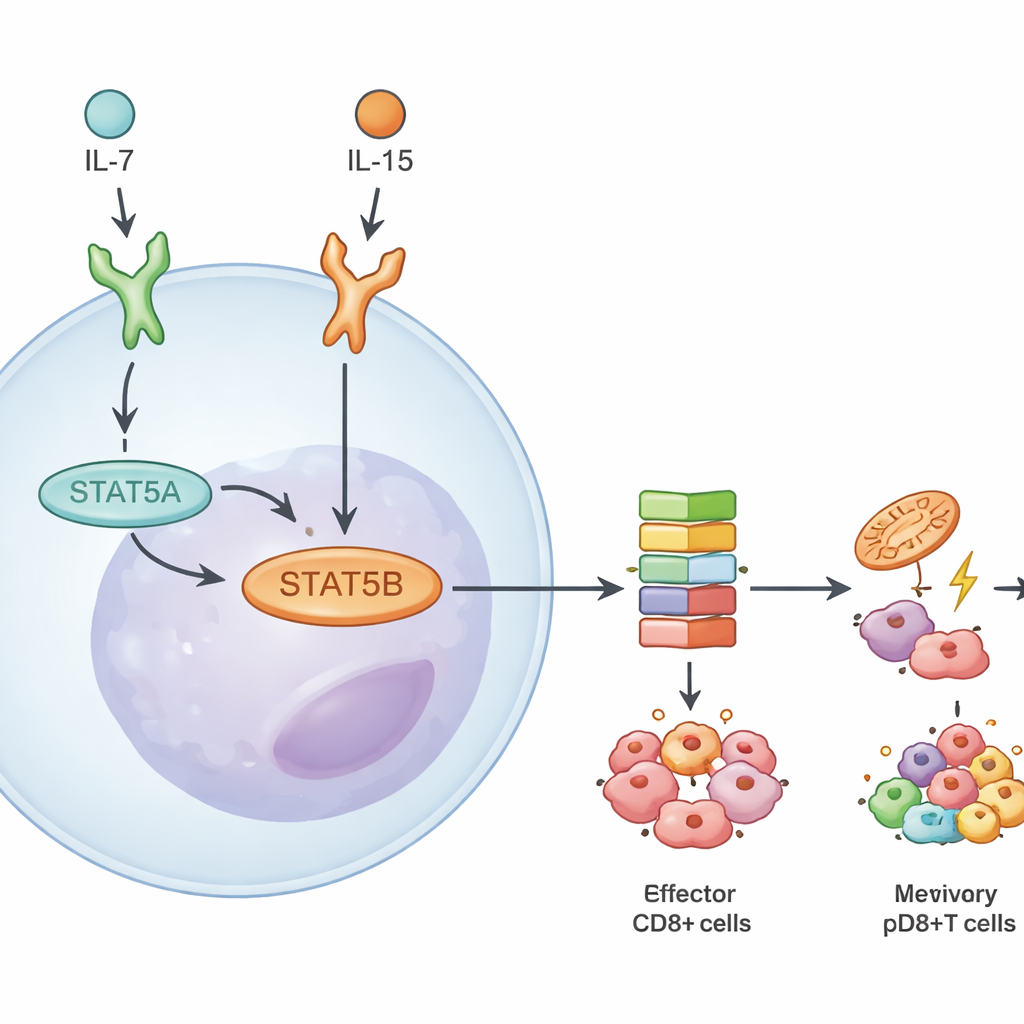
Approfondendo, il gruppo ha misurato quanto di ciascun paralogo è presente e come rispondono i geni quando uno dei due manca. Nei linfociti T CD8+ STAT5B costituiva circa due terzi della proteina e del trascritto STAT5 totali. La perdita di STAT5B riduceva l’attivazione del passaggio chiave di fosforilazione della via più della perdita di STAT5A. Quando i ricercatori hanno sequenziato l’RNA di cellule CD8+ naive, effettrici e di memoria stimolate da due citochine, IL-7 e IL-15, hanno trovato molti più geni deregolarizzati in assenza di STAT5B rispetto a quando mancava solo STAT5A. Molti di questi geni controllano la sopravvivenza, il metabolismo e la formazione della memoria, sottolineando STAT5B come il principale motore delle risposte alle citochine nei linfociti killer.
Stessi target nel DNA ma azioni specifiche al contesto
Nonostante il predominio di STAT5B, i due paraloghi occupavano in gran parte le stesse aree del genoma. Tramite mappe di legame, gli autori hanno osservato che la maggior parte dei siti di DNA a impatto elevato era legata sia da STAT5A sia da STAT5B. Quando hanno reintrodotto una forma costitutivamente attiva di STAT5A in cellule carenti, questa aumentava in larga misura i geni raggiungibili anche da STAT5B, suggerendo che veri e propri target esclusivi di STAT5A sono rari e relativamente deboli. Le differenze emergevano invece da quanto intensamente e in quali situazioni STAT5B agisce. Le risposte variavano a seconda della citochina che segnalava (IL-7 vs IL-15), se la cellula T era naive o di memoria e se apparteneva alla linea CD4+ o CD8+. Per esempio, l’IL-15 attivava programmi genici più ampi guidati da STAT5B rispetto all’IL-7, specialmente nelle cellule T CD8+ di memoria.
Una firma genica per tracciare l’attività di STAT5 nelle malattie
Per catturare l’essenza di questa via, gli investigatori hanno distillato una “firma STAT5 core” di 85 geni che compariva attraverso diverse citochine e stati dei linfociti T CD8+. Sovrapponendo questa firma a dati di RNA a singola cellula provenienti da topi infettati da virus, essa ha evidenziato un cluster distinto di CD8+ precoci effettrici o precocemente esauste, le cellule che stavano sperimentando una forte e recente stimolazione da citochine. La firma risultava molto meno attiva in cellule pienamente esauste o riposate, suggerendo che può agire come un faro bioinformatico per intensa segnalazione STAT5 durante le risposte immunitarie e forse nei tumori guidati da attività aberrante di STAT5B.
Cosa significa questo per i pazienti e le terapie
Per un non specialista, il messaggio principale è che STAT5A e STAT5B sono come due leve sullo stesso pannello di controllo, ma una leva, STAT5B, è più lunga e viene tirata più spesso. Entrambe contribuiscono a come i linfociti killer sopravvivono, riposano e ricordano, tuttavia STAT5B ha un’influenza particolarmente forte sui loro numeri e sui programmi genici critici. Chiarendo questa asimmetria e fornendo una firma genica dell’attività STAT5, lo studio offre una mappa concettuale per progettare immunoterapie più precise — sia modulando farmaci a base di citochine, sia ingegnerizzando cellule T, sia interpretando dati genomici dei pazienti — che sfruttino la potenza dei linfociti killer senza sbilanciare il sistema immunitario verso la malattia.
Citazione: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Parole chiave: STAT5B, Linfociti T CD8, segnalazione da citochine, immunoterapia, differenziamento delle cellule T