Clear Sky Science · sv
Asymmetri och redundans hos STAT5-paraloger i olika differentieringsstadier av CD8+-T‑celler
Varför detta är viktigt för framtida immunoterapier
Många av dagens mest lovande behandlingar mot cancer och autoimmuna sjukdomar verkar genom att påverka våra egna immunceller, i synnerhet CD8+-“mördare” T‑celler, så att de antingen aktiveras hårdare eller dämpas. En viktig molekylär brytare i dessa celler är proteinet STAT5, som i praktiken finns i två nästan identiska varianter. Denna studie ställer en förenklat formulerad men terapeutiskt viktig fråga: är dessa tvillingar verkligen utbytbara, eller styr den ena i praktiken mest?
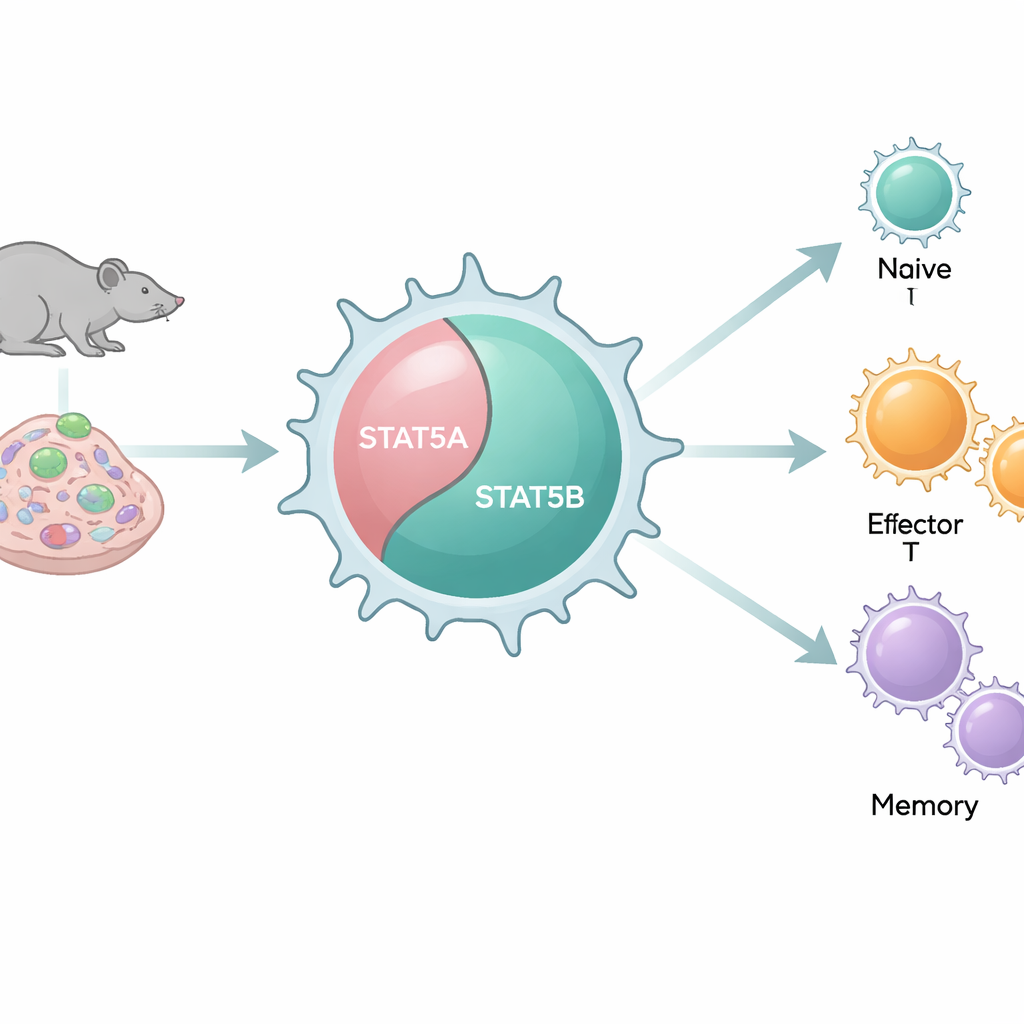
Två lika brytare som beter sig olika
Våra genom innehåller två nära besläktade kopior, eller paraloger, av STAT5: STAT5A och STAT5B. Eftersom de är så lika på molekylnivå och binder många av samma DNA‑sekvenser har de ofta behandlats som redundanta komponenter. Men patienter med allvarliga STAT5B‑mutationer utvecklar tydliga immunproblem, medan motsvarande defekter i STAT5A är ovanligare. Med hjälp av flera musmodeller som systematiskt tar bort STAT5A, STAT5B eller båda i olika kombinationer undersöker författarna hur varje paralog påverkar antal och funktion hos CD8+-T‑celler i levande organismer och i celler.
Nyckelroll för STAT5B i att hålla mördande T‑celler i balans
När det totala STAT5‑nivåerna sänktes sjönk antalet CD8+-T‑celler kraftigt i lymfkörtlar, mjälte och benmärg, vilket ledde till skeva förhållanden mellan hjälpar‑ (CD4+) och mördande (CD8+) T‑celler. Blandade benmärgstransplantationer visade att detta till stor del beror på ett problem inne i T‑cellerna själva, inte endast förändringar i deras omgivning. Förlusten var mest uttalad när STAT5B saknades, och möss som bara hade en kopia av STAT5A klarade sig sämst. Samtidigt skiftade de kvarvarande CD8+-T‑cellerna bort från ett vilande, naivt tillstånd mot mer erfarna effektor‑ och minnesstadier, men paradoxalt nog kunde de inte fullt utrusta sig med viktiga mördande funktioner såsom specifika enzymer och receptorer. Detta visar att STAT5 fungerar som en väktare av både antalet och kvaliteten hos mördande T‑celler, där STAT5B bär största tyngden.
Ojämlika partner under huven
Genom att gå djupare mätte teamet hur mycket av varje paralog som finns och hur gener svarar när en av dem saknas. I CD8+-T‑celler utgjorde STAT5B ungefär två tredjedelar av det totala STAT5‑proteinet och budbärar‑RNA:t. Förlust av STAT5B minskade aktiveringen av väggenoms centrala fosforyleringssteg mer än förlust av STAT5A. När forskarna sekvenserade RNA från naiva, effektor‑ och minnes CD8+-T‑celler stimulerade med två cytokiner, IL‑7 och IL‑15, fann de många fler gener som var felreglerade i avsaknad av STAT5B än när endast STAT5A saknades. Många av dessa gener kontrollerar överlevnad, metabolism och minnesbildning, vilket befäster STAT5B som huvuddrivkraften i cytokinsvar hos mördande T‑celler.
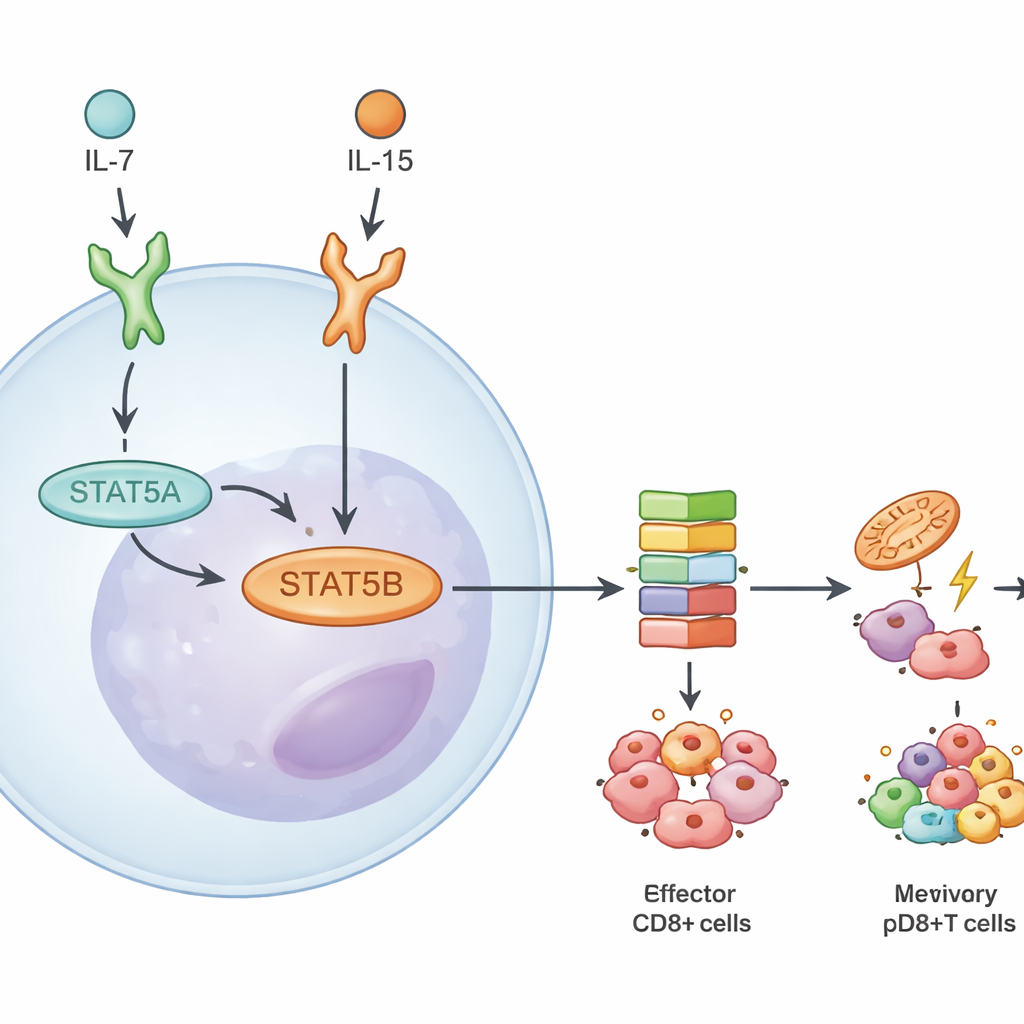
Delade DNA‑mål men situationsspecifika handlingar
Trots STAT5B:s dominans visade sig de två paralogerna ha mycket gemensamt i det genomiska landskapet. Genom bindningskartor såg författarna att de flesta högeffektiva DNA‑platserna var bundna av både STAT5A och STAT5B. När de återinförde en alltid aktiv form av STAT5A i bristfälliga celler ökade det i huvudsak uttrycket av gener som också var åtkomliga för STAT5B, vilket tyder på att verkliga STAT5A‑endast‑mål är sällsynta och relativt svaga. Istället uppstod skillnader i hur starkt och i vilka situationer STAT5B verkar. Svaren varierade beroende på vilken cytokin som signalerade (IL‑7 vs. IL‑15), om T‑cellen var naiv eller minnesbildad, och om den tillhörde CD4+‑ eller CD8+‑linjen. IL‑15 aktiverade till exempel bredare STAT5B‑drivna genprogram än IL‑7, särskilt i minnes CD8+-T‑celler.
En gen‑signatur för att spåra STAT5‑aktivitet vid sjukdom
För att fånga kärnan i denna bana destillerade undersökarna en 85‑geners ‘‘core STAT5‑signature’’ som återkom över olika cytokiner och CD8+-T‑cellsstadier. När de lade denna signatur över en enskildcells‑RNA‑datamängd från virusinfekterade möss tändes en tydlig klusterbildning i tidiga effektor‑ eller tidigt uttömda CD8+-T‑celler — just de celler som upplever stark, färsk cytokinpåverkan. Signaturen var mycket mindre aktiv i fullt uttröttade eller vilande celler, vilket tyder på att den kan fungera som en bioinformatisk fyr för intensiv STAT5‑signalering under immunrespons och möjligen i tumörer drivna av abnorm STAT5B‑aktivitet.
Vad detta betyder för patienter och terapier
För icke‑specialisten är huvudbudskapet att STAT5A och STAT5B fungerar som två spakar på samma kontrollpanel, men en spak, STAT5B, är längre och används oftare. Båda bidrar till hur mördande T‑celler överlever, vilar och bildar minne, men STAT5B har ett särskilt starkt inflytande över deras antal och kritiska genprogram. Genom att klargöra denna asymmetri, och genom att erbjuda en genbaserad signatur för STAT5‑aktivitet, ger studien en konceptuell karta för att utforma mer precisa immunoterapier — vare sig det handlar om att finjustera cytokiner, konstruera T‑celler eller tolka patienters genomdata — som kan utnyttja mördande T‑cellers kraft utan att rubba immunsystemet i skadlig riktning.
Citering: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Nyckelord: STAT5B, CD8 T‑celler, cytokinsignalering, immunoterapi, T‑cellsdifferentiation