Clear Sky Science · ru
Асимметрия и избыточность паралогов STAT5 при различных состояниях дифференцировки CD8+ Т-клеток
Почему это важно для будущих иммунных терапий
Многие из наиболее перспективных сегодня методов лечения рака и аутоиммунных заболеваний действуют, подтягивая или сдерживая собственные иммунные клетки, особенно CD8+ «киллерные» T-клетки. Ключевой молекулярный переключатель в этих клетках — белок STAT5, который на самом деле существует в виде двух почти идентичных версий. В этом исследовании задан простой на первый взгляд, но имеющий большие терапевтические последствия вопрос: действительно ли эти «близнецы» взаимозаменяемы или один из них тихо управляет процессом?
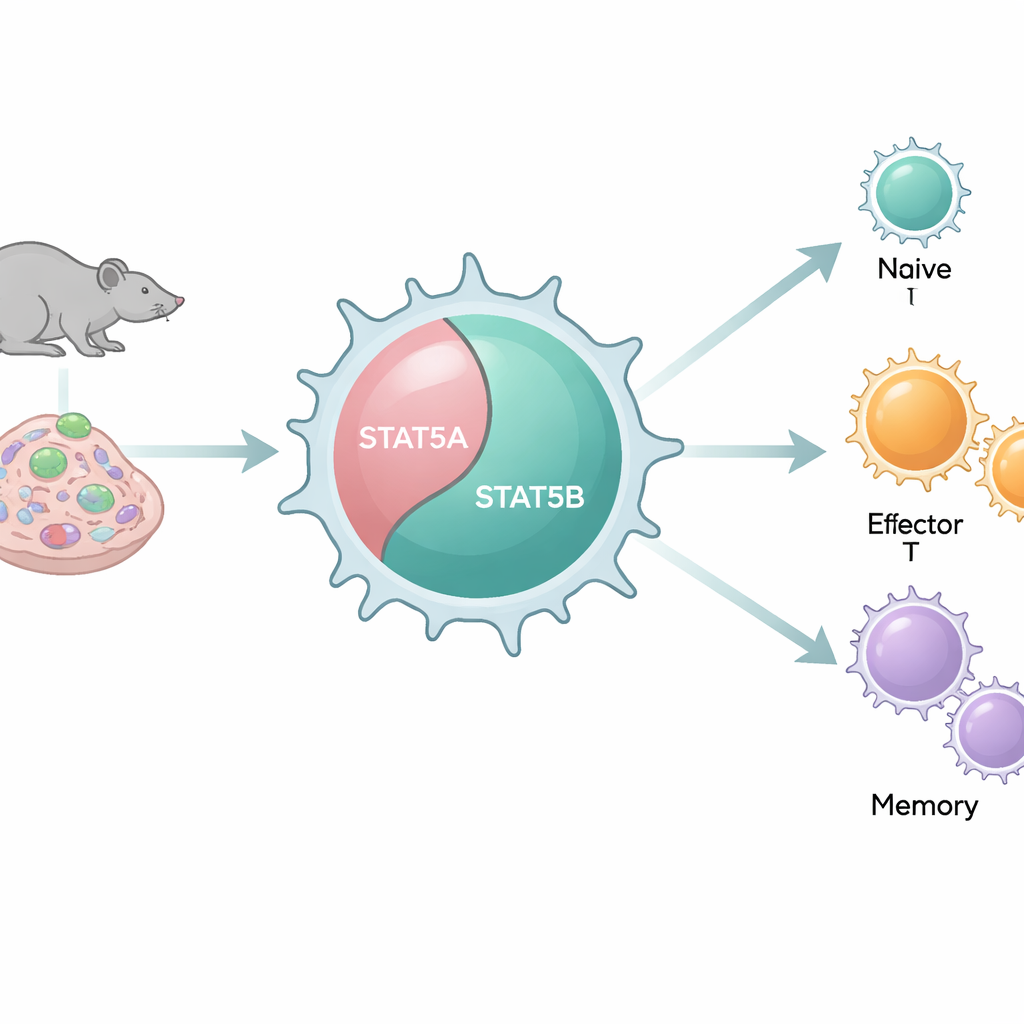
Два похожих переключателя, которые ведут себя по-разному
В нашем геноме есть две тесно родственные копии, или паралога, STAT5: STAT5A и STAT5B. Поскольку они молекулярно очень похожи и связываются со многими одними и теми же участками ДНК, их часто считали избыточными компонентами. Тем не менее у пациентов с повреждающими мутациями STAT5B развиваются серьёзные проблемы с иммунитетом, тогда как сопоставимые дефекты STAT5A встречаются редко. Авторы, используя набор мышиных моделей, в которых систематически удаляют STAT5A, STAT5B или оба паралога в разных сочетаниях, исследуют, как каждый паралог влияет на количество и поведение CD8+ Т-клеток в организме и в клеточных системах.
Ключевая роль STAT5B в поддержании баланса киллерных T-клеток
Когда общий уровень STAT5 был снижен, количество CD8+ Т-клеток резко уменьшилось в лимфатических узлах, селезёнке и костном мозге, что привело к смещению соотношения помощников (CD4+) и киллеров (CD8+). Смешанные трансплантаты костного мозга показали, что это во многом связано с проблемой внутри самих T-клеток, а не только с изменением их окружения. Наибольшая утрата наблюдалась при отсутствии STAT5B, а мыши, опиравшиеся только на одну копию STAT5A, чувствовали себя хуже всего. Вместе с тем оставшиеся CD8+ Т-клетки сместились от состояние покоя, наивных клеток, к более опытным эффекторным и памятьным состояниям, но парадоксально не могли полностью снарядить себя ключевыми «убийственными» инструментами, такими как специфические ферменты и рецепторы. Это показывает STAT5 как хранителя как численности, так и качества киллерных T-клеток, причём STAT5B несёт наибольшую нагрузку.
Неравные партнёры внутри механизма
Углубляя изучение, команда измеряла, сколько каждого паралога присутствует и как реагируют гены при отсутствии каждого из них. В CD8+ Т-клетках STAT5B составлял примерно две трети от общего количества белка и мРНК STAT5. Потеря STAT5B сильнее снижала активацию ключевого фосфорилирования в пути, чем потеря STAT5A. Когда исследователи секвенировали РНК наивных, эффекторных и памятьных CD8+ Т-клеток, стимулированных двумя цитокинами — IL-7 и IL-15, — они обнаружили значительно больше генов с нарушенной регуляцией при отсутствии STAT5B, чем при дефиците только STAT5A. Многие из этих генов контролируют выживание, метаболизм и формирование памяти, что подчёркивает STAT5B как основной драйвер цитокиновых ответов в киллерных T-клетках.
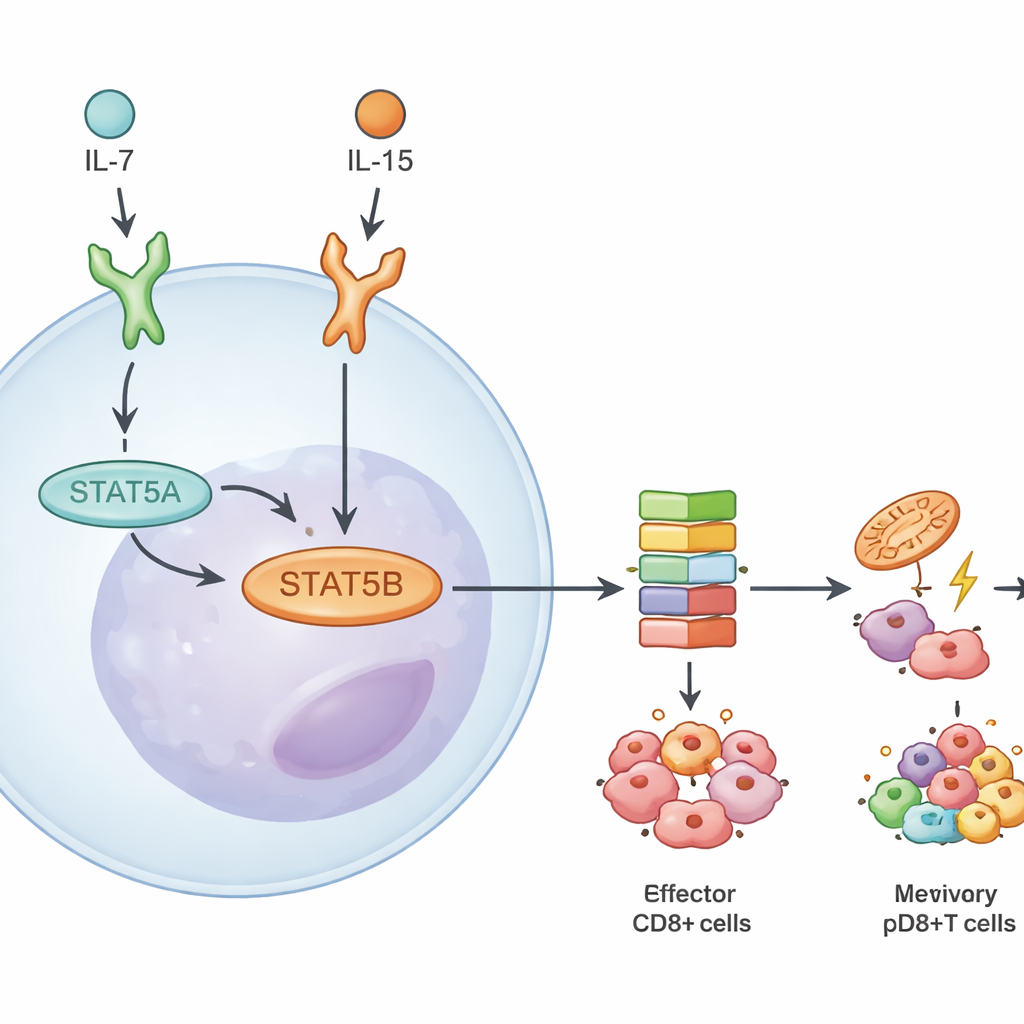
Общие ДНК-мишени, но контекст-зависимые действия
Несмотря на доминирование STAT5B, оказалось, что оба паралога занимают большую часть одинаковой геномной территории. По картам связывания авторы увидели, что большинство высокоэффективных участков ДНК связываются и STAT5A, и STAT5B. Когда они повторно вводили постоянно активную форму STAT5A в дефицитные клетки, это в значительной степени усиливало те же гены, к которым имел доступ и STAT5B, что указывает на то, что истинные мишени, доступные только STAT5A, редки и относительно слабые. Вместо этого различия возникали из того, насколько сильно и в каких ситуациях действует STAT5B. Ответы варьировались в зависимости от того, какой цитокин сигнализировал (IL-7 vs. IL-15), находилась ли T-клетка в наивном или памятьном состоянии и к какому типу — CD4+ или CD8+ — она принадлежала. Например, IL-15 запускал более широкие программы генов, управляемые STAT5B, чем IL-7, особенно в памятьных CD8+ Т-клетках.
Генетический отпечаток для отслеживания активности STAT5 в заболеваниях
Чтобы охарактеризовать суть этого сигнального пути, исследователи выделили 85-генный «основной сигнатурный набор STAT5», который проявлялся при разных цитокинах и состояниях CD8+ Т-клеток. Когда они наложили эту сигнатуру на данные одиночных клеток РНК-секвенирования от инфицированных вирусом мышей, она подсветила отдельный кластер ранних эффекторных или ранне истощённых CD8+ Т-клеток — те самые клетки, которые испытывают сильную свежую цитокиновую стимуляцию. Сигнатура была значительно менее активна в полностью истощённых или покоящихся клетках, что говорит о том, что она может служить биоинформатическим маяком интенсивной STAT5-сигнализации во время иммунных ответов и, возможно, в раках, вызванных аномальной активностью STAT5B.
Что это означает для пациентов и лечения
Для неспециалиста ключевая мысль такова: STAT5A и STAT5B — это как два рычага на одной панели управления, но один рычаг, STAT5B, длиннее и тянется чаще. Оба влияют на выживание, состояние покоя и память киллерных T-клеток, но STAT5B оказывает уникально сильное влияние на их численность и ключевые генетические программы. Прояснив эту асимметрию и предложив генную сигнатуру активности STAT5, исследование даёт концептуальную карту для разработки более точных иммунотерапий — будь то настройка цитокиновых препаратов, инженерия T-клеток или интерпретация геномных данных пациентов — которые используют силу киллерных T-клеток, не нарушая баланс иммунной системы и не приводя к заболеваниям.
Цитирование: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Ключевые слова: STAT5B, CD8 T cells, цитокиновая сигнализация, иммунотерапия, дифференцировка T-клеток