Clear Sky Science · fr
Asymétrie et redondance des paralogues STAT5 au cours des états de différenciation des lymphocytes T CD8+
Pourquoi cela importe pour les thérapies immunitaires à venir
De nombreux traitements anticancéreux et contre les maladies auto-immunes les plus prometteurs d’aujourd’hui agissent en modulant nos propres cellules immunitaires, en particulier les lymphocytes T CD8+ « cytotoxiques », pour les rendre plus actifs ou les calmer. Un interrupteur moléculaire clé dans ces cellules est une protéine nommée STAT5, qui existe en réalité en deux versions presque jumelles. Cette étude pose une question apparemment simple mais aux grandes implications thérapeutiques : ces deux jumeaux sont-ils vraiment interchangeables, ou l’un d’eux pilote-t-il discrètement la réponse ?
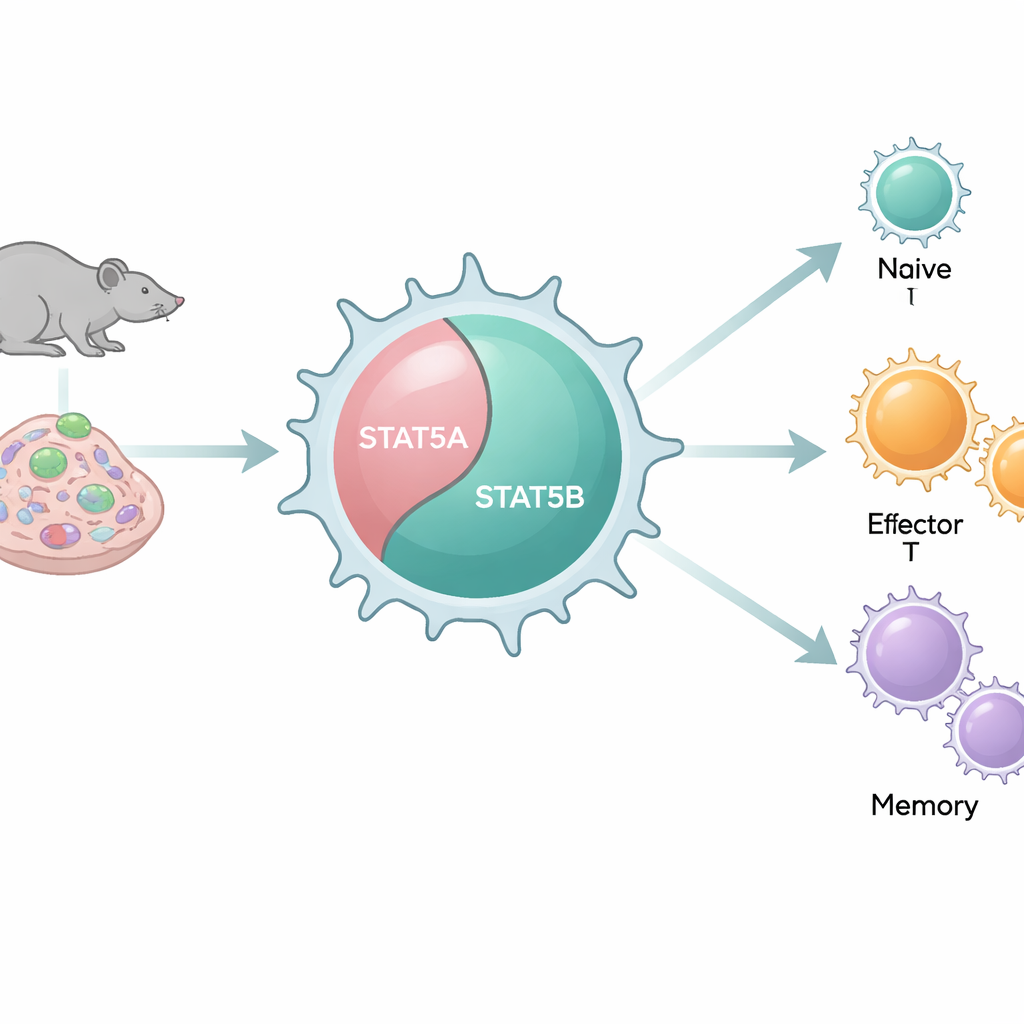
Deux interrupteurs similaires, mais au comportement distinct
Notre génome porte deux copies étroitement apparentées, ou paralogues, de STAT5 : STAT5A et STAT5B. Parce qu’elles se ressemblent beaucoup au niveau moléculaire et se lient à de larges régions d’ADN communes, elles ont souvent été traitées comme des éléments redondants. Pourtant, des patients porteurs de mutations délétères de STAT5B développent des troubles immunitaires graves, alors que des défauts comparables de STAT5A sont rares. En utilisant une batterie de modèles murins supprimant systématiquement STAT5A, STAT5B ou les deux selon différentes combinaisons, les auteurs examinent comment chaque paralogue façonne en conditions in vivo et ex vivo le nombre et le comportement des lymphocytes T CD8+.
Rôle clé de STAT5B dans le maintien de l’équilibre des lymphocytes cytotoxiques
Lorsque le niveau total de STAT5 a été réduit, les lymphocytes T CD8+ ont fortement diminué dans les ganglions lymphatiques, la rate et la moelle osseuse, entraînant des rapports déséquilibrés entre lymphocytes T auxiliaires (CD4+) et cytotoxiques (CD8+). Des greffes médullaires mixtes ont montré que ce phénomène tient principalement à un défaut intrinsèque aux cellules T elles-mêmes, et non seulement à des modifications de leur environnement. La perte était la plus sévère en l’absence de STAT5B, et les souris ne disposant que d’une copie unique de STAT5A étaient les plus affectées. Parallèlement, les CD8+ restants ont basculé d’un état naïf au repos vers des états effecteurs et mémoires plus expérimentés, mais paradoxalement n’ont pas pu s’équiper complètement d’outils cytotoxiques essentiels comme certaines enzymes et récepteurs. Cela révèle STAT5 comme un gardien à la fois du nombre et de la qualité des lymphocytes cytotoxiques, STAT5B portant le poids le plus important.
Partenaires inégaux sous le capot
En approfondissant, l’équipe a mesuré la quantité de chaque paralogue présente et la réponse des gènes quand l’un ou l’autre manque. Dans les lymphocytes T CD8+, STAT5B représentait environ les deux tiers de la protéine et des transcrits totaux de STAT5. La perte de STAT5B réduisait l’activation de l’étape clé de phosphorylation de la voie plus fortement que la perte de STAT5A. Lorsque les chercheurs ont séquencé l’ARN de cellules CD8+ naïves, effectrices et mémoires stimulées par deux cytokines, IL-7 et IL-15, ils ont trouvé bien plus de gènes déréglés en l’absence de STAT5B que lorsque seul STAT5A manquait. Nombre de ces gènes contrôlent la survie, le métabolisme et la formation de la mémoire, ce qui souligne STAT5B comme le principal moteur des réponses aux cytokines dans les lymphocytes cytotoxiques.
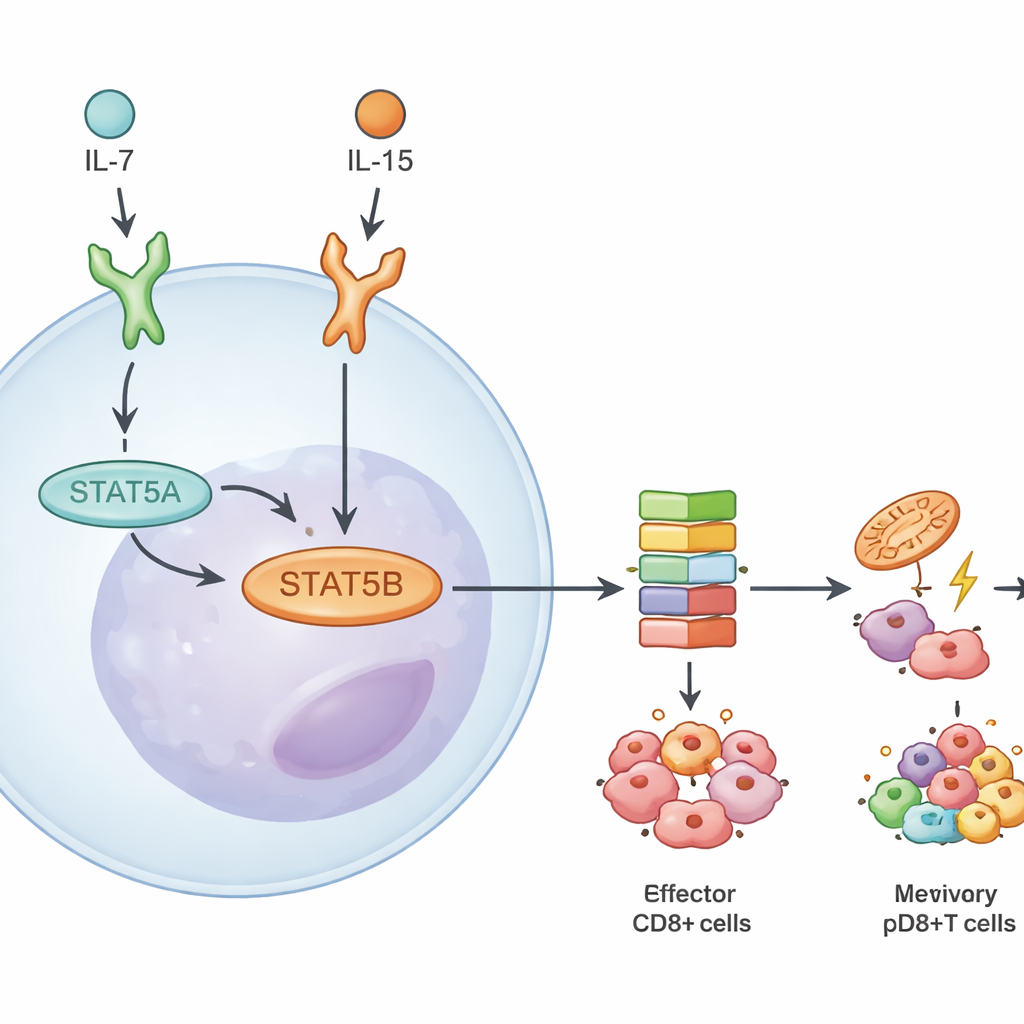
Cibles d’ADN partagées mais actions dépendantes du contexte
Malgré la dominance de STAT5B, les deux paralogues occupent en grande partie le même territoire génomique. À partir de cartes de liaison, les auteurs ont observé que la plupart des sites d’ADN à fort impact étaient liés à la fois par STAT5A et STAT5B. Quand ils ont réintroduit une forme constitutivement active de STAT5A dans des cellules déficientes, cela a principalement réactivé des gènes également accessibles à STAT5B, suggérant que de véritables cibles exclusivement STAT5A sont rares et relativement faibles. Les différences tiennent plutôt à l’intensité et aux circonstances d’action de STAT5B. Les réponses variaient selon la cytokine signalante (IL-7 vs IL-15), l’état de la cellule T (naïve ou mémoire) et l’appartenance à la lignée CD4+ ou CD8+. Par exemple, l’IL-15 déclenchait des programmes géniques plus larges pilotés par STAT5B que l’IL-7, notamment dans les cellules T CD8+ mémoires.
Une signature génique pour suivre l’activité de STAT5 en pathologie
Pour saisir l’essentiel de cette voie, les chercheurs ont distillé une « signature STAT5 fondamentale » de 85 gènes qui se retrouvait à travers différentes cytokines et états des lymphocytes T CD8+. Lorsqu’ils ont superposé cette signature à des données d’ARN monocellulaire provenant de souris infectées par un virus, elle a illuminé un groupe distinct de CD8+ effecteurs précoces ou d’exhaustion précoce — précisément les cellules recevant une stimulation cytokine fraîche et prononcée. La signature était beaucoup moins active dans les cellules pleinement excédées ou au repos, suggérant qu’elle peut servir de balise bioinformatique pour une signalisation STAT5 intense au cours des réponses immunitaires et peut‑être dans des cancers entraînés par une activité anormale de STAT5B.
Ce que cela signifie pour les patients et les traitements
Pour un non-spécialiste, la conclusion est que STAT5A et STAT5B sont comme deux leviers sur un même panneau de commande, mais qu’un levier, STAT5B, est plus long et actionné plus souvent. Les deux contribuent à la survie, au repos et à la mémoire des lymphocytes cytotoxiques, pourtant STAT5B exerce une influence particulièrement forte sur leurs effectifs et sur des programmes géniques critiques. En clarifiant cette asymétrie, et en proposant une signature génique de l’activité STAT5, l’étude fournit une carte conceptuelle pour concevoir des immunothérapies plus précises — que ce soit en modulant des médicaments cytokiniques, en ingénierie de cellules T ou en interprétant des données génomiques de patients — afin d’exploiter la puissance des lymphocytes cytotoxiques sans basculer le système immunitaire vers la maladie.
Citation: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Mots-clés: STAT5B, lymphocytes T CD8, signalisation par les cytokines, immunothérapie, différenciation des cellules T