Clear Sky Science · pl
Asymetria i redundancja paralogów STAT5 w różnych stanach różnicowania limfocytów CD8+
Dlaczego to ma znaczenie dla przyszłych terapii immunologicznych
Wiele z dziś najbardziej obiecujących terapii przeciwnowotworowych i przeciwautoimmunologicznych działa poprzez modulację własnych komórek układu odpornościowego — w szczególności „zabójczych” limfocytów T CD8+, zachęcając je do silniejszej reakcji lub do stłumienia aktywności. Kluczowym molekularnym przełącznikiem w tych komórkach jest białko o nazwie STAT5, które występuje w dwóch niemal bliźniaczych wersjach. W badaniu postawiono pozornie proste pytanie o dużych implikacjach terapeutycznych: czy te bliźniaki są rzeczywiście zamienne, czy też jeden z nich w praktyce rozdaje karty?
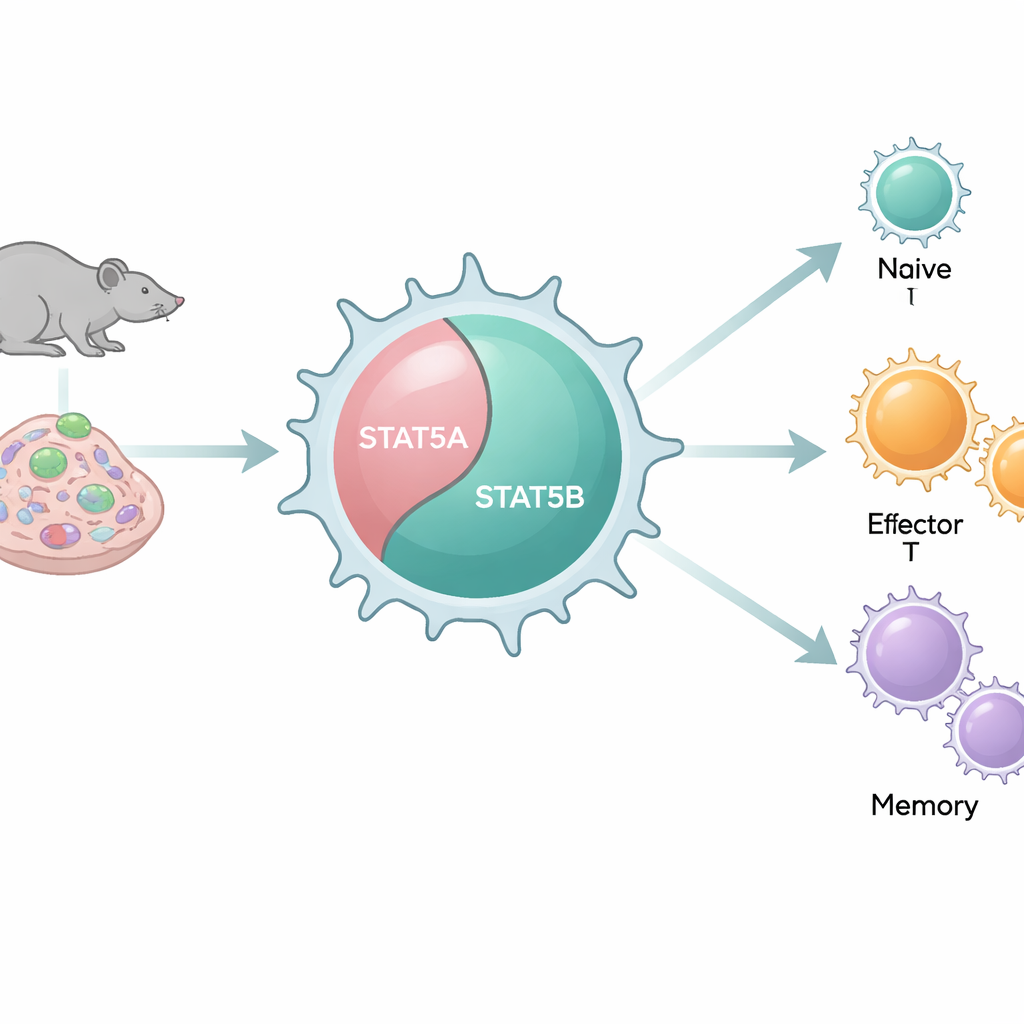
Dwa podobne przełączniki, które zachowują się inaczej
W naszym genomie znajdują się dwa blisko spokrewnione kopie, czyli paralogi, STAT5: STAT5A i STAT5B. Ponieważ są bardzo podobne na poziomie molekularnym i wiążą wiele tych samych odcinków DNA, często traktowano je jako części redundantne. Jednak pacjenci z uszkadzającymi mutacjami w STAT5B rozwijają poważne zaburzenia immunologiczne, podczas gdy porównywalne defekty STAT5A występują rzadko. Wykorzystując serię modeli mysich, które systematycznie usuwają STAT5A, STAT5B lub oba w różnych kombinacjach, autorzy badania analizują, jak każdy paralog kształtuje liczbę i zachowanie limfocytów CD8+ zarówno in vivo, jak i in vitro.
Kluczowa rola STAT5B w utrzymaniu równowagi komórek zabójczych
Gdy całkowity poziom STAT5 został zmniejszony, liczba limfocytów CD8+ spadła gwałtownie w węzłach chłonnych, śledzionie i szpiku kostnym, prowadząc do zaburzenia proporcji limfocytów pomocniczych (CD4+) do zabójczych (CD8+). Przeszczepy mieszanej szpiku kostnego wykazały, że jest to w dużej mierze problem wewnątrz samych komórek T, a nie tylko zmiana środowiska. Ubytek był najsilniejszy przy braku STAT5B, a myszy opierające się tylko na jednej kopii STAT5A radziły sobie najmniej dobrze. Równocześnie pozostałe limfocyty CD8+ przesunęły się z stanu spoczynkowego, naiwnych, w stronę doświadczonych stanów efektorowych i pamięciowych, ale paradoksalnie nie były w stanie w pełni uzbroić się w kluczowe narzędzia zabójcze, takie jak określone enzymy i receptory. To ujawnia STAT5 jako strażnika zarówno liczby, jak i jakości komórek zabójczych, przy czym STAT5B ma największe znaczenie.
Nierówni partnerzy pod maską
Badając to głębiej, zespół zmierzył, ile każdego paralogu jest obecne i jak zmienia się ekspresja genów przy braku jednego z nich. W limfocytach CD8+ STAT5B stanowił około dwóch trzecich całkowitego białka i transkryptu STAT5. Utrata STAT5B bardziej osłabiła aktywację kluczowego etapu fosforylacji w tej ścieżce niż utrata STAT5A. Gdy naukowcy sekwencjonowali RNA z naiwnych, efektorowych i pamięciowych limfocytów CD8+ stymulowanych dwoma cytokinami, IL-7 i IL-15, znaleźli znacznie więcej genów z nieprawidłową regulacją przy braku STAT5B niż przy braku jedynie STAT5A. Wiele z tych genów kontroluje przeżycie, metabolizm i tworzenie pamięci, co podkreśla rolę STAT5B jako głównego kierowcy odpowiedzi na cytokiny w komórkach zabójczych.
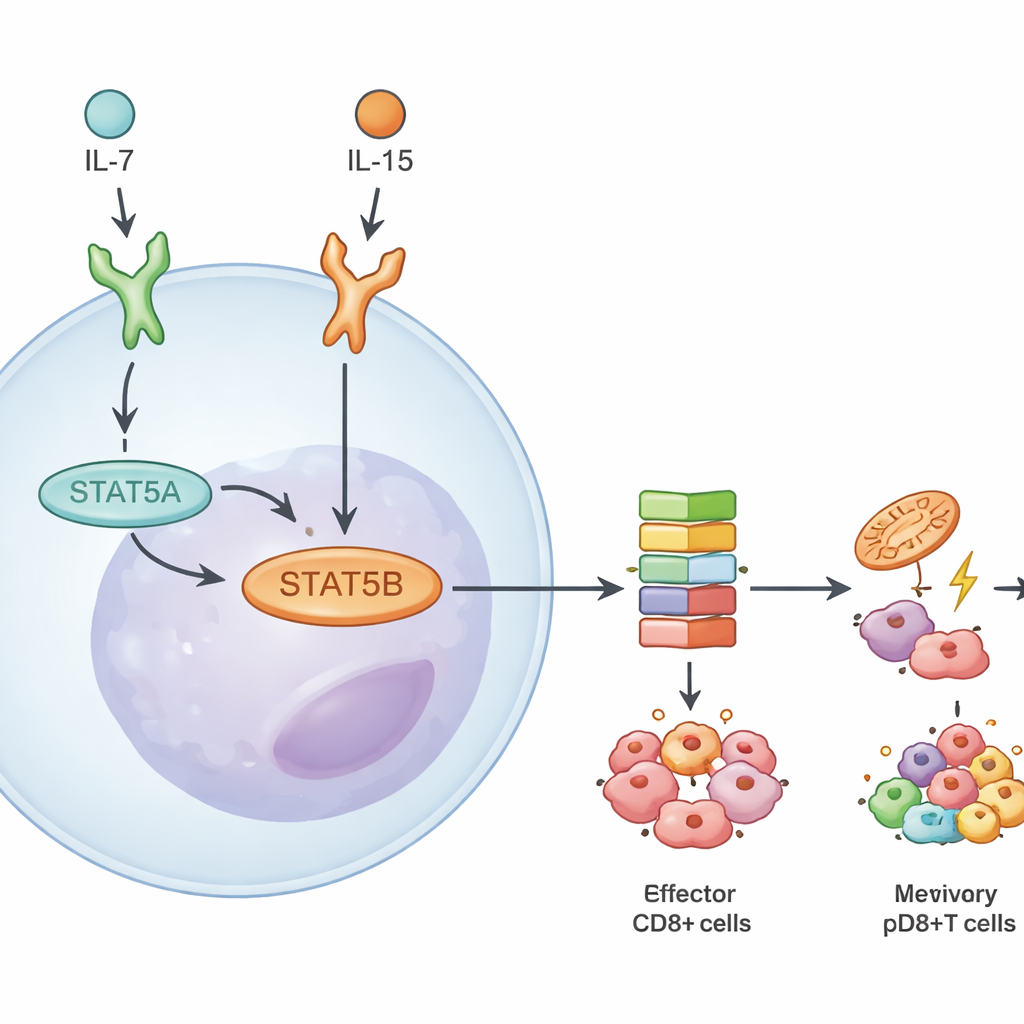
Wspólne cele DNA, ale działania zależne od kontekstu
Pomimo dominacji STAT5B, oba paralogi okazały się zajmować dużą część tego samego genomowego terytorium. Na mapach wiązań autorzy zaobserwowali, że większość miejsc o dużym znaczeniu była związana zarówno przez STAT5A, jak i STAT5B. Gdy ponownie wprowadzili do komórek brakujących STAT5 aktywną, nieustannie włączoną formę STAT5A, w dużej mierze wzmocniła ona geny dostępne również dla STAT5B, co sugeruje, że prawdziwie specyficzne cele wyłącznie dla STAT5A są rzadkie i stosunkowo słabe. Różnice wynikały raczej z siły działania i sytuacji, w jakich STAT5B funkcjonuje. Odpowiedzi różniły się w zależności od sygnału cytokiny (IL-7 vs. IL-15), stanu komórki (naiwna vs. pamięciowa) oraz przynależności do linii CD4+ lub CD8+. Na przykład IL-15 uruchamiał szersze programy genowe napędzane przez STAT5B niż IL-7, szczególnie w pamięciowych limfocytach CD8+.
Sygnatura genowa do śledzenia aktywności STAT5 w chorobie
Aby uchwycić istotę tej ścieżki, badacze wydestylowali 85-genową „rdzeniową sygnaturę STAT5”, która pojawiała się przy różnych cytokinach i stanach limfocytów CD8+. Po nałożeniu tej sygnatury na dane pojedynczych komórek RNA z myszy zakażonych wirusem, uwidoczniła się wyraźna grupa wczesnych komórek efektorowych lub wczesnych wyczerpanych CD8+, czyli tych, które doświadczają silnej, świeżej stymulacji cytokinowej. Sygnatura była znacznie słabiej aktywna w komórkach w pełni wyczerpanych lub spoczynkowych, co sugeruje, że może ona służyć jako bioinformatyczna latarnia wskazująca silne sygnalizowanie STAT5 podczas odpowiedzi immunologicznej, a być może także w nowotworach napędzanych nieprawidłową aktywnością STAT5B.
Co to oznacza dla pacjentów i terapii
Dla osoby niezaznajomionej z tematem kluczowy wniosek jest taki, że STAT5A i STAT5B działają jak dwa dźwignie na tej samej tablicy sterującej, ale jedna dźwignia — STAT5B — jest dłuższa i jest używana częściej. Oba paralogi przyczyniają się do tego, jak komórki zabójcze przeżywają, odpoczywają i tworzą pamięć, jednak STAT5B ma wyjątkowo silny wpływ na ich liczebność i na krytyczne programy genowe. Wyjaśniając tę asymetrię i przedstawiając genową sygnaturę aktywności STAT5, badanie dostarcza koncepcyjnej mapy do projektowania bardziej precyzyjnych immunoterapii — czy to przez dostrajanie leków cytokinowych, inżynierię komórek T, czy interpretację danych genomowych pacjentów — które wykorzystują potencjał komórek zabójczych bez przesunięcia równowagi układu odpornościowego ku chorobie.
Cytowanie: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Słowa kluczowe: STAT5B, Limfocyty CD8, sygnalizacja cytokin, immunoterapia, różnicowanie limfocytów T