Clear Sky Science · he
חוסר סימטריה ומחזוריות בין פארלוגים של STAT5 במצבי הבדלה של תאי T CD8+
מדוע זה חשוב לטיפולים חיסוניים עתידיים
הרבה מהטיפולים המבטיחים כיום בסרטן ובמחלות אוטואימוניות פועלים על ידי דחיפה קלה של תאי החיסון שלנו, ובעיקר תאי T CD8+ “הרוצחים”, להיאבק חזק יותר או להירגע. מתג מולקולרי מרכזי בתאים אלה הוא חלבון הנקרא STAT5, שמופיע למעשה בשתי גרסאות כמעט זהות. המחקר הזה שואל שאלה נראית פשוטה אך בעלת השלכות תרפויטיות גדולות: האם התאומים האלה אכן ניתנים להחלפה זה בזה, או שאחד מהם שולט בשקט?
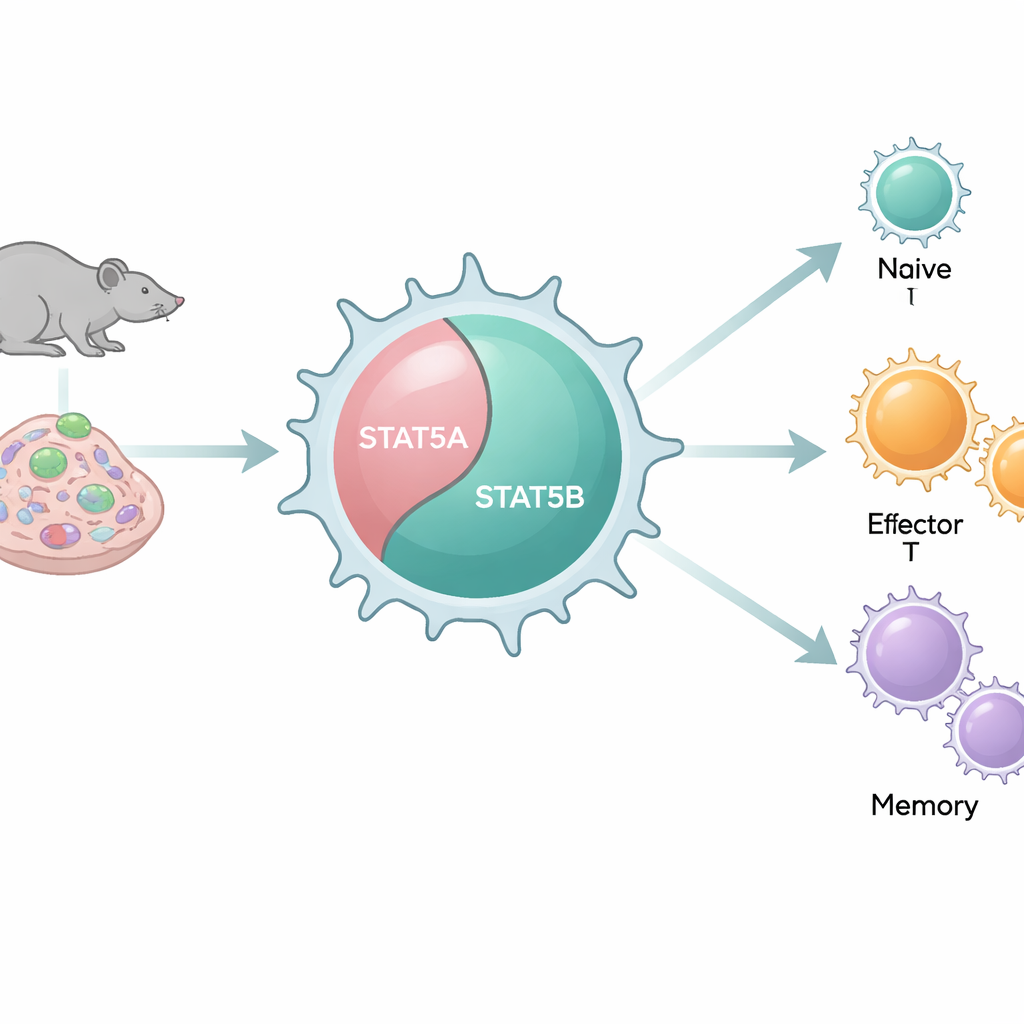
שני מתגים דומים שמתנהגים אחרת
הגנום שלנו נושא שתי עותקים קרובים, או פארלוגים, של STAT5: STAT5A ו-STAT5B. כי הם דומים כל כך ברמת המולקולות ונקשרים לרוב אותם מקטעי DNA, נטו להתייחס אליהם כאל רכיבים מיותרים זה לזה. עם זאת, מטופלים עם מוטציות מזיקות ב-STAT5B מפתחים בעיות חיסוניות חמורות, בעוד פגמים מקבילים ב-STAT5A נדירים. באמצעות מערך דגמי עכבר שמסירים באופן שיטתי את STAT5A, STAT5B או שניהם בשילובים שונים, החוקרים בוחנים כיצד כל פארלוג מעצב את מספרי התאים והתנהגותם של תאי T CD8 באורגניזמים חיים ובתאים בודדים.
תפקיד מפתח ל-STAT5B בשמירה על איזון תאי הרוצחים
כשהרמות הכוללות של STAT5 הורדו, תאי T CD8 ירדו באופן חמור בקשרי לימפה, בטחול ובמח העצם, מה שהביא לשיעורים מעוותים של תאי עזר (CD4+) מול תאי רוצח (CD8+). השתלות מח עצם מעורבות הראו שמדובר בעיקר בבעיה פנימית לתאים עצמם ולא רק בשינויים בסביבתם. הירידה הייתה החמורה ביותר כש-STAT5B נעדר, ובעכברים שהסתמכו על עותק אחד של STAT5A המצב היה הגרוע ביותר. באותו הזמן, תאי CD8 שנותרו התזזזו ממצב מנוחה נאיבי לעבר מצבי אפקטור וזיכרון מנוסים יותר, אך באופן פרדוקסלי לא יכלו לצייד עצמם במלואם בכלי ההרג המרכזיים כגון אנזימים וקולטנים מסוימים. ממצאים אלה מציירים את STAT5 כשומר על מספרם ואיכותם של תאי הרוצחים, כאשר STAT5B נושא בנטל הגדול יותר.
שותפים לא שווים מתחת למכסה המנוע
בחינה מעמיקה יותר בדקה כמה מכל פארלוג נוכח וכיצד הגנים מגיבים כאשר כל אחד מהם חסר. בתאי T CD8, STAT5B הרכיב בערך שני שלישים מסך חלבון והמסר של STAT5. חוסר ב-STAT5B הוריד את הפעלת שלב הפוספורילציה המרכזי במסלול יותר מאשר חוסר ב-STAT5A. כשחוקרים רצפו RNA מתאי CD8 נאיביים, אפקטורים וזיכרון שהועלו על ידי שני ציטוקינים, IL-7 ו-IL-15, הם מצאו הרבה יותר גנים שמוגדרים באופן לקוי בהיעדר STAT5B לעומת חוסר ב-STAT5A בלבד. רבים מהגנים הללו שולטים בהישרדות, מטבוליזם וביצירת זיכרון, מה שמבליט את STAT5B ככוח המניע המרכזי של תגובות ציטוקיניות בתאי רוצח.
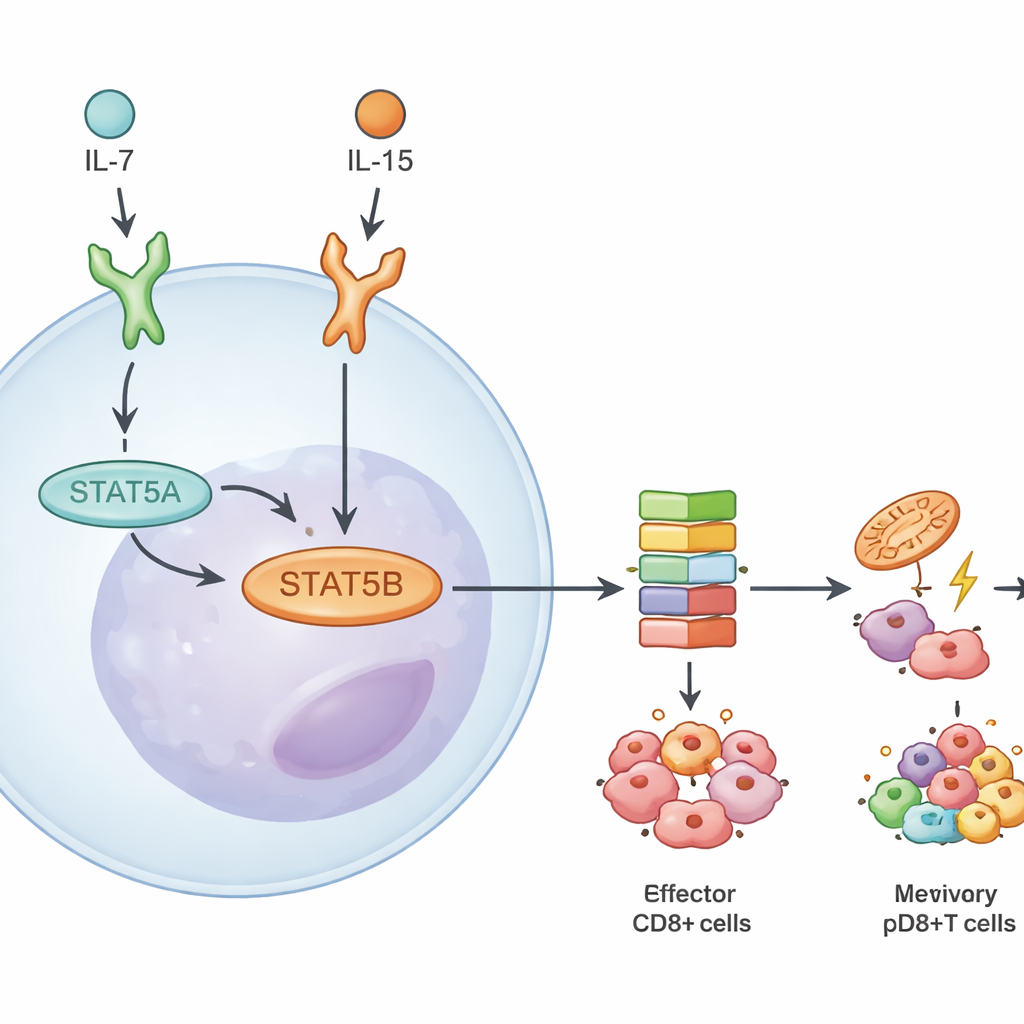
יעדי DNA משותפים אך פעולות תלויות הקשר
למרות הדומיננטיות של STAT5B, שני הפארלוגים תפסו הרבה משטח הגנום זהה. במפות קשירה ראו החוקרים שרוב אתרי ה-DNA בעלי השפעה גבוהה נקשרו הן על ידי STAT5A והן על ידי STAT5B. כאשר הם החזירו צורת STAT5A תמיד-פעילה לתאים חסרים, היא שיפרה בעיקר גנים שגם היו נגישים ל-STAT5B, מה שמרמז שמטרות ייחודיות ל-STAT5A הן נדירות וחלשות יחסית. במקום זאת, ההבדלים נבעו מעוצמת הפעולה ובאילו מצבים STAT5B פועל. התגובות השתנו בהתאם לאיזה ציטוקין איתר אותת (IL-7 לעומת IL-15), האם תאי ה-T היו נאיביים או זיכרון, והאם הם השתייכו לקו ה-CD4+ או ה-CD8+. למשל, IL-15 עורר תוכניות גנים רחבות יותר מונעות-STAT5B מאשר IL-7, במיוחד בתאי CD8 זיכרון.
חתימת גנים למעקב אחרי פעילות STAT5 במחלה
כדי לתמצת את המהות של המסלול, החוקרים זיקקו "חתימת STAT5 ליבה" בת 85 גנים שהופיעה על פני ציטוקינים ומצבי תאי CD8 שונים. כששילבו חתימה זו לנתוני RNA חד-תאיים ממכרסמים נגועים ויראלית, היא הדליקה אשכול מובחן של תאי CD8 אפקטור מוקדמים או מותשים-מוקדם, אותם תאים שחווים גירוי ציטוקיני חזק וטרי. החתימה הייתה פחות פעילה בתאים מותשים לחלוטין או מנוחים, מה שמרמז שהיא יכולה לשמש כמגדלור ביואינפורמטיבי לאותות STAT5 אינטנסיביים במהלך תגובות חיסוניות ואולי גם בסרטנים שמונעים על ידי פעילות מיותרת של STAT5B.
מה זה אומר למטופלים ולתרפיות
ללא היכרות ספציפית, המסר העיקרי הוא ש-STAT5A ו-STAT5B הם כמו שני ידיות בלוח בקרה אחד, אך ידית אחת, STAT5B, ארוכה יותר ונמשכת בתדירות גבוהה יותר. שני הפארלוגים תורמים לאופן שבו תאי הרוצחים שורדים, נחים ונזכרים, אך ל-STAT5B השפעה חזקה וייחודית על מספריהם ועל תוכניות גנים קריטיות. בהבהרת חוסר הסימטריה הזו, ובהצעת חתימת גנים לפעילות STAT5, המחקר מספק מפת מושגית לעיצוב אימונותרפיות מדויקות יותר — בין אם על ידי כוונון תרופות ציטוקינים, הנדסת תאים, או פרשנות נתוני גנום של מטופלים — שמנצלת את כוחם של תאי הרוצחים מבלי להזיז את המערכת החיסונית לעבר מחלה.
ציטוט: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
מילות מפתח: STAT5B, תאי T CD8, אותת ציטוקיני, אימונותרפיה, הבדלת תאי T