Clear Sky Science · ar
اللاتماثل والتكرار في نظائر STAT5 عبر حالات تمايز خلايا T CD8+
لماذا هذا مهم للعلاجات المناعية المستقبلية
تعمل العديد من أكثر العلاجات الواعدة اليوم للسرطان والأمراض المناعية الذاتية عن طريق دفع خلايانا المناعية نفسها، لا سيما خلايا T CD8+ «القاتلة»، للقتال بقوة أكبر أو التوقف عن النشاط. مفتاح جزيئي في هذه الخلايا هو بروتين يدعى STAT5، الذي يوجد في الواقع بنسختين متقاربتين جداً. تطرح هذه الدراسة سؤالاً بسيطاً ظاهرياً لكنه ذو تبعات علاجية كبيرة: هل هاتان النسختان قابلتان للاستبدال تماماً، أم أن إحداهما تقود العملية بصمت؟
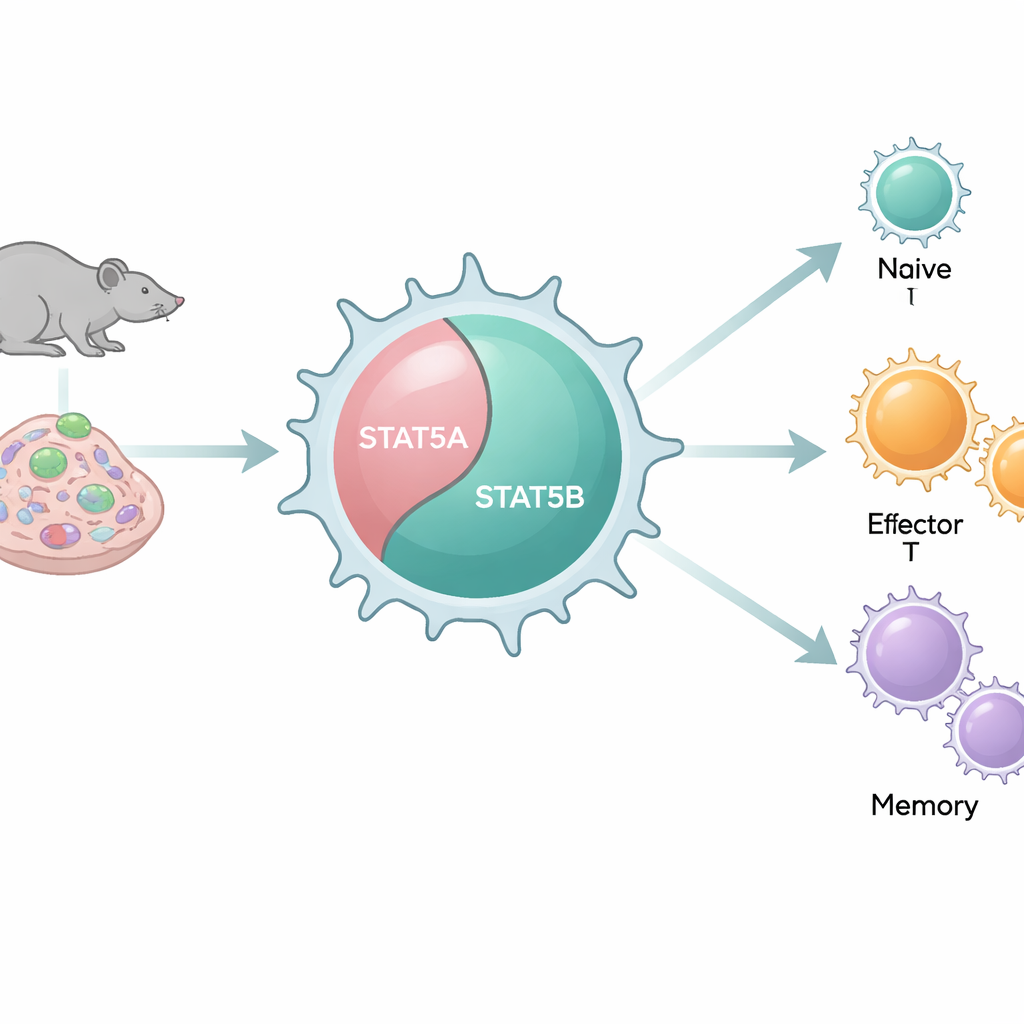
مفتاحان متشابهان يتصرفان بشكل مختلف
يحمل جينومنا نسختين مرتبطتين عن كثب، أو نظيرتين (paralogs)، من STAT5: STAT5A وSTAT5B. وبما أنهما متشابهان على المستوى الجزيئي ويرتبطان بالعديد من مناطق الحمض النووي نفسها، فقد اعتُبرا غالباً أجزاء زائدة عن بعضها. ومع ذلك، يُصاب المرضى باضطرابات مناعية خطيرة عند وجود طفرات ضارة في STAT5B، بينما عيوب مماثلة في STAT5A نادرة. باستخدام مجموعة من نماذج الفئران التي تزيل منهجياً STAT5A أو STAT5B أو كلاهما بتوليفات مختلفة، يفحص المؤلفون كيف يشكل كل نظير عدد وسلوك خلايا T CD8+ في الكائنات الحية والخلايا المعزولة.
دور رئيسي لـ STAT5B في الحفاظ على توازن خلايا T القاتلة
عندما خُفضت مستويات STAT5 الإجمالية، انخفضت خلايا T CD8+ بشكل حاد في العقد اللمفاوية والطحال ونخاع العظم، مما أدى إلى اختلال نسب بين خلايا المساعدة (CD4+) والخلايا القاتلة (CD8+). أظهرت عمليات زراعة نخاع عظم مختلطة أن السبب يعود معظم الأحيان إلى مشكلة داخل خلايا T نفسها، وليس مجرد تغيرات في بيئتها. كان الفقدان أشد عندما غاب STAT5B، وكانت الفئران التي تعتمد على نسخة واحدة من STAT5A هي الأسوأ حالاً. في الوقت نفسه، انتقلت خلايا CD8+ المتبقية من حالة سكون وطفولية نحو حالات أكثر خبرة مثل الخلايا الفاعلة والذاكرة، لكنها، بشكل متناقض، لم تتمكن من التسلح بالكامل بأدوات القتل الأساسية مثل إنزيمات ومستقبلات محددة. يكشف هذا أن STAT5 يعمل كحارس لكل من عدد وجودة خلايا T القاتلة، مع ثقل أكبر لـ STAT5B.
شركاء غير متكافئين تحت الغطاء
بالغوص أعمق، قاس الفريق كمية كل نظير ومدى استجابة الجينات عند غياب كلٍ منهما. في خلايا T CD8+، شكل STAT5B نحو ثلثي إجمالي بروتين ورسالة STAT5. قلل فقدان STAT5B تنشيط خطوة الفسفرة الرئيسية في المسار أكثر من فقدان STAT5A. عندما نسخ الباحثون الحمض النووي الرايبوزي من خلايا CD8+ الطفولية والفاعلة والذاكرية المنبهة بواسطة سيتوكينين، IL-7 وIL-15، وجدوا عدداً أكبر بكثير من الجينات المختلة التنظيم في غياب STAT5B مقارنةً عندما كان STAT5A فقط ناقصاً. تتحكم العديد من هذه الجينات في البقاء والتمثيل الغذائي وتكوين الذاكرة، مما يبرز STAT5B كسائق رئيسي لاستجابات السيتوكين في خلايا T القاتلة.
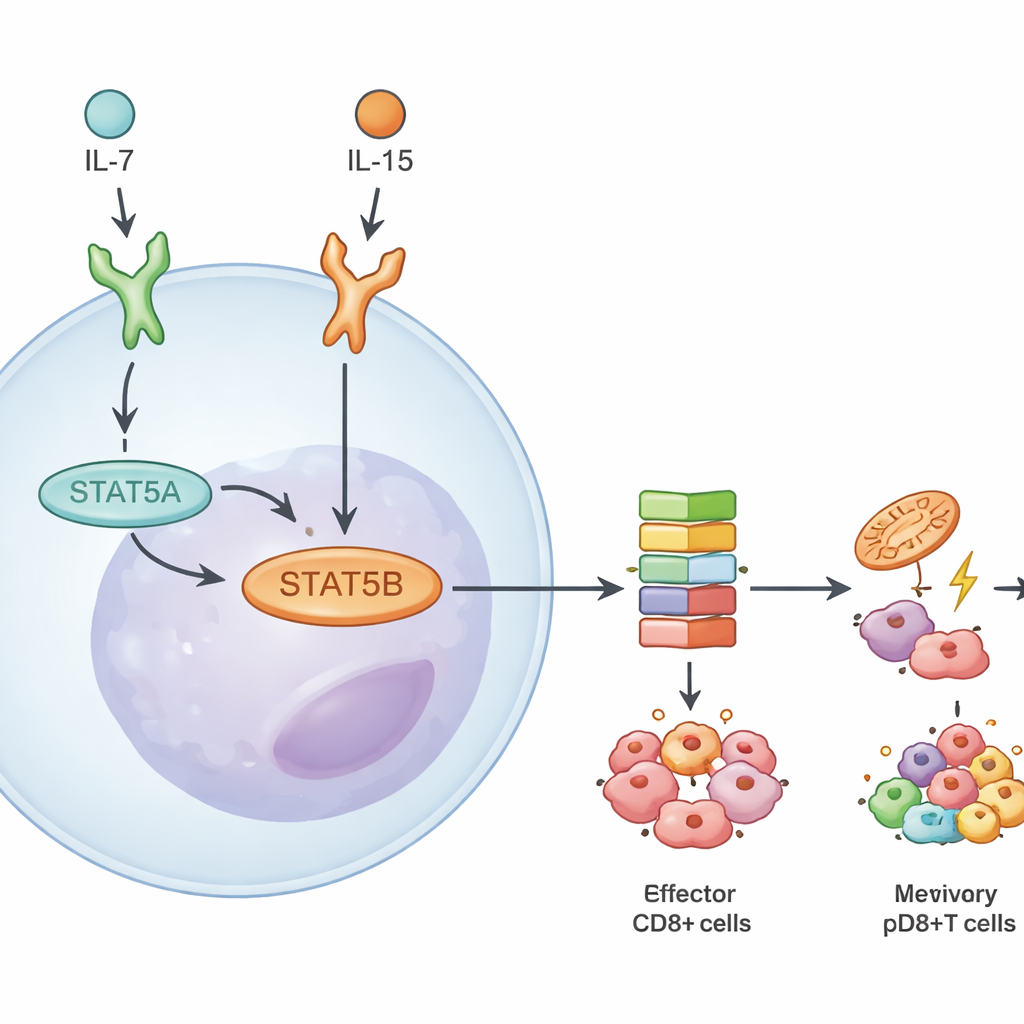
أهداف DNA مشتركة لكن أفعال محددة بالسياق
رغم هيمنة STAT5B، تبين أن النظيرين يشغلان الكثير من نفس المواقع الجينية. باستخدام خرائط الارتباط، رأى المؤلفون أن معظم مواقع الحمض النووي ذات التأثير العالي كانت مرتبطة كلاً من STAT5A وSTAT5B. عندما أعادوا إدخال شكل STAT5A دائماً المنشط في خلايا ناقصة، عزز ذلك إلى حد كبير الجينات التي كان STAT5B أيضاً قادراً على الوصول إليها، مما يشير إلى أن الأهداف الخاصة بـ STAT5A فقط نادرة وضعيفة نسبياً. بدلاً من ذلك، نشأت الاختلافات من قوة عمل STAT5B وفي أي حالات يعمل. تنوعت الاستجابات اعتماداً على أي سيتوكين أرسل الإشارة (IL-7 مقابل IL-15)، وما إذا كانت الخلية طفولية أو ذاكرية، وإذا كانت تنتمي إلى سلالة CD4+ أو CD8+. فعلى سبيل المثال، حفز IL-15 برامج جينية أوسع يقودها STAT5B مقارنةً بـ IL-7، لا سيما في خلايا T CD8+ الذاكرية.
توقيع جيني لتعقّب نشاط STAT5 في المرض
لالتقاط جوهر هذا المسار، استخلص الباحثون «توقيع STAT5 الأساسي» المكوّن من 85 جيناً والذي ظهر عبر سيتوكينات وحالات خلايا T CD8+ مختلفة. عند تطبيق هذا التوقيع على بيانات RNA أحادي الخلية من فئران مصابة بفيروس، أبرز عنقوداً مميزاً من خلايا CD8+ الفاعلة المبكرة أو المتعبة مبكراً، وهي الخلايا التي تتعرض لتحفيز سيتوكيني قوي وجديد. كان التوقيع أقل نشاطاً بكثير في الخلايا المستنفدة تماماً أو الخاملة، مما يشير إلى أنه يمكن أن يعمل كمنارة بيوإعلامية لإشارات STAT5 المكثفة أثناء الاستجابات المناعية وربما في أنواع السرطان التي تقودها نشاطات شاذة لـ STAT5B.
ما الذي يعنيه هذا للمرضى والعلاجات
لغير المتخصص، الخلاصة أن STAT5A وSTAT5B يشبهان رافعتين على لوحة التحكم نفسها، لكن إحدى الروافع، STAT5B، أطول وتُسحب أكثر. كلاهما يساهم في كيفية بقاء خلايا T القاتلة وراحتها وتكوين الذاكرة، ومع ذلك لِـ STAT5B تأثير فريد وقوي على أعدادها وعلى برامج جينية حاسمة. من خلال توضيح هذا اللاتماثل، ومن خلال تقديم توقيع جيني لنشاط STAT5، توفر الدراسة خريطة مفهومية لتصميم علاجات مناعية أكثر دقة — سواء عبر ضبط أدوية السيتوكين، أو هندسة الخلايا التائية، أو تفسير بيانات الجينوم المرضى — التي تستغل قدرة خلايا T القاتلة دون أن تزيح التوازن المناعي نحو المرض.
الاستشهاد: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
الكلمات المفتاحية: STAT5B, خلايا T CD8, إشارة السيتوكين, العلاج المناعي, تمايز خلايا T