Clear Sky Science · pt
Assimetria e redundância dos paralogos STAT5 nos estados de diferenciação de células T CD8+
Por que isso importa para futuras terapias imunológicas
Muitos dos tratamentos mais promissores contra câncer e doenças autoimunes atuam ao modular nossas próprias células imunes, especialmente as células T CD8+ “assassinas”, para que ataquem com mais força ou se acalmem. Um interruptor molecular chave nessas células é uma proteína chamada STAT5, que na verdade existe em duas versões quase gêmeas. Este estudo faz uma pergunta aparentemente simples, mas com grandes implicações terapêuticas: esses gêmeos são realmente intercambiáveis ou um deles dirige o processo de forma preponderante?
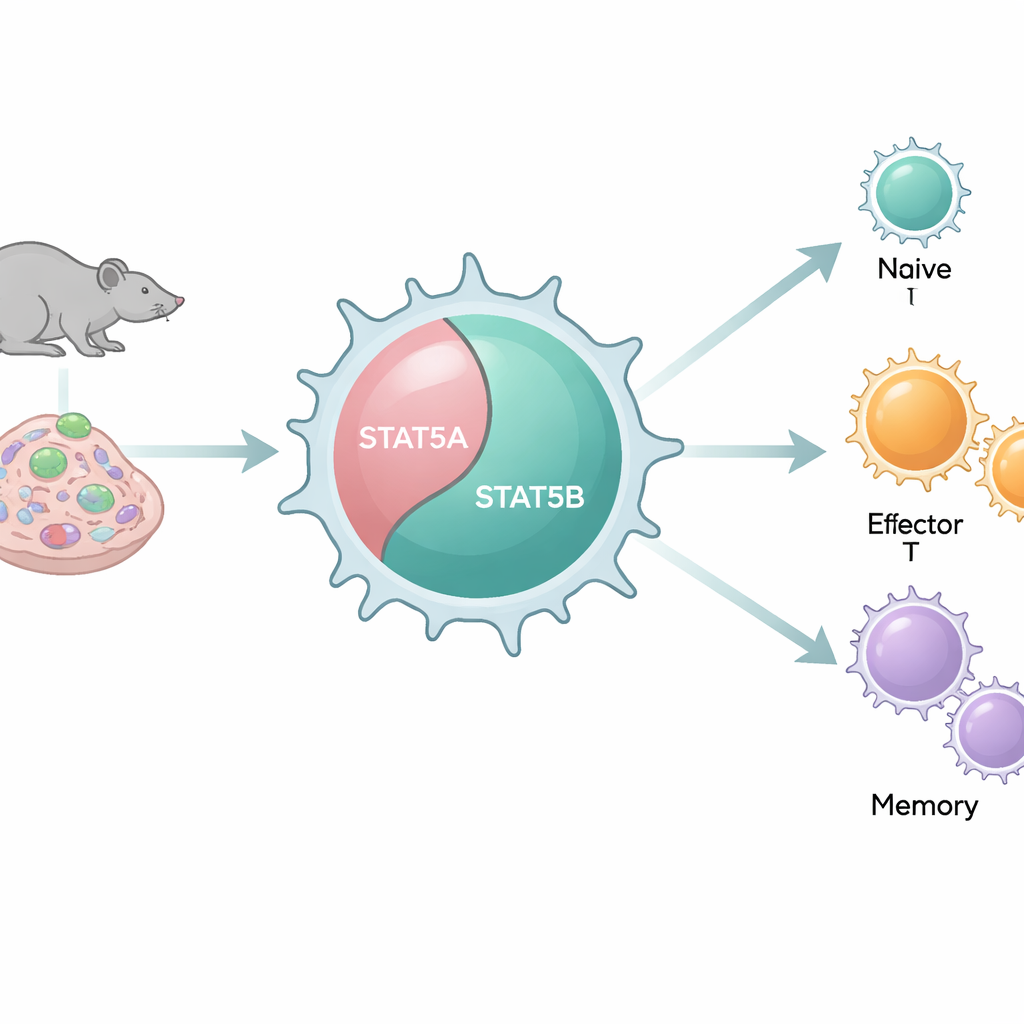
Dois interruptores similares que se comportam de forma diferente
Nossos genomas carregam duas cópias estreitamente relacionadas, ou paralogos, de STAT5: STAT5A e STAT5B. Porque são tão parecidas a nível molecular e se ligam a muitos dos mesmos trechos de DNA, muitas vezes foram tratadas como partes redundantes. Ainda assim, pacientes com mutações deletérias em STAT5B desenvolvem problemas imunológicos graves, enquanto defeitos comparáveis em STAT5A são raros. Usando um conjunto de modelos de camundongos que removem sistematicamente STAT5A, STAT5B ou ambos em diferentes combinações, os autores investigam como cada paralogo molda o número e o comportamento das células T CD8+ em organismos vivos e em células isoladas.
Papel chave de STAT5B em manter o equilíbrio das células T assassinas
Quando os níveis totais de STAT5 foram reduzidos, as células T CD8+ caíram acentuadamente em linfonodos, baço e medula óssea, levando a proporções alteradas entre células T auxiliares (CD4+) e assassinas (CD8+). Transplantes de medula óssea mista mostraram que isso se deve em grande parte a um problema intrínseco às próprias células T, e não apenas a mudanças no ambiente. A perda foi mais severa quando STAT5B estava ausente, e camundongos que dependiam de uma única cópia de STAT5A foram os mais afetados. Ao mesmo tempo, as células T CD8+ remanescentes migraram de um estado ingênuo e em repouso para estados mais experientes de efector e memória, mas paradoxalmente não conseguiram se equipar plenamente com ferramentas essenciais de ataque, como enzimas e receptores específicos. Isso revela STAT5 como um guardião tanto dos números quanto da qualidade das células T assassinas, com STAT5B carregando o peso maior.
Parceiros desiguais sob o capô
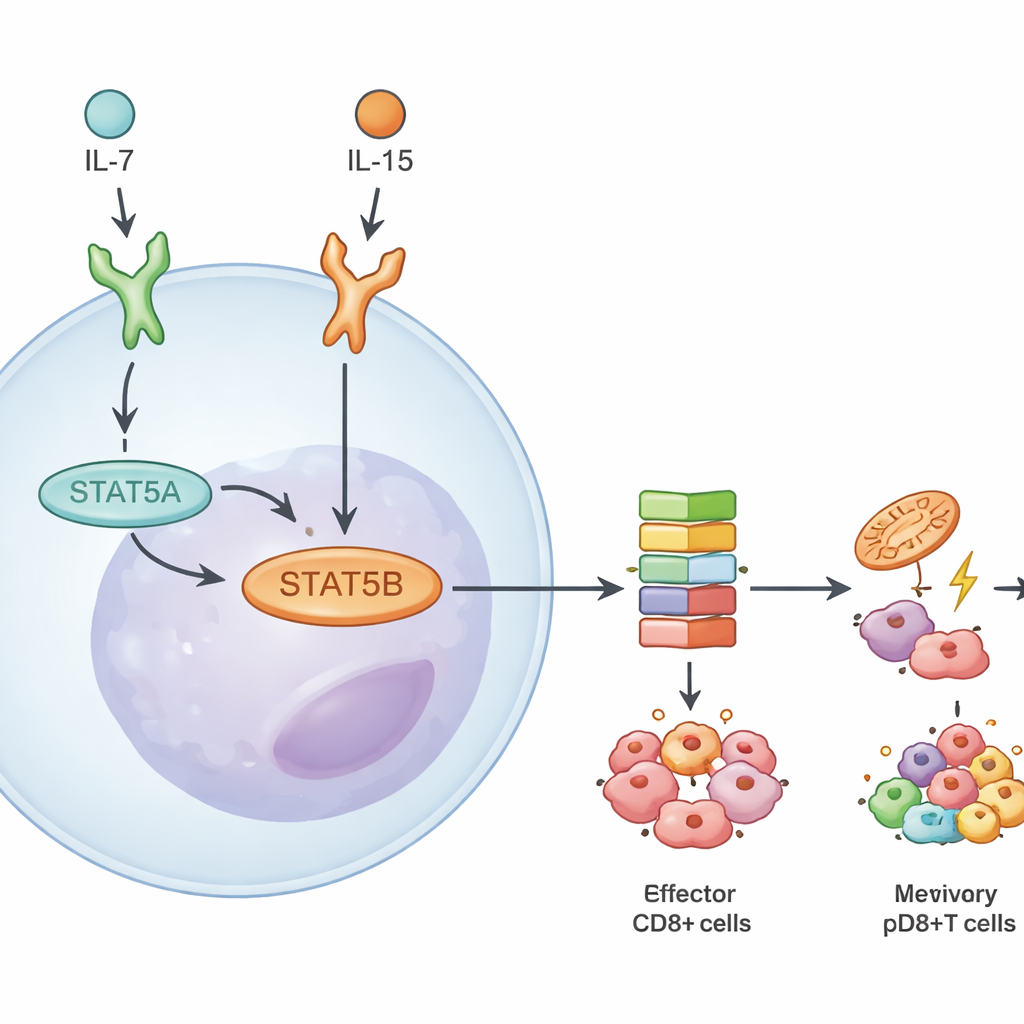
Ao investigar mais a fundo, a equipe mediu quanto de cada paralogo está presente e como os genes respondem quando um deles falta. Em células T CD8+, STAT5B constituiu aproximadamente dois terços do total da proteína e do transcrito STAT5. A perda de STAT5B reduziu a ativação da etapa chave de fosforilação da via mais do que a perda de STAT5A. Quando os pesquisadores sequenciaram o RNA de células T CD8+ ingênuas, efectoras e de memória estimuladas por duas citocinas, IL-7 e IL-15, encontraram muito mais genes desregulados na ausência de STAT5B do que quando apenas STAT5A faltava. Muitos desses genes controlam sobrevivência, metabolismo e formação de memória, ressaltando STAT5B como o principal condutor das respostas a citocinas nas células T assassinas.
Alvos de DNA compartilhados, mas ações específicas ao contexto
Apesar do predomínio de STAT5B, os dois paralogos acabaram ocupando grande parte do mesmo território genômico. Usando mapas de ligação, os autores observaram que a maioria dos sítios de DNA de alto impacto era ligada por ambos STAT5A e STAT5B. Quando reintroduziram uma forma sempre ativa de STAT5A em células deficientes, isso impulsionou em grande parte genes que também eram acessíveis por STAT5B, sugerindo que alvos exclusivos de STAT5A são raros e relativamente fracos. Em vez disso, as diferenças surgiram de quão fortemente e em que situações STAT5B age. As respostas variaram dependendo de qual citocina sinalizava (IL-7 versus IL-15), se a célula T era ingênua ou de memória, e se pertencia à linhagem CD4+ ou CD8+. A IL-15, por exemplo, desencadeou programas gênicos mais amplos dirigidos por STAT5B do que a IL-7, especialmente em células T CD8+ de memória.
Uma assinatura gênica para rastrear a atividade de STAT5 em doenças
Para capturar a essência dessa via, os investigadores destilaram uma “assinatura core STAT5” de 85 genes que apareceu através de diferentes citocinas e estados de células T CD8+. Ao sobrepor essa assinatura a dados de RNA de célula única de camundongos infectados por vírus, ela destacou um aglomerado distinto de células T CD8+ de efetor inicial ou início de exaustão, as mesmas células que experimentavam forte e recente estimulação por citocinas. A assinatura foi muito menos ativa em células totalmente exaustas ou em repouso, sugerindo que pode atuar como um farol bioinformático para sinalização intensa de STAT5 durante respostas imunes e possivelmente em cânceres impulsionados por atividade aberrante de STAT5B.
O que isso significa para pacientes e terapias
Para um público não especializado, a mensagem principal é que STAT5A e STAT5B são como duas alavancas em um mesmo painel de controle, mas uma alavanca, STAT5B, é mais longa e acionada com mais frequência. Ambos contribuem para como as células T assassinas sobrevivem, descansam e lembram, porém STAT5B tem uma influência singularmente forte sobre seus números e sobre programas gênicos cruciais. Ao esclarecer essa assimetria e ao oferecer uma assinatura gênica da atividade de STAT5, o estudo fornece um mapa conceitual para projetar imunoterapias mais precisas — seja ajustando drogas baseadas em citocinas, engenheirando células T ou interpretando dados genômicos de pacientes — que aproveitem o poder das células T assassinas sem levar o sistema imune ao desequilíbrio.
Citação: Ristin, S., Dalzell, M., Armstrong, C. et al. Asymmetry and redundancy of STAT5 paralogs across CD8+ T cell differentiation states. Commun Biol 9, 529 (2026). https://doi.org/10.1038/s42003-026-09999-9
Palavras-chave: STAT5B, células T CD8, sinalização por citocinas, imunoterapia, diferenciação de células T