Clear Sky Science · tr
Kolorektal kanserin karaciğer metastaz yollarını ortaya çıkarmada CCDC3 aracılı mekanizmaları ortaya çıkarmak için YZ’yi birleştirmek
Bu araştırma neden önemli
Kolorektal kanser dünya genelinde en yaygın kanserlerden biridir ve birçok ölüm hastalık yalnızca karaciğere yayıldıktan sonra gerçekleşir. Doktorlar, kromozomları çok instabil olan tümörlerin genellikle daha agresif ve tedavisi daha zor olduğunu biliyor, ancak çevredeki kanser dışı hücrelerin tümörleri bu tehlikeli duruma nasıl ittiği belirsizdi. Bu çalışma, tümör çevresindeki destek hücreleri ile kanser hücreleri arasındaki gizli bir iletişim hattını ortaya koyuyor; genetik kargaşayı tetikleyen ve karaciğer metastazlarını besleyen bir olay zincirini açığa çıkarıyor—ve bunu durdurmanın yeni yollarına işaret ediyor.
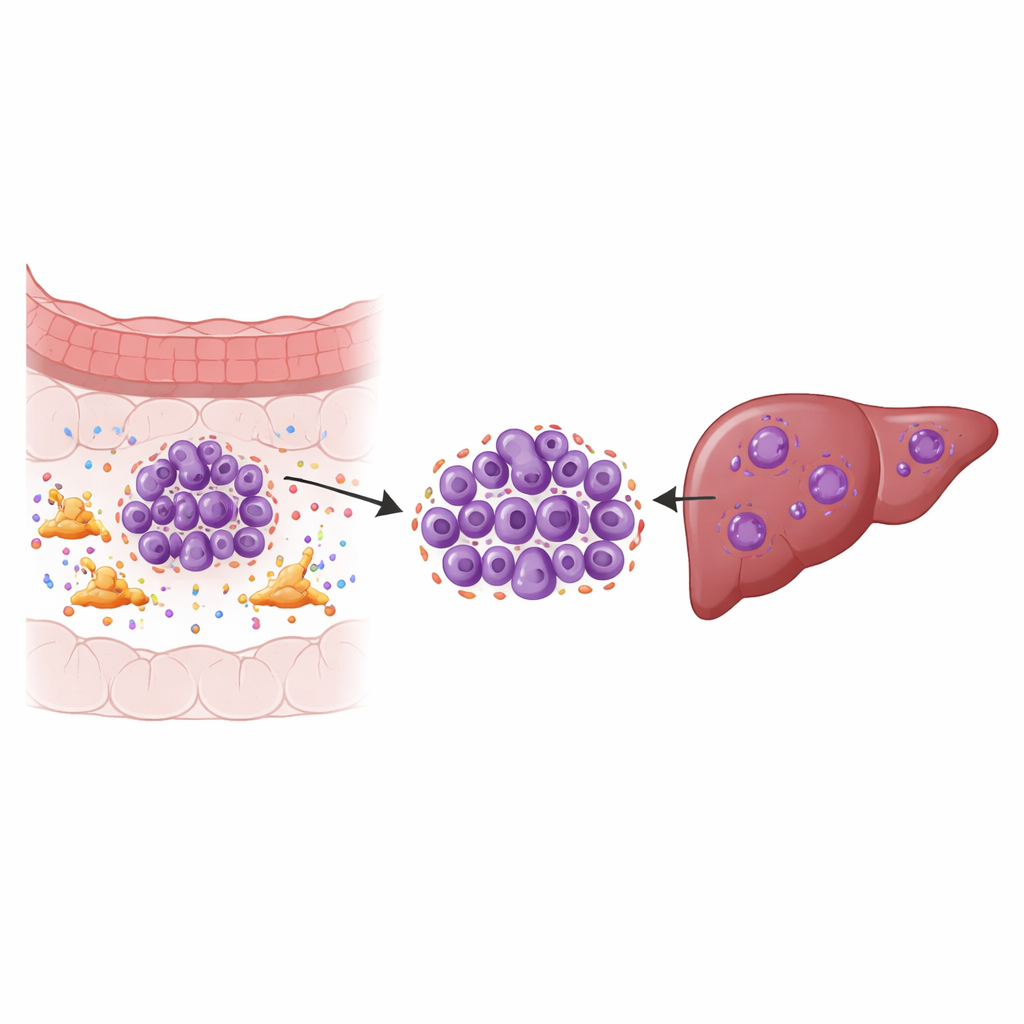
Tümör çevresindeki gizli yardımcılar
Solid tümörler sadece kanser hücrelerinin kümeleri değildir; onlar birer ekosistemdir. Bu ekosistemin kilit sakinlerinden biri, tümör çevresini yeniden şekillendiren ve çok sayıda sinyal molekülü salgılayan bir bağ doku hücresi türü olan kanserle ilişkili fibroblastlardır. Araştırmacılar birincil kolorektal tümörler, eşleşen karaciğer metastazları, yakın normal dokular ve kandan alınan örneklerde tek hücre RNA dizileme kullandılar; dokuz ana hücre tipini haritalandırdılar ve ardından kanser hücrelerine yakından baktılar. Karaciğerde belirli tümör alt grupları keşfettiler; bu gruplar, kromozomların kopyalanması ve bölünmesinde sık hatalarla ilişkili olan güçlü kromozomal kararsızlık belirtileri gösteriyordu—bu durum hızlı büyüme, tedavi direnci ve kötü sağkalımla bağlantılıdır.
Tehlikeli tümör hücreleri için sayısal bir skor
Hangi kanserlerin en yüksek riske sahip olduğunu anlamak için ekip, birden çok kanıt katmanını yakalayan bileşik bir “kararsızlık indeksi” oluşturdu: gen ekspresyonu desenleri, çıkarımsal kromozom kopya sayısı değişiklikleri ve bilinen kararsızlığa ilişkin genler. Yüksek skorlu tümör hücreleri birincil tümörlere göre karaciğer metastazlarında çok daha yaygındı. Bu yüksek indeksli hücreler aşırı aktif bir hücre döngüsü, daha fazla DNA hasarı ve onarım faaliyeti ve işgal ile yayılma ile ilişkili özellikler gösteriyordu. Başka bir deyişle, kromozomlar ne kadar kararsızsa, kanser hücreleri o kadar saldırgan ve uyum sağlayabilir görünüyordu—bu da kararsızlığın sadece kanserin bir yan ürünü değil, ilerlemesinin bir itici gücü olduğu fikrini destekliyor.
Fibroblastlardan gelen gizli bir sinyal
Sıradaki soru, tümör ortamında kanser hücrelerini bu kararsız duruma iten şeyin ne olduğu idi. Farklı hücre tiplerinin sinyal molekülleri yoluyla nasıl “konuştuğunu” analiz ederek, araştırmacılar özellikle fibroblastlar ile kromozomal olarak kararsız tümör hücreleri arasında güçlü bir iletişim buldular. Özellikle bir fibroblast grubu karaciğer metastazlarında zenginleşmişti ve daha kötü hasta sağkalımıyla ilişkilendirildi. Bu fibroblastlarda aktif olan genler, kararsızlığı yüksek kanser hücrelerindeki genlerle karşılaştırıldığında bir tanesi öne çıktı: CCDC3, ağırlıklı olarak fibroblastlar tarafından üretilen ve birincil tümörlere kıyasla karaciğer lezyonlarında çok daha bol bulunan, az çalışılmış bir proteindi. Tümörlerinde daha yüksek CCDC3 düzeyleri olan hastalar genellikle daha kısa süre yaşadı; bu da bu sinyalin agresif hastalığın ana teşvik edicilerinden biri olabileceğini düşündürüyor.
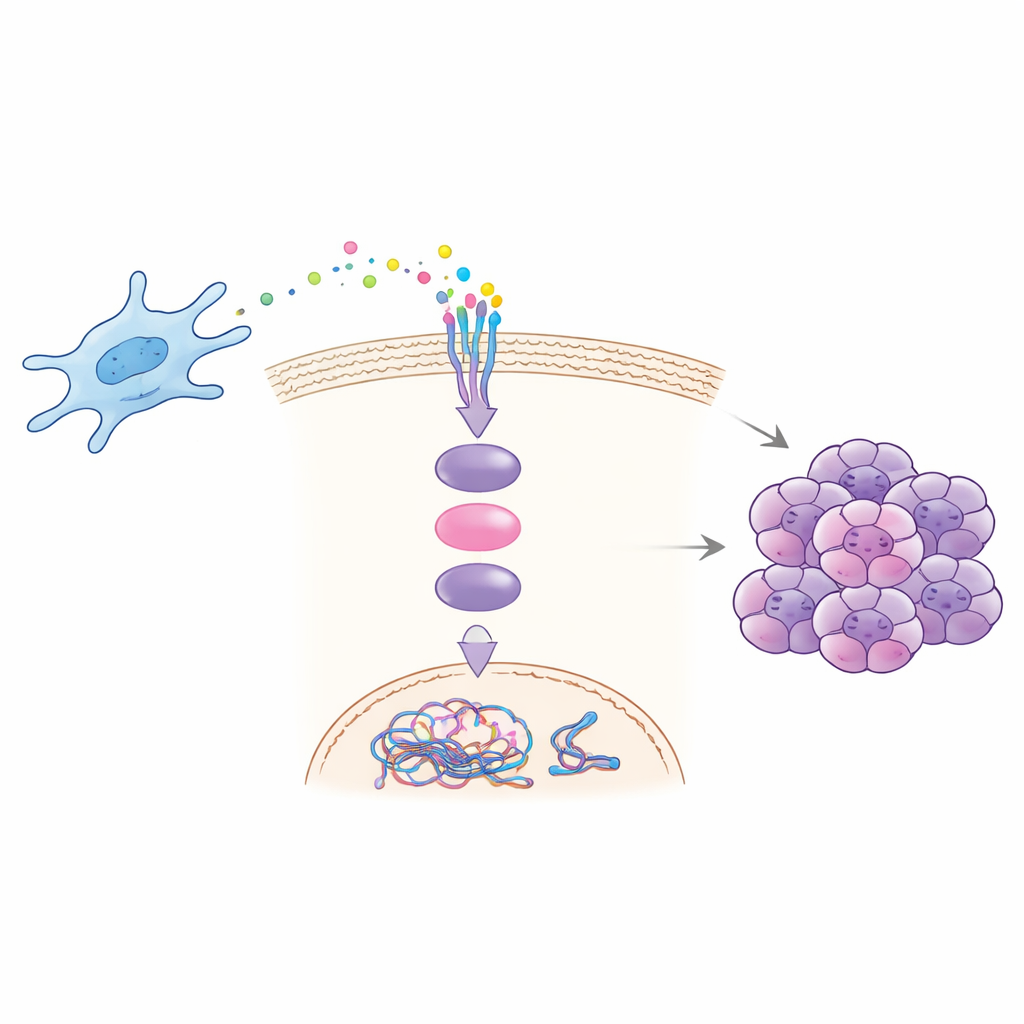
Bir sinyalin zincirleme reaksiyonu nasıl tetiklediği
Laboratuvar ve hayvan deneyleri CCDC3’ün maligniteyi nasıl sürüklediğini ortaya koydu. Karaciğer metastazlarından alınan fibroblastlar daha fazla CCDC3 salgıladı ve kanser hücreleri ile birlikte yetiştirildiklerinde, kanser hücrelerinin göç etme, invaze etme, koloni oluşturma ve kromozomal kararsızlık belirtileri gösterme yeteneklerini artırdı. Saflaştırılmış CCDC3 eklenmesi kanser hücrelerinde bu etkileri yeniden üretti; fibroblastlarda CCDC3 bloke edildiğinde ise bu etkiler azaldı. Ekip, CCDC3’ün kanser hücreleri üzerindeki CXCR3 adlı bir reseptöre bağlandığını ve bunun ardından hücre içindeki iyi bilinen bir haberci proteini, STAT3’ü aktive ettiğini gösterdi. STAT3 aktifleştikten sonra çekirdeğe gidip doğrudan DNA replikasyonunu lisanslamaya yardımcı olan CDT1 adlı proteinin üretimini artırıyor. Aşırı CDT1, DNA kopyalamanın normal zamanlamasını ve doğruluğunu bozarak kromozom hatalarını ve kararsızlığı teşvik ediyor.
Mekanizmadan potansiyel tedaviye
Bu zincirin her adımını—CCDC3, CXCR3, STAT3 veya CDT1—seçici olarak bloke ederek araştırmacılar, petri kaplarında ve fare modellerinde kanser hücrelerinin invazif davranışını ve büyümesini zayıflatabildiler. Ek CCDC3 verilen farelerde daha büyük tümörler ve daha fazla karaciğer metastazı gelişirken, CCDC3’e karşı bir antikor veya bir STAT3 inhibitörü ile tedavi edilenlerde tümör büyümesi daha yavaş ve karaciğer lezyonları daha azdı. Bu bulgular, tümör çevresini kanser hücrelerindeki içsel genetik kargaşaya bağlayan net bir fibroblast–tümör sinyal yolunu tanımlıyor. Hastalar için bu çalışma, CCDC3–CXCR3–STAT3–CDT1 eksenini hedeflemenin ya da CCDC3 düzeylerini agresif hastalığın bir uyarı işareti olarak kullanmanın bir gün kolorektal kanserin karaciğer metastazlarını önlemeye veya tedavi etmeye yardımcı olabileceğini öne sürüyor.
Atıf: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Anahtar kelimeler: kolorektal kanser, karaciğer metastazı, tümör mikroçevresi, kromozomal kararsızlık, kanserle ilişkili fibroblastlar