Clear Sky Science · es
Combinando IA para revelar las vías mediadas por CCDC3 en la metástasis hepática del cáncer colorrectal
Por qué importa esta investigación
El cáncer colorrectal es uno de los tumores más frecuentes en el mundo, y muchas muertes se producen cuando la enfermedad ya se ha diseminado al hígado. Los médicos saben que los tumores con cromosomas muy inestables tienden a ser más agresivos y más difíciles de tratar, pero no estaba claro cómo las células no cancerosas circundantes contribuyen a empujar a los tumores hacia ese estado peligroso. Este estudio descubre una línea de comunicación oculta entre las células de apoyo alrededor del tumor y las células cancerosas, revelando una cadena de eventos que genera caos genético y alimenta las metástasis hepáticas—y apunta a nuevas formas de detenerlo.
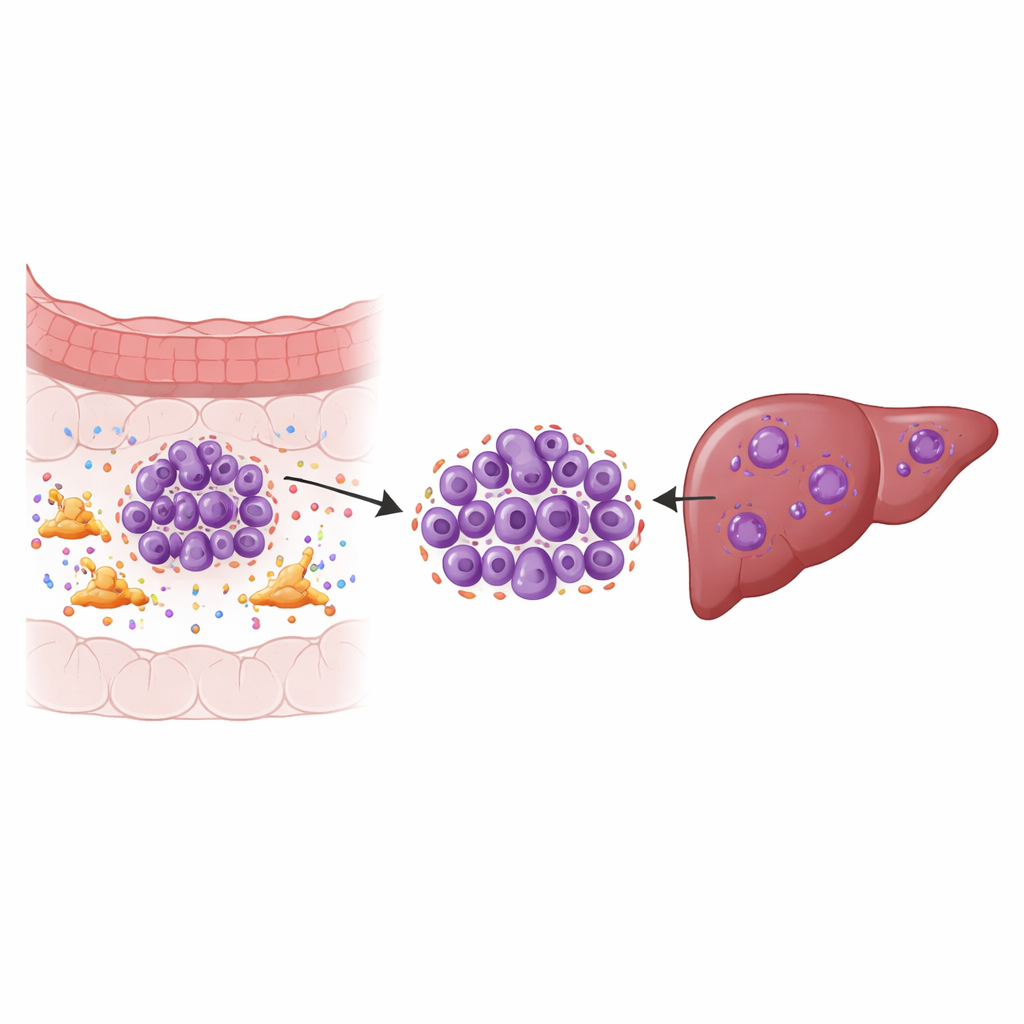
Los ayudantes ocultos alrededor del tumor
Los tumores sólidos no son solo grupos de células cancerosas; son ecosistemas. Un habitante clave de este ecosistema es el fibroblasto asociado al cáncer, un tipo de célula del tejido conectivo que remodela el entorno del tumor y secreta numerosas moléculas de señalización. Utilizando secuenciación de ARN de célula única en muestras de tumores colorrectales primarios, metástasis hepáticas coincidentes, tejidos normales cercanos y sangre, los investigadores cartografiaron nueve tipos celulares principales y luego se centraron en las propias células tumorales. Descubrieron subgrupos tumorales específicos en el hígado que mostraban señales claras de inestabilidad cromosómica—errores frecuentes en cómo se copian y separan los cromosomas—lo cual se asocia con crecimiento rápido, resistencia al tratamiento y mala supervivencia.
Una puntuación numérica para las células tumorales peligrosas
Para entender qué cánceres corren más riesgo, el equipo construyó un “índice de inestabilidad” compuesto que integraba múltiples capas de evidencia: patrones de expresión génica, cambios inferidos en el número de copias cromosómicas y genes conocidos relacionados con la inestabilidad. Las células tumorales con puntuaciones altas eran mucho más frecuentes en las metástasis hepáticas que en los tumores primarios. Estas células de alto índice mostraron un ciclo celular sobreactivado, más actividad de daño y reparación del ADN, y rasgos asociados con invasión y diseminación. En otras palabras, cuanto más inestables eran los cromosomas, más agresivas y adaptables parecían las células cancerosas—lo que respalda la idea de que la inestabilidad no es solo un efecto secundario del cáncer, sino un impulsor de su progresión.
Una señal secreta de los fibroblastos
La siguiente pregunta fue qué elemento del microambiente tumoral podría estar empujando a las células cancerosas hacia ese estado inestable. Al analizar cómo los distintos tipos celulares «se comunican» mediante moléculas señalizadoras, los investigadores encontraron una comunicación especialmente intensa entre los fibroblastos y las células tumorales con inestabilidad cromosómica. Un grupo particular de fibroblastos estaba enriquecido en las metástasis hepáticas y se asociaba con una peor supervivencia de los pacientes. Cuando los genes activos en estos fibroblastos se compararon con los de las células cancerosas con alto índice de inestabilidad, destacó uno: CCDC3, una proteína poco estudiada que se producía principalmente en fibroblastos y era mucho más abundante en las lesiones hepáticas que en los tumores primarios. Los pacientes cuyos tumores presentaban niveles más altos de CCDC3 tendían a vivir menos tiempo, lo que sugiere que esta señal podría ser un promotor clave de la enfermedad agresiva.
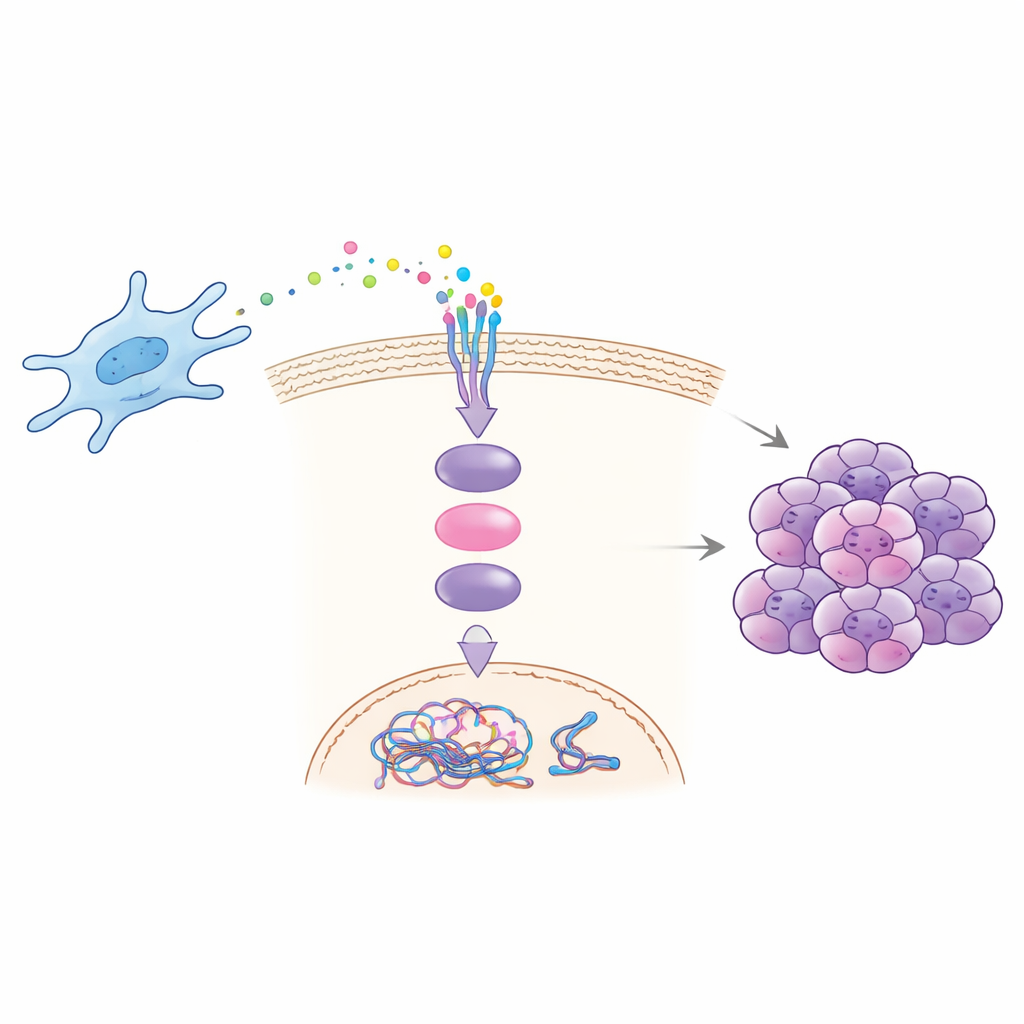
Cómo una señal desencadena una reacción en cadena
Experimentos de laboratorio y en animales revelaron cómo CCDC3 impulsa la malignidad. Los fibroblastos extraídos de metástasis hepáticas secretaban más CCDC3 y, cuando se cultivaban junto a células cancerosas, aumentaban la capacidad de las células tumorales para migrar, invadir, formar colonias y mostrar signos de inestabilidad cromosómica. Añadir CCDC3 purificado a las células cancerosas reprodujo estos efectos, mientras que bloquear CCDC3 en fibroblastos los redujo. El equipo demostró que CCDC3 se une a un receptor llamado CXCR3 en las células cancerosas, que a su vez activa una proteína mensajera intracelular bien conocida, STAT3. Una vez activada, STAT3 viaja al núcleo y aumenta directamente la producción de CDT1, una proteína que ayuda a autorizar la replicación del ADN. El exceso de CDT1 altera la sincronía y la precisión normales de la copia del ADN, promoviendo errores cromosómicos e inestabilidad.
Del mecanismo al posible tratamiento
Al bloquear selectivamente cada paso de esta cadena—CCDC3, CXCR3, STAT3 o CDT1—los investigadores pudieron frenar el comportamiento invasivo y el crecimiento de las células cancerosas en placas de cultivo y en modelos de ratón. Los ratones a los que se les administró CCDC3 adicional desarrollaron tumores más grandes y más metástasis hepáticas, mientras que aquellos tratados con un anticuerpo contra CCDC3 o un inhibidor de STAT3 mostraron un crecimiento tumoral más lento y menos lesiones hepáticas. Estos hallazgos definen una ruta de señalización clara de fibroblasto a tumor que conecta el microambiente tumoral con el caos genético interno de las células cancerosas. Para los pacientes, este trabajo sugiere que dirigir la vía CCDC3–CXCR3–STAT3–CDT1, o usar los niveles de CCDC3 como señal de alerta de enfermedad agresiva, podría algún día ayudar a prevenir o tratar las metástasis hepáticas del cáncer colorrectal.
Cita: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Palabras clave: cáncer colorrectal, metástasis hepática, microambiente tumoral, inestabilidad cromosómica, fibroblastos asociados al cáncer