Clear Sky Science · sv
Kombinera AI för att avslöja CCDC3-medierade vägar vid levermetastaser från kolorektal cancer
Varför denna forskning är viktig
Kolorektal cancer är en av de vanligaste cancerformerna i världen, och många dödsfall inträffar först efter att sjukdomen spridit sig till levern. Kliniker vet att tumörer med hög kromosomal instabilitet tenderar att vara mer aggressiva och svårare att behandla, men det har varit oklart hur de omgivande icke-cancerösa cellerna bidrar till att driva tumörer mot detta farliga tillstånd. Denna studie avslöjar en dold kommunikationslinje mellan stödjeceller runt tumören och cancerceller, som pekar på en kedja av händelser som skapar genetiskt kaos och driver levermetastaser — och som pekar på nya sätt att stoppa det.
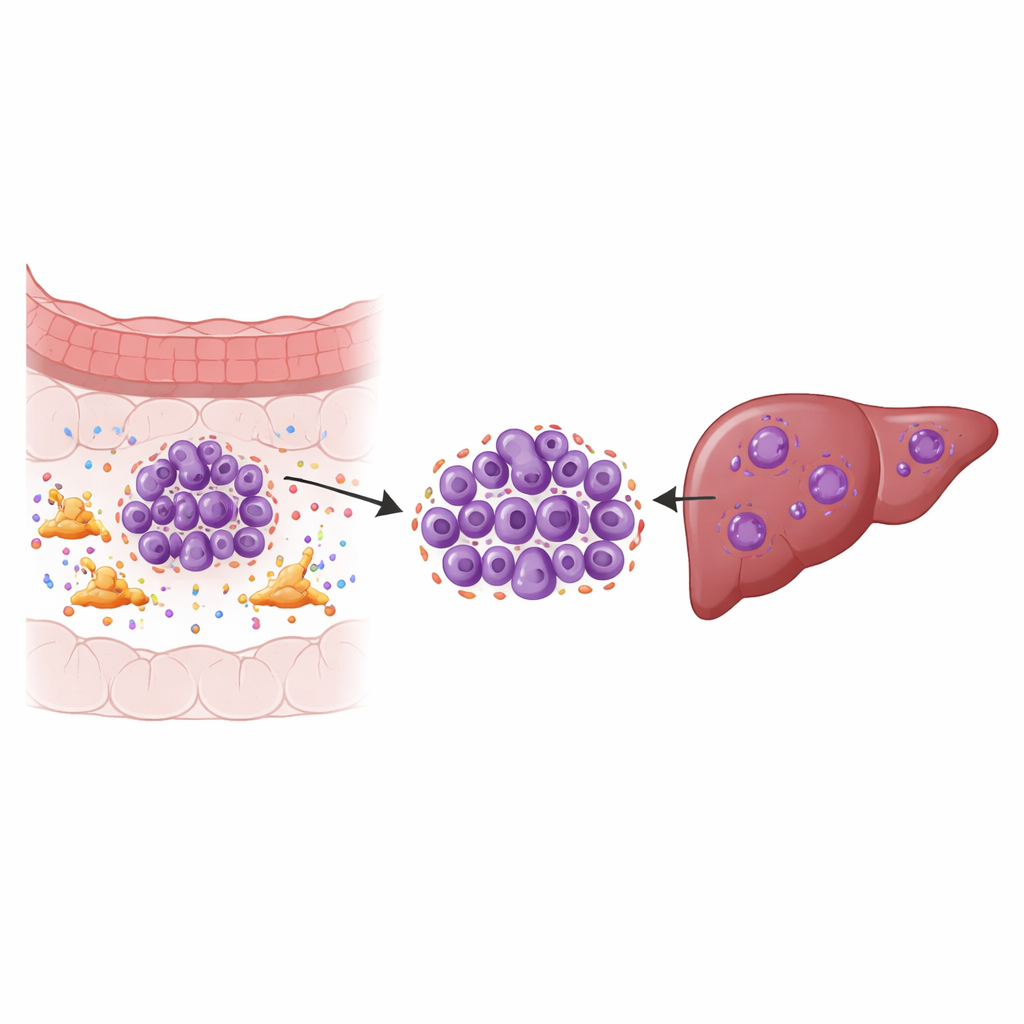
De dolda hjälparna runt tumören
Solida tumörer är inte bara klumpar av cancerceller; de är ekosystem. En viktig invånare i detta ekosystem är cancerassocierade fibroblaster, en typ av bindvävscell som omformar området runt tumören och utsöndrar många signalmolekyler. Genom att använda enkelcells-RNA-sekvensering på prover från primära kolorektala tumörer, matchande levermetastaser, närliggande normalvävnad och blod kartlade forskarna nio huvudcelltyper och zoomade sedan in på cancercellerna själva. De upptäckte specifika tumörundergrupper i levern som visade tydliga tecken på kromosomal instabilitet — frekventa fel i hur kromosomer kopieras och delas — vilket är kopplat till snabb tillväxt, behandlingsresistens och sämre överlevnad.
En numerisk poäng för farliga tumörceller
För att förstå vilka cancerformer som är mest i riskzonen byggde gruppen ett sammansatt ”instabilitetsindex” som fångade flera bevislager: genuttrycksmönster, härledda förändringar i kromosomantal och kända instabilitetsrelaterade gener. Tumörceller med höga poäng var betydligt vanligare i levermetastaser än i primära tumörer. Dessa högt indexerade celler visade en överaktiv cellcykel, mer DNA-skada och reparationsaktivitet samt egenskaper förknippade med invasion och spridning. Med andra ord, ju mer instabila kromosomerna var, desto mer aggressiva och anpassningsbara framstod cancercellerna — vilket stöder idén att instabilitet inte bara är en bieffekt av cancer utan en drivkraft för dess progression.
En hemlig signal från fibroblaster
Nästa fråga var vad i tumörmiljön som kunde driva cancerceller mot detta instabila tillstånd. Genom att analysera hur olika celltyper "pratar" med varandra via signalmolekyler fann forskarna särskilt stark kommunikation mellan fibroblaster och de kromosomalt instabila tumörcellerna. En särskild grupp fibroblaster var förhöjd i levermetastaser och kopplad till sämre patientöverlevnad. När generna som var aktiva i dessa fibroblaster jämfördes med dem i instabilitets‑höga cancerceller framträdde en gen: CCDC3, ett litet studerat protein som huvudsakligen producerades av fibroblaster och var mycket mer rikligt i leverlesioner än i primära tumörer. Patienter vars tumörer hade högre nivåer av CCDC3 tenderade att ha kortare överlevnad, vilket tyder på att denna signal kan vara en nyckelfaktor för aggressiv sjukdom.
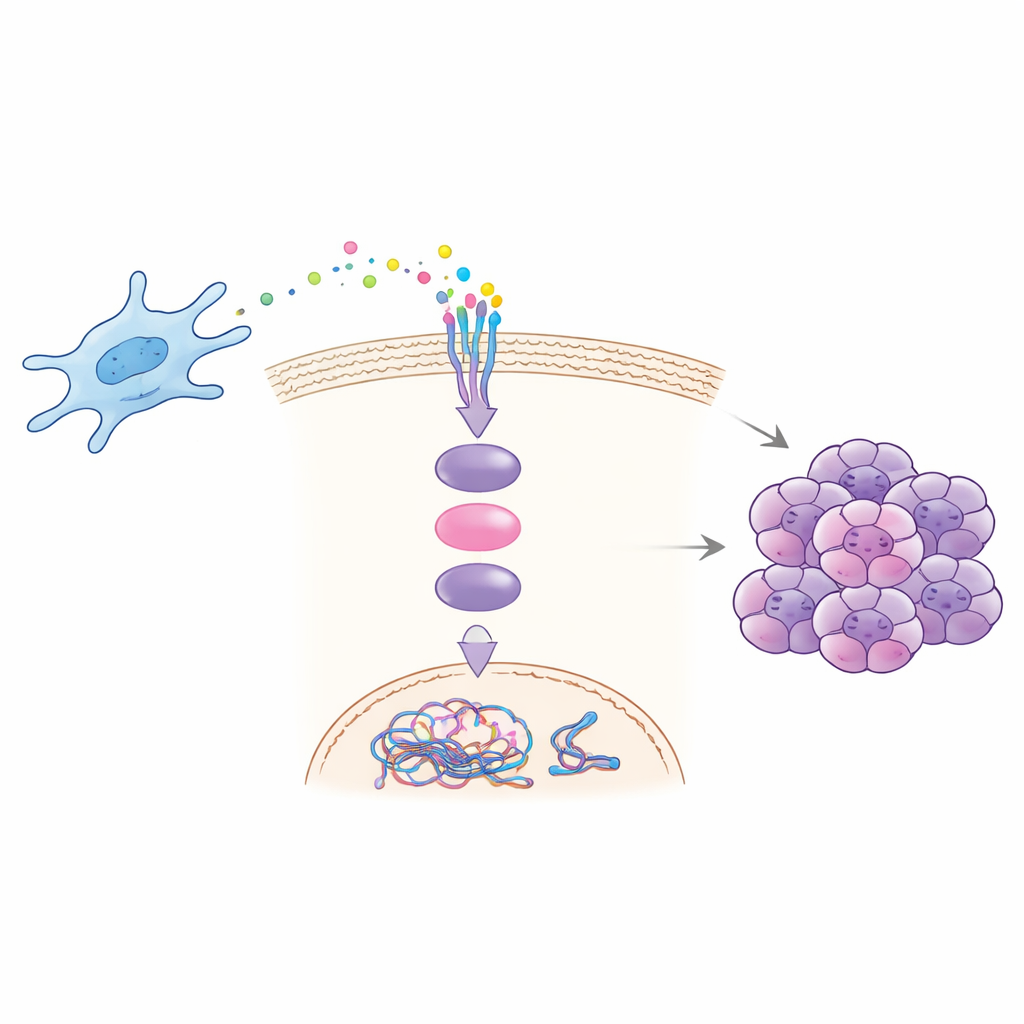
Hur en signal utlöser en kedjereaktion
Laboratorie- och djurexperiment visade hur CCDC3 driver malignitet. Fibroblaster tagna från levermetastaser utsöndrade mer CCDC3 och när de odlades tillsammans med cancerceller ökade de cancercellernas förmåga att migrera, invadera, bilda kolonier och uppvisa tecken på kromosomal instabilitet. Tillsats av renat CCDC3 till cancerceller reproducerade dessa effekter, medan blockering av CCDC3 i fibroblaster minskade dem. Forskarna visade att CCDC3 binder till en receptor kallad CXCR3 på cancerceller, vilket sedan aktiverar ett välkänt budbärarprotein inne i cellen, STAT3. När STAT3 aktiveras färdas det till kärnan och ökar direkt produktionen av CDT1, ett protein som hjälper till att reglera DNA-replikationens start. Överskott av CDT1 rubbar den normala tidpunkten och noggrannheten i DNA-kopieringen, vilket främjar kromosomfel och instabilitet.
Från mekanism till potentiell behandling
Genom att selektivt blockera varje steg i denna kedja — CCDC3, CXCR3, STAT3 eller CDT1 — kunde forskarna dämpa cancercellernas invasiva beteende och tillväxt i odlingsskålar och i musmodeller. Möss som fick extra CCDC3 utvecklade större tumörer och fler levermetastaser, medan de som behandlades med en antikropp mot CCDC3 eller en STAT3-hämmare hade långsammare tumörtillväxt och färre leverlesioner. Dessa fynd definierar en tydlig fibroblast-till-tumör signalväg som länkar tumörmiljön till internt genetiskt kaos i cancerceller. För patienter antyder detta att inriktning på CCDC3–CXCR3–STAT3–CDT1-axeln, eller att använda CCDC3-nivåer som en varningsmarkör för aggressiv sjukdom, en dag kan hjälpa till att förebygga eller behandla levermetastaser från kolorektal cancer.
Citering: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Nyckelord: kolorektal cancer, levermetastaser, tumörmikromiljö, kromosomal instabilitet, cancerassocierade fibroblaster