Clear Sky Science · pl
Łączenie SI w celu ujawnienia ścieżek pośredniczonych przez CCDC3 w przerzutach raka jelita grubego do wątroby
Dlaczego te badania są istotne
Rak jelita grubego jest jednym z najczęstszych nowotworów na świecie, a wiele zgonów następuje dopiero po rozsianiu choroby do wątroby. Lekarze wiedzą, że guzy o wysoce niestabilnych chromosomach mają tendencję do większej agresywności i są trudniejsze w leczeniu, jednak nie było jasne, w jaki sposób otaczające komórki niebędące nowotworowymi przyczyniają się do osiągnięcia tego niebezpiecznego stanu. To badanie ujawnia ukryty kanał komunikacji między komórkami wspierającymi guz a komórkami nowotworowymi, odkrywając łańcuch zdarzeń, który napędza chaos genetyczny i sprzyja przerzutom do wątroby — oraz wskazując nowe sposoby jego zatrzymania.
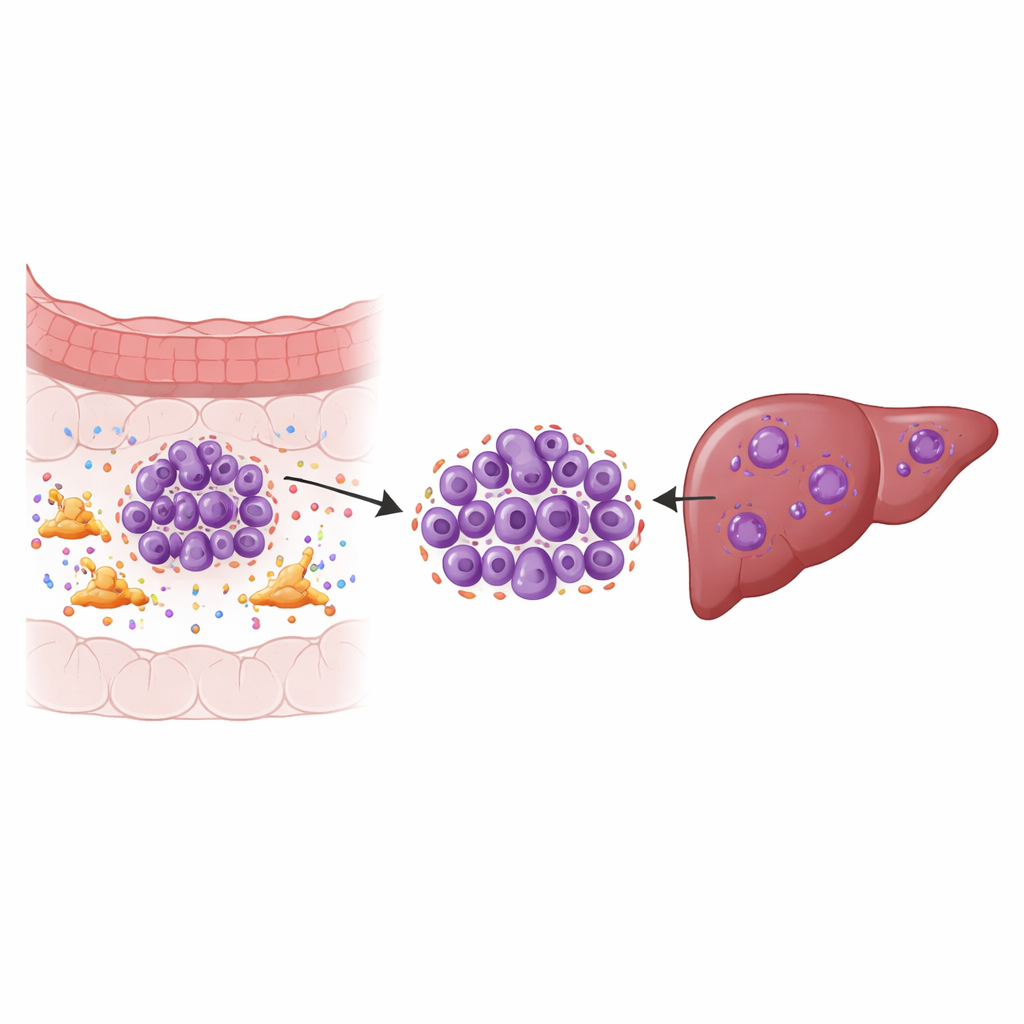
Ukryci pomocnicy wokół guza
Guzy lity nie są jedynie zbitkami komórek nowotworowych; są ekosystemami. Jednym z kluczowych mieszkańców tego ekosystemu są fibroblasty związane z rakiem, typ komórek tkanki łącznej, które przebudowują otoczenie guza i wydzielają liczne molekuły sygnałowe. Wykorzystując sekwencjonowanie RNA pojedynczych komórek w próbkach z pierwotnych guzów jelita grubego, odpowiadających przerzutów do wątroby, pobliskich tkanek prawidłowych i krwi, badacze zmapowali dziewięć głównych typów komórek, a następnie skupili się na samych komórkach nowotworowych. Odkryli specyficzne podgrupy guzów w wątrobie wykazujące silne oznaki niestabilności chromosomalnej — częste błędy w kopiowaniu i podziale chromosomów — co wiąże się z szybkim wzrostem, opornością na leczenie i słabym przeżyciem.
Liczbowy wskaźnik dla niebezpiecznych komórek guza
Aby zrozumieć, które nowotwory są najbardziej zagrożone, zespół opracował złożony „wskaźnik niestabilności”, który odzwierciedlał wiele poziomów dowodów: wzorce ekspresji genów, wnioskowane zmiany liczby kopii chromosomów oraz znane geny związane z niestabilnością. Komórki nowotworowe o wysokich wynikach były znacznie częstsze w przerzutach wątroby niż w guzach pierwotnych. Komórki o wysokim wskaźniku wykazywały nadaktywność cyklu komórkowego, większe uszkodzenia DNA i aktywność naprawczą oraz cechy związane z inwazją i rozsiewem. Innymi słowy, im bardziej niestabilne chromosomy, tym bardziej agresywne i plastyczne wydawały się komórki nowotworowe — co wspiera pogląd, że niestabilność nie jest tylko efektem ubocznym raka, lecz napędem jego postępu.
Tajny sygnał od fibroblastów
Następne pytanie brzmiało: co w mikrośrodowisku guza może popychać komórki nowotworowe ku temu niestabilnemu stanowi. Analizując, jak różne typy komórek „rozmawiają” ze sobą poprzez molekuły sygnałowe, badacze znaleźli szczególnie silną komunikację między fibroblastami a komórkami nowotworowymi z niestabilnymi chromosomami. Okazała się pewna grupa fibroblastów wzbogacona w przerzutach wątroby i związana z gorszym przeżyciem pacjentów. Porównanie genów aktywnych w tych fibroblastach z genami w komórkach nowotworowych o wysokiej niestabilności wyodrębniło jeden wyróżniający się: CCDC3, słabo poznane białko produkowane głównie przez fibroblasty, znacznie bardziej obfite w zmianach wątrobowych niż w guzach pierwotnych. Pacjenci, których guzy miały wyższe poziomy CCDC3, mieli tendencję do krótszego przeżycia, co sugeruje, że ten sygnał może być kluczowym promotorem agresywnej choroby.
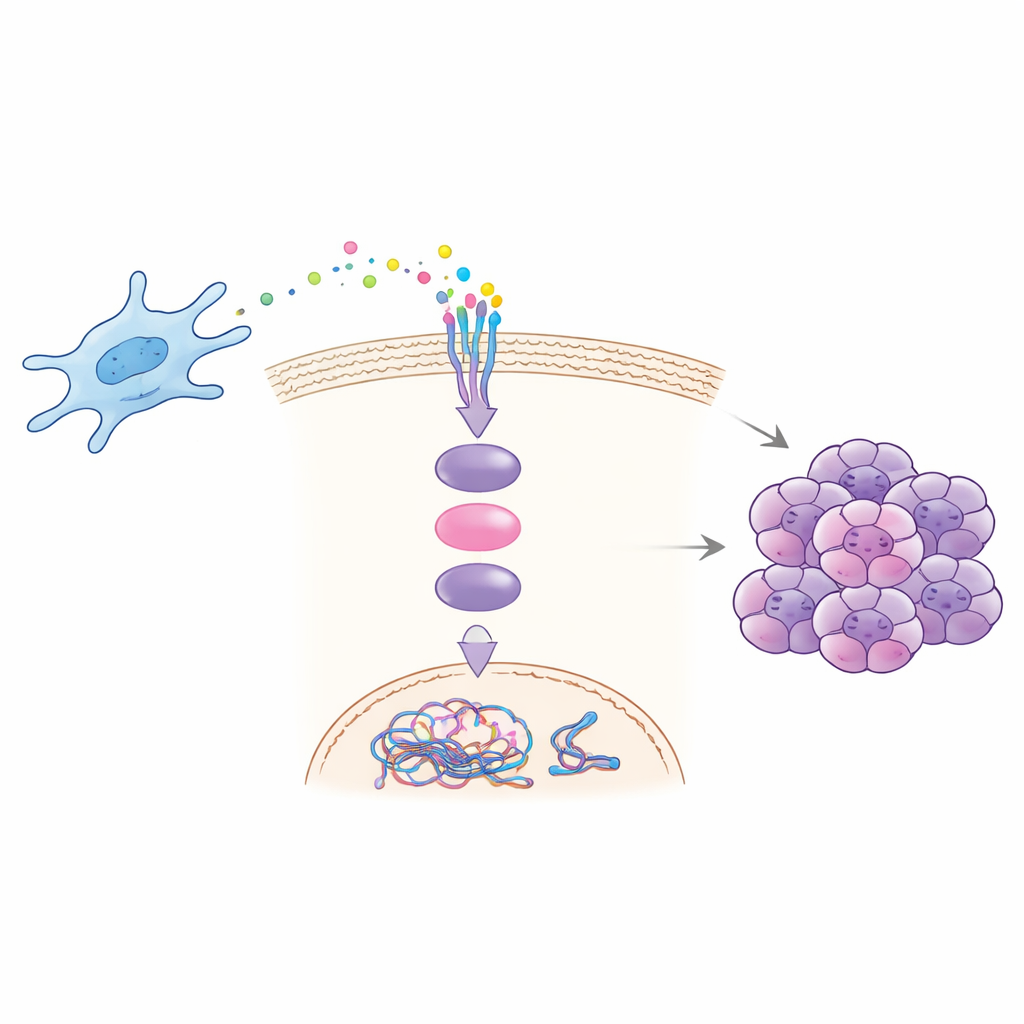
Jak jeden sygnał uruchamia reakcję łańcuchową
Badania laboratoryjne i na zwierzętach ujawniły, jak CCDC3 napędza złośliwość. Fibroblasty pobrane z przerzutów wątroby wydzielały więcej CCDC3 i w hodowlach współkulturowych z komórkami nowotworowymi zwiększały ich zdolność do migracji, inwazji, formowania kolonii oraz przejawiania cech niestabilności chromosomalnej. Dodanie oczyszczonego CCDC3 do komórek nowotworowych odtworzyło te efekty, podczas gdy blokowanie CCDC3 w fibroblastach je osłabiło. Zespół wykazał, że CCDC3 wiąże się z receptorem o nazwie CXCR3 na komórkach nowotworowych, co następnie aktywuje znany białkowy przekaźnik wewnątrzkomórkowy, STAT3. Po aktywacji STAT3 przemieszcza się do jądra i bezpośrednio zwiększa produkcję CDT1, białka uczestniczącego w licencjonowaniu replikacji DNA. Nadmiar CDT1 zaburza prawidłowe tempo i dokładność kopiowania DNA, sprzyjając błędom chromosomalnym i niestabilności.
Od mechanizmu do potencjalnego leczenia
Poprzez selektywne blokowanie każdego etapu tego łańcucha — CCDC3, CXCR3, STAT3 lub CDT1 — badacze byli w stanie osłabić inwazyjne zachowanie i wzrost komórek nowotworowych w hodowlach oraz w modelach mysich. Myszy otrzymujące dodatkowe CCDC3 rozwijały większe guzy i więcej przerzutów do wątroby, podczas gdy te leczone przeciwciałem przeciw CCDC3 lub inhibitorem STAT3 miały wolniejszy wzrost guza i mniej zmian wątrobowych. Wyniki te definiują jasną ścieżkę sygnalizacji od fibroblastów do guza, która łączy mikrośrodowisko guza z wewnętrznym chaosem genetycznym w komórkach nowotworowych. Dla pacjentów praca ta sugeruje, że ukierunkowanie osi CCDC3–CXCR3–STAT3–CDT1 lub użycie poziomów CCDC3 jako sygnału ostrzegawczego przed agresywną chorobą mogłoby pewnego dnia pomóc w zapobieganiu lub leczeniu przerzutów raka jelita grubego do wątroby.
Cytowanie: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Słowa kluczowe: rak jelita grubego, przerzuty do wątroby, mikrośrodowisko guza, niestabilność chromosomalna, fibroblasty związane z rakiem