Clear Sky Science · nl
Combinatie van AI onthult CCDC3-gemedieerde paden van levermetastasen bij colorectale kanker
Waarom dit onderzoek ertoe doet
Colorectale kanker is een van de meest voorkomende vormen van kanker wereldwijd, en veel sterfgevallen doen zich pas voor nadat de ziekte naar de lever is uitgezaaid. Artsen weten dat tumoren met sterk instabiele chromosomen doorgaans agressiever zijn en moeilijker te behandelen, maar het was onduidelijk hoe de omliggende niet-kankercellen bijdragen aan het duwen van tumoren naar die gevaarlijke staat. Deze studie legt een verborgen communicatielijn bloot tussen ondersteunende cellen rond de tumor en de kankercellen, en onthult een keten van gebeurtenissen die genetische chaos aanwakkert en levermetastasen voedt — en wijst op nieuwe manieren om dat te stoppen.
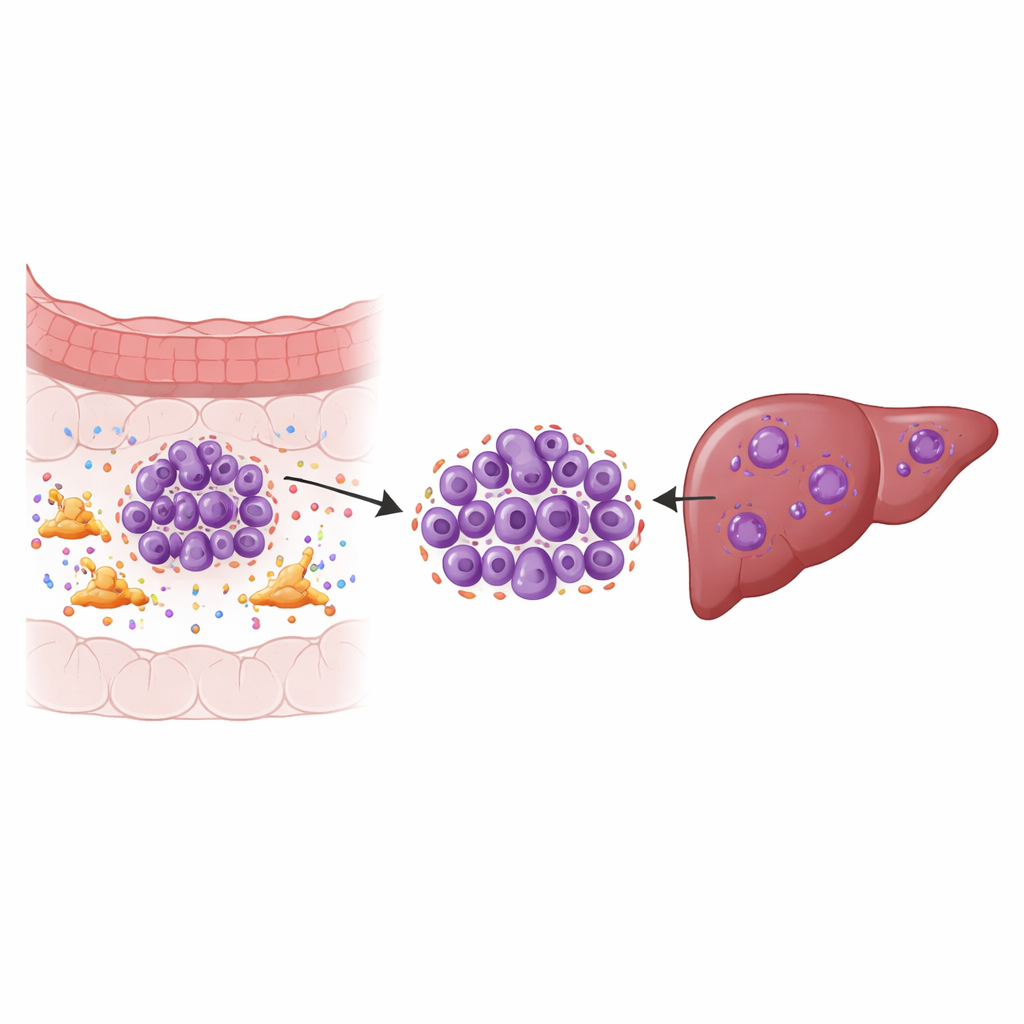
De verborgen helpers rond de tumor
Solide tumoren zijn niet slechts hoopjes kankercellen; het zijn ecosystemen. Een belangrijke bewoner van dit ecosysteem is de kanker-geassocieerde fibroblast, een type bindweefselcel die het gebied rond de tumor herstructureert en veel signaalmoleculen afscheidt. Met single-cell RNA-sequencing van monsters uit primaire colorectale tumoren, bijpassende levermetastasen, nabijgelegen normaal weefsel en bloed, brachten de onderzoekers negen belangrijke celtypen in kaart en zoemden daarna in op de kankercellen zelf. Ze ontdekten specifieke tumorsubgroepen in de lever die sterke tekenen van chromosomale instabiliteit vertoonden — frequente fouten bij het kopiëren en verdelen van chromosomen — wat samenhangt met snelle groei, therapieresistentie en slechte overleving.
Een numerieke score voor gevaarlijke tumorcellen
Om te begrijpen welke kankers het meest risico lopen, bouwde het team een samengestelde “instabiliteitsindex” die meerdere lagen bewijs vastlegde: genexpressiepatronen, afgeleide veranderingen in het aantal chromosoomkopieën en bekende instabiliteitsgerelateerde genen. Tumorcellen met hoge scores kwamen veel vaker voor in levermetastasen dan in primaire tumoren. Deze cellen met een hoge index vertoonden een overactieve celdeling, meer activiteit rond DNA-schade en -herstel, en kenmerken die samenhangen met invasie en verspreiding. Met andere woorden: hoe instabieler de chromosomen, hoe agressiever en aanpasbaarder de kankercellen leken — wat de idee ondersteunt dat instabiliteit niet slechts een bijproduct van kanker is, maar een drijvende kracht achter de progressie ervan.
Een geheim signaal van fibroblasten
De volgende vraag was wat in de tumoromgeving de kankercellen in deze instabiele richting duwt. Door te analyseren hoe verschillende celtypen met elkaar “praten” via signaalmoleculen, vonden de onderzoekers vooral sterke communicatie tussen fibroblasten en de chromosomaal instabiele tumorcellen. Een specifieke groep fibroblasten was verrijkt in levermetastasen en gekoppeld aan slechtere overleving van patiënten. Toen de genen die actief zijn in deze fibroblasten werden vergeleken met die in instabiliteit-hoge kankercellen, stak er één gen bovenuit: CCDC3, een weinig bestudeerd eiwit dat voornamelijk door fibroblasten werd geproduceerd en veel overvloediger voorkwam in leverletsels dan in primaire tumoren. Patiënten van wie de tumoren hogere CCDC3-niveaus hadden, leefden gemiddeld korter, wat suggereert dat dit signaal een belangrijke bevorderaar van agressieve ziekte zou kunnen zijn.
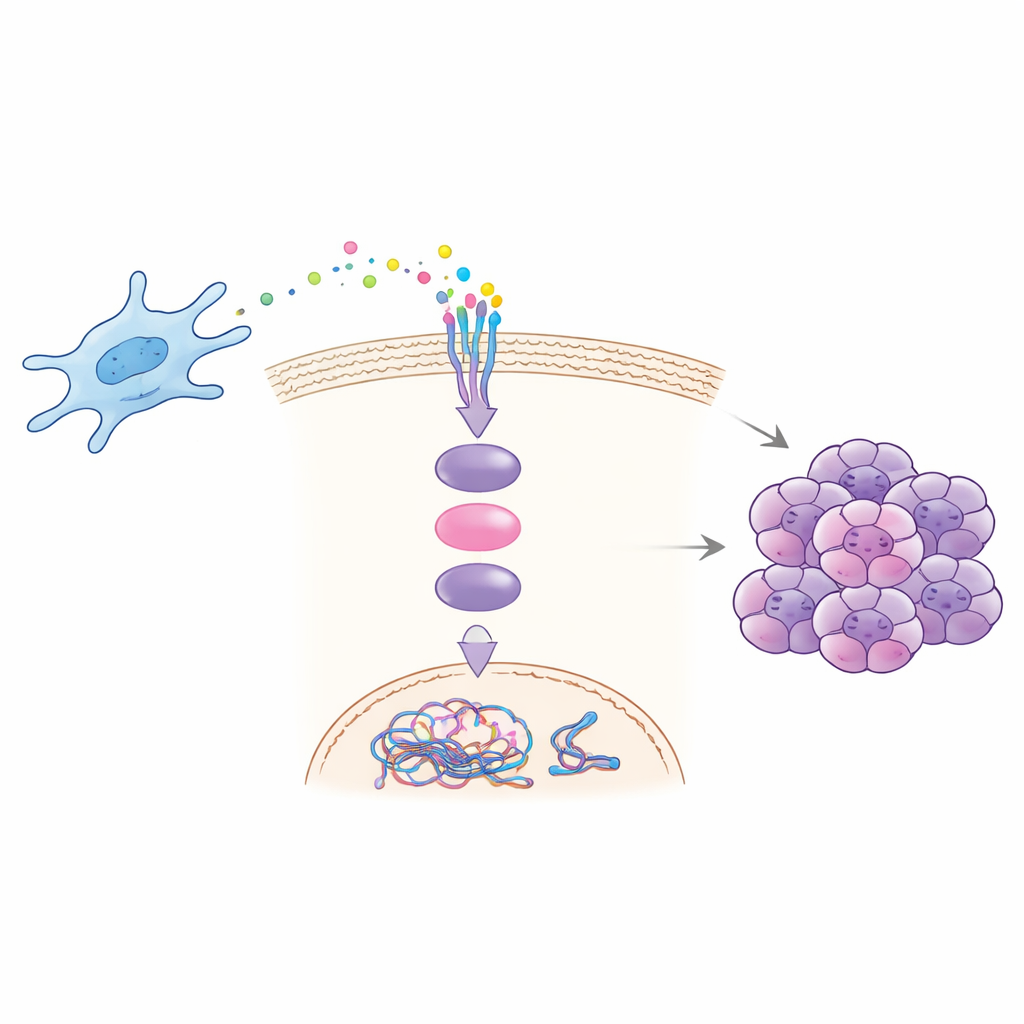
Hoe één signaal een kettingreactie veroorzaakt
Laboratorium- en proefdierexperimenten lieten zien hoe CCDC3 maligniteit stimuleert. Fibroblasten afkomstig uit levermetastasen scheidden meer CCDC3 af en verhoogden, wanneer ze samen met kankercellen werden gekweekt, het vermogen van die kankercellen om te migreren, invaderen, kolonies te vormen en tekenen van chromosomale instabiliteit te vertonen. Het toevoegen van gepurificeerd CCDC3 aan kankercellen reproduceerde deze effecten, terwijl het blokkeren van CCDC3 in fibroblasten ze verminderde. Het team toonde aan dat CCDC3 bindt aan een receptor genaamd CXCR3 op kankercellen, die vervolgens een bekend boodschapper-eiwit binnen de cel activeert: STAT3. Eenmaal geactiveerd reist STAT3 naar de kern en verhoogt direct de productie van CDT1, een eiwit dat helpt bij het 'licenseren' van DNA-replicatie. Overmaat aan CDT1 verstoort de normale timing en nauwkeurigheid van DNA-kopieën, wat chromosoomfouten en instabiliteit bevordert.
Van mechanisme naar potentiële behandeling
Door elke stap in deze keten selectief te blokkeren — CCDC3, CXCR3, STAT3 of CDT1 — konden de onderzoekers het invasieve gedrag en de groei van kankercellen in kweek en in muismodellen verminderen. Muizen die extra CCDC3 kregen ontwikkelden grotere tumoren en meer levermetastasen, terwijl muizen die werden behandeld met een antilichaam tegen CCDC3 of een STAT3-remmer tragere tumorgroei en minder leverletsels hadden. Deze bevindingen definiëren een duidelijke fibroblast-naar-tumor signaalroute die de tumoromgeving koppelt aan interne genetische chaos in kankercellen. Voor patiënten suggereert dit werk dat het richten op de CCDC3–CXCR3–STAT3–CDT1-as, of het gebruik van CCDC3-niveaus als waarschuwingsteken voor agressieve ziekte, ooit zou kunnen helpen bij het voorkomen of behandelen van levermetastasen van colorectale kanker.
Bronvermelding: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Trefwoorden: colorectale kanker, levermetastasen, tumormicro-omgeving, chromosomale instabiliteit, kanker-geassocieerde fibroblasten