Clear Sky Science · ar
الجمع بين الذكاء الاصطناعي لكشف المسارات التي يتوسطها CCDC3 في نقائل سرطان القولون والمستقيم إلى الكبد
لماذا يهم هذا البحث
يعد سرطان القولون والمستقيم واحدًا من أكثر السرطانات شيوعًا عالميًا، وتحدث العديد من الوفيات بعد انتشار المرض إلى الكبد. يعرف الأطباء أن الأورام ذات الكروموسومات شديدة عدم الاستقرار تميل لأن تكون أكثر عدوانية وأكثر صعوبة في العلاج، لكن ظل غامضًا كيف تسهم الخلايا غير السرطانية المحيطة في دفع الأورام إلى هذه الحالة الخطيرة. يكشف هذا البحث عن خط اتصال مخفي بين خلايا الدعم حول الورم وخلايا السرطان، موضحًا سلسلة من الأحداث التي تدفع إلى الفوضى الجينية وتغذي نقائل الكبد—ومشيرًا إلى طريق جديد لوقفها.
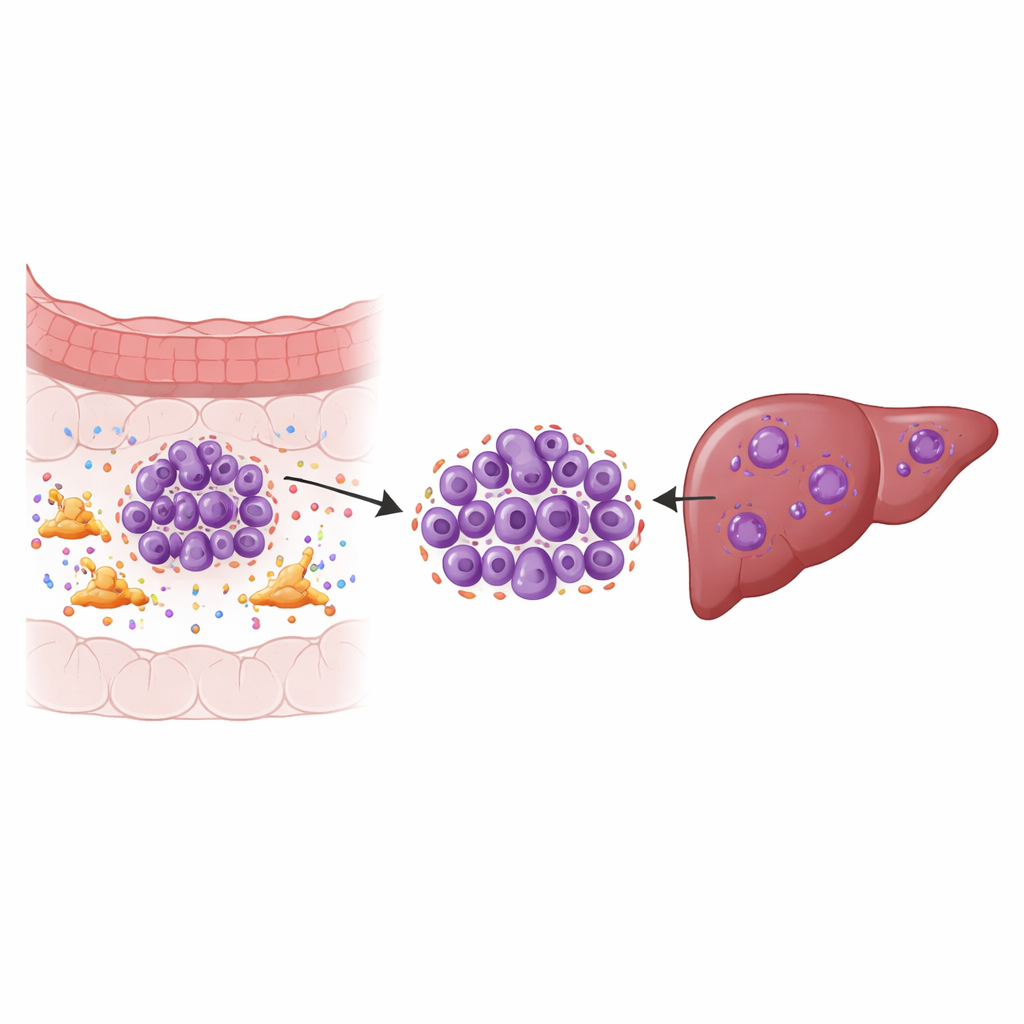
المساعدون الخفيون حول الورم
الأورام الصلبة ليست مجرد مجموعات من الخلايا السرطانية؛ إنها أنظمة بيئية. أحد عناصر هذا النظام هو الخلايا الليفية المرتبطة بالسرطان، وهي نوع من خلايا النسيج الضام التي تعيد تشكيل المنطقة حول الورم وتفرز العديد من جزيئات الإشارة. باستخدام تسلسل RNA أحادي الخلية على عينات من أورام القولون والمستقيم الأولية، ونقائلها المتطابقة في الكبد، والأنسجة السليمة المجاورة، والدم، رسم الباحثون خريطة لتسعة أنواع خلوية رئيسية ثم ركزوا على الخلايا السرطانية نفسها. اكتشفوا مجموعات ورمية محددة في الكبد أظهرت علامات قوية لعدم الاستقرار الكروموسومي—أخطاء متكررة في كيفية نسخ وتقسيم الكروموسومات—وهو ما يرتبط بنمو سريع ومقاومة للعلاج وبقاء ضعيف.
مؤشر رقمي للخلايا الورمية الخطرة
لفهم أي السرطانات في خطر أكبر، بنى الفريق «مؤشر عدم الاستقرار» مركبًا يجمع طبقات متعددة من الأدلة: أنماط التعبير الجيني، والتغيرات المستنتجة في عدد نسخ الكروموسومات، وجينات معروفة مرتبطة بعدم الاستقرار. كانت الخلايا الورمية ذات الدرجات العالية أكثر شيوعًا بكثير في نقائل الكبد مقارنةً بالأورام الأولية. أظهرت هذه الخلايا ذات المؤشر العالي دورة خلوية مفرطة النشاط، ومزيدًا من نشاط تلف الحمض النووي وإصلاحه، وسمات مرتبطة بالغزو والانتشار. بعبارة أخرى، كلما زاد عدم استقرار الكروموسومات، بدا أن الخلايا السرطانية أكثر عدوانية وقابلية للتكيف—مما يدعم الفكرة بأن عدم الاستقرار ليس مجرد أثر جانبي للسرطان، بل محرك لتقدمه.
إشارة سرية من الخلايا الليفية
كان السؤال التالي ما الذي في بيئة الورم قد يدفع الخلايا السرطانية نحو هذه الحالة غير المستقرة. من خلال تحليل كيفية «تحدث» الأنواع الخلوية المختلفة مع بعضها عبر جزيئات الإشارة، وجد الباحثون تواصلًا قويًا بشكل خاص بين الخلايا الليفية والخلايا الورمية ذات عدم الاستقرار الكروموسومي. كانت مجموعة معينة من الخلايا الليفية معززة في نقائل الكبد ومرتبطة ببقاء أسوأ للمرضى. عند مقارنة الجينات النشطة في هذه الخلايا الليفية مع تلك في الخلايا السرطانية ذات المؤشر العالي لعدم الاستقرار، برز جين واحد: CCDC3، وهو بروتين قليل الدراسة يُنتج بشكل رئيسي بواسطة الخلايا الليفية وكان أكثر وفرة بكثير في الآفات الكبدية مقارنةً بالأورام الأولية. صاح المرضى الذين كانت أورامهم تحتوي على مستويات أعلى من CCDC3 بفترة بقاء أقصر، مما يوحي بأن هذه الإشارة قد تكون محفزًا رئيسيًا للمرض العدواني.
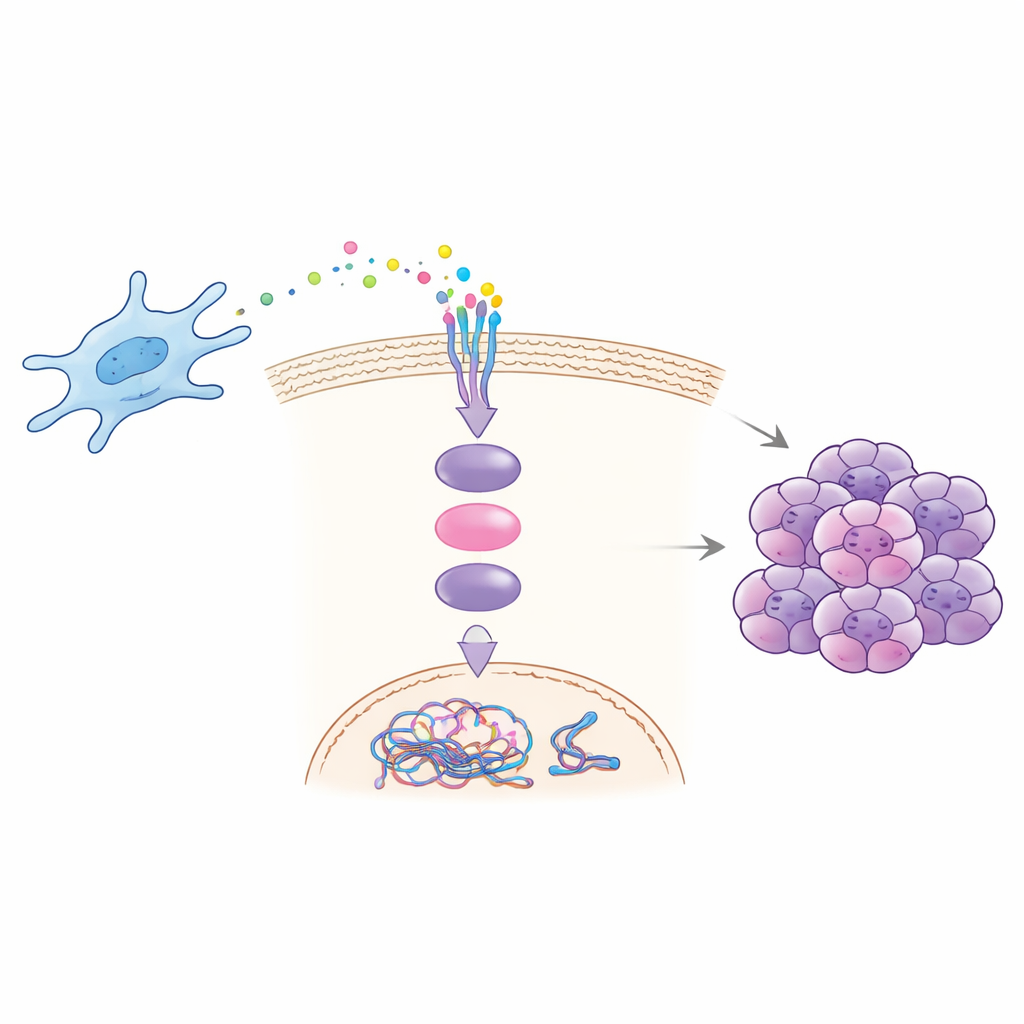
كيف تطلق إشارة واحدة سلسلة تفاعلات
كشفت تجارب مخبرية وعلى الحيوانات كيف يقود CCDC3 الخباثة. الخلايا الليفية المأخوذة من نقائل الكبد أفرزت المزيد من CCDC3 وعند زراعتها مع الخلايا السرطانية عززت قدرة الخلايا السرطانية على الهجرة والغزو وتشكيل المستعمرات وإظهار علامات عدم الاستقرار الكروموسومي. إعادة إضافة CCDC3 المنقى إلى الخلايا السرطانية أعادت إنتاج هذه التأثيرات، بينما أدى حجب CCDC3 في الخلايا الليفية إلى تقليلها. أظهر الفريق أن CCDC3 يرتبط بمستقبل يُدعى CXCR3 على الخلايا السرطانية، والذي ينشط بعد ذلك بروتين رسول معروف داخل الخلية، STAT3. عند تفعيله، ينتقل STAT3 إلى النواة ويزيد مباشرة من إنتاج CDT1، وهو بروتين يساعد على ترخيص تكرار الحمض النووي. يؤدي فائض CDT1 إلى تعطيل التوقيت والدقة الطبيعيين لنسخ الحمض النووي، مما يعزز أخطاء الكروموسومات وعدم الاستقرار.
من الآلية إلى العلاج المحتمل
من خلال حجب كل خطوة من هذه السلسلة بشكل انتقائي—CCDC3 أو CXCR3 أو STAT3 أو CDT1—تمكن الباحثون من تقليص سلوك الغزو ونمو الخلايا السرطانية في أطباق وزراعات حيوانية. طورت الفئران التي أعطيت CCDC3 إضافيًا أورامًا أكبر ومزيدًا من نقائل الكبد، بينما كانت الفئران المعالجة بأجسام مضادة ضد CCDC3 أو بمثبط STAT3 تُظهر نموًا أبطأ للأورام وقلة في الآفات الكبدية. تحدد هذه النتائج مسار إشارة واضحًا من الخلايا الليفية إلى الورم يربط بين بيئة الورم والفوضى الجينية الداخلية في الخلايا السرطانية. وللمرضى، يشير هذا العمل إلى أن استهداف محور CCDC3–CXCR3–STAT3–CDT1، أو استخدام مستويات CCDC3 كعلامة تحذيرية للمرض العدواني، قد يساعد يومًا ما في منع أو علاج نقائل الكبد الناجمة عن سرطان القولون والمستقيم.
الاستشهاد: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
الكلمات المفتاحية: سرطان القولون والمستقيم, نقائل الكبد, البيئة الميكروية للورم, عدم استقرار كروموسومي, الخلايا الليفية المرتبطة بالسرطان