Clear Sky Science · de
KI-Kombination zur Aufdeckung CCDC3-vermittelter Signalwege bei Lebermetastasen kolorektaler Karzinome
Warum diese Forschung wichtig ist
Kolorektales Karzinom gehört zu den weltweit häufigsten Krebserkrankungen, und viele Todesfälle treten erst auf, nachdem sich die Krankheit in die Leber ausgebreitet hat. Ärztinnen und Ärzte wissen, dass Tumoren mit stark instabilen Chromosomen tendenziell aggressiver sind und schlechter behandelbar, doch lange war unklar, wie die umliegenden nicht‑tumorösen Zellen die Tumoren in diesen gefährlichen Zustand treiben. Diese Studie deckt eine bisher verborgene Kommunikationsachse zwischen den Stützzellen rund um den Tumor und den Krebszellen auf, beschreibt eine Abfolge von Ereignissen, die genetisches Chaos vorantreibt und Lebermetastasen befeuert — und zeigt mögliche Ansatzpunkte, um diesen Prozess zu stoppen.
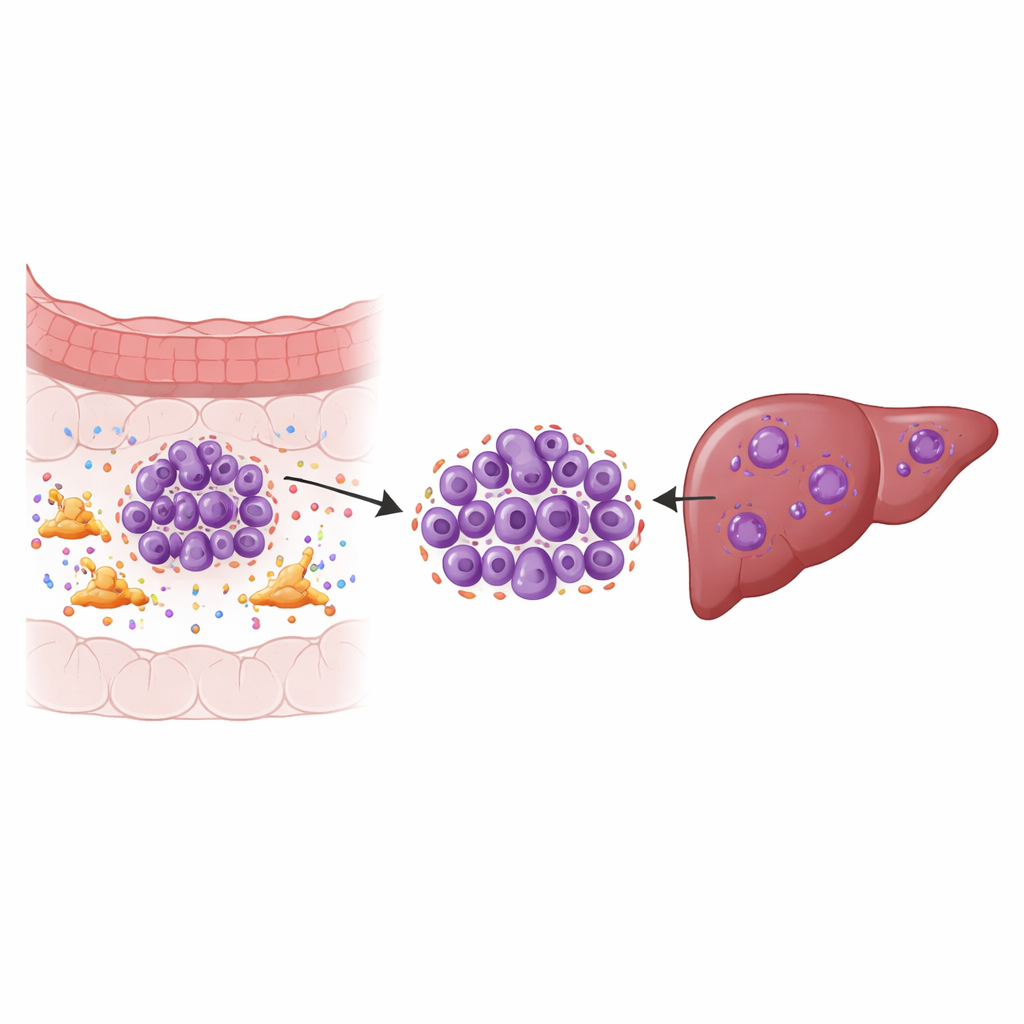
Die verborgenen Helfer um den Tumor
Feste Tumoren sind nicht nur Ansammlungen von Krebszellen; sie sind Ökosysteme. Ein zentraler Bewohner dieses Ökosystems sind tumorassoziierte Fibroblasten, eine Art Bindegewebszellen, die das Umfeld des Tumors umbauen und zahlreiche Signalmoleküle ausschütten. Anhand von Einzelzell‑RNA‑Sequenzierung an Proben aus Primärtumoren des Kolons, den passenden Lebermetastasen, benachbarter normaler Gewebe und Blut kartierten die Forschenden neun Hauptzelltypen und untersuchten dann die Tumorzellen im Detail. Sie identifizierten bestimmte Tumoruntergruppen in der Leber, die deutliche Anzeichen chromosomaler Instabilität zeigten — häufige Fehler bei Kopie und Aufteilung von Chromosomen —, was mit schnellem Wachstum, Therapieresistenz und schlechter Überlebensprognose verbunden ist.
Ein numerischer Index für gefährliche Tumorzellen
Um zu bestimmen, welche Tumoren am stärksten gefährdet sind, entwickelten die Forschenden einen zusammengesetzten „Instabilitätsindex“, der mehrere Evidenzschichten erfasste: Genexpressionsmuster, inferierte Veränderungen der Chromosomenkopienzahl und bekannte Instabilitäts‑assoziierte Gene. Tumorzellen mit hohen Werten traten in Lebermetastasen deutlich häufiger auf als in Primärtumoren. Diese Hoch‑Index‑Zellen zeigten einen überaktiven Zellzyklus, verstärkte Aktivität von DNA‑Schadens‑ und Reparaturmechanismen sowie Merkmale, die mit Invasion und Ausbreitung assoziiert sind. Anders gesagt: Je instabiler die Chromosomen, desto aggressiver und anpassungsfähiger erschienen die Krebszellen — was die Vorstellung stützt, dass Instabilität nicht nur eine Begleiterscheinung, sondern ein Treiber des Fortschreitens ist.
Ein geheimes Signal der Fibroblasten
Die nächste Frage war, was in der Tumorumgebung die Krebszellen in diesen instabilen Zustand treiben könnte. Durch die Analyse, wie verschiedene Zelltypen über Signalmoleküle „miteinander sprechen“, fanden die Forschenden besonders starke Kommunikation zwischen Fibroblasten und den chromosomal instabilen Tumorzellen. Eine bestimmte Fibroblasten‑Untergruppe war in Lebermetastasen angereichert und mit schlechterem Patient*innenüberleben verbunden. Beim Vergleich der in diesen Fibroblasten aktiven Gene mit denen der Instabilitäts‑hohen Krebszellen stach ein Gen hervor: CCDC3, ein bisher wenig untersuchtes Protein, das hauptsächlich von Fibroblasten produziert wurde und in Leberherden deutlich häufiger vorkam als in Primärtumoren. Patientinnen und Patienten mit höheren CCDC3‑Werten in ihren Tumoren hatten tendenziell eine kürzere Überlebenszeit, was darauf hindeutet, dass dieses Signal ein zentraler Förderer aggressiven Verhaltens sein könnte.
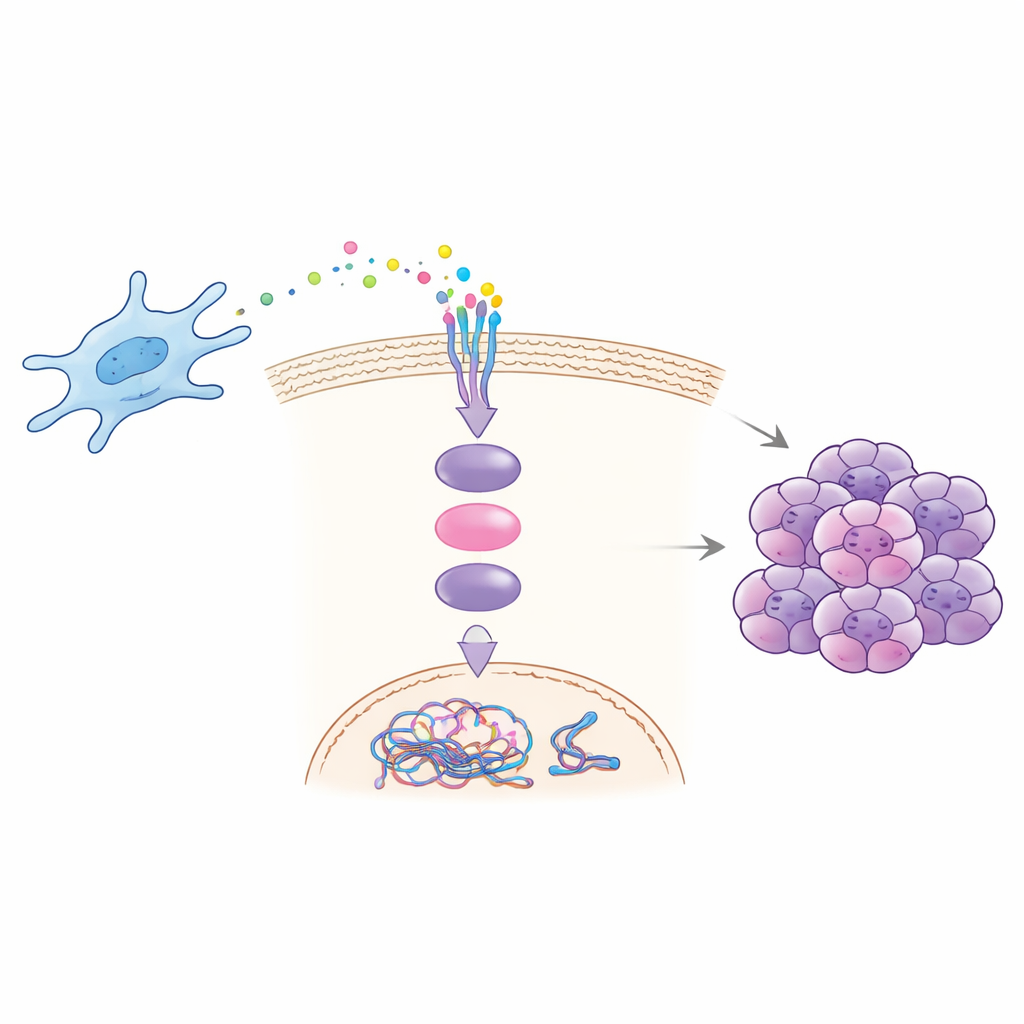
Wie ein Signal eine Kettenreaktion auslöst
Labor‑ und Tierexperimente erklärten, wie CCDC3 die Malignität antreibt. Aus Lebermetastasen isolierte Fibroblasten schütteten mehr CCDC3 aus und steigerten, wenn sie zusammen mit Krebszellen kultiviert wurden, die Wanderungs‑, Invasions‑ und Koloniebildungsfähigkeit der Krebszellen sowie Anzeichen chromosomaler Instabilität. Die Zugabe von gereinigtem CCDC3 an Krebszellen reproduzierte diese Effekte, während das Blockieren von CCDC3 in Fibroblasten sie abschwächte. Das Team zeigte, dass CCDC3 an einen Rezeptor namens CXCR3 auf Krebszellen bindet, der anschließend das bekannte Signalprotein STAT3 im Inneren der Zelle aktiviert. Aktiviertes STAT3 wandert in den Kern und erhöht direkt die Produktion von CDT1, einem Protein, das die Lizenzierung der DNA‑Replikation unterstützt. Ein Übermaß an CDT1 stört das normale Timing und die Genauigkeit der DNA‑Kopieprozesse und fördert so Chromosomenfehler und Instabilität.
Vom Mechanismus zur potenziellen Therapie
Durch selektives Blockieren jeder Stufe dieser Kette — CCDC3, CXCR3, STAT3 oder CDT1 — konnten die Forschenden das invasive Verhalten und das Wachstum der Krebszellen in Zellkulturen und Mausmodellen abschwächen. Mäuse, denen zusätzliches CCDC3 verabreicht wurde, entwickelten größere Tumoren und mehr Lebermetastasen, während Tiere, die mit einem Antikörper gegen CCDC3 oder einem STAT3‑Inhibitor behandelt wurden, langsameres Tumorwachstum und weniger Leberherde zeigten. Diese Ergebnisse definieren eine klare Fibroblasten‑zu‑Tumor‑Signalachse, die die Tumorumgebung mit innerer genetischer Unordnung in Krebszellen verbindet. Für Patientinnen und Patienten legt die Arbeit nahe, dass die gezielte Blockade der CCDC3–CXCR3–STAT3–CDT1‑Achse oder die Nutzung von CCDC3‑Werten als Warnsignal für aggressiven Krankheitsverlauf eines Tages helfen könnte, Lebermetastasen beim kolorektalen Karzinom vorzubeugen oder zu behandeln.
Zitation: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Schlüsselwörter: kolorektales Karzinom, Lebermetastasen, Tumormikroumgebung, chromosomale Instabilität, tumorassoziierte Fibroblasten