Clear Sky Science · pt
Combinando IA para revelar vias mediadas por CCDC3 na metástase hepática do câncer colorretal
Por que esta pesquisa importa
O câncer colorretal está entre os tipos de câncer mais comuns no mundo, e muitas mortes ocorrem apenas após a doença se espalhar para o fígado. Os médicos sabem que tumores com cromossomos altamente instáveis tendem a ser mais agressivos e mais difíceis de tratar, mas não estava claro como as células não cancerosas ao redor ajudam a empurrar os tumores para esse estado perigoso. Este estudo revela uma linha de comunicação oculta entre células de suporte ao redor do tumor e as células cancerígenas, mostrando uma cadeia de eventos que promove o caos genético e alimenta metástases no fígado — e apontando para novas formas de interrompê-la.
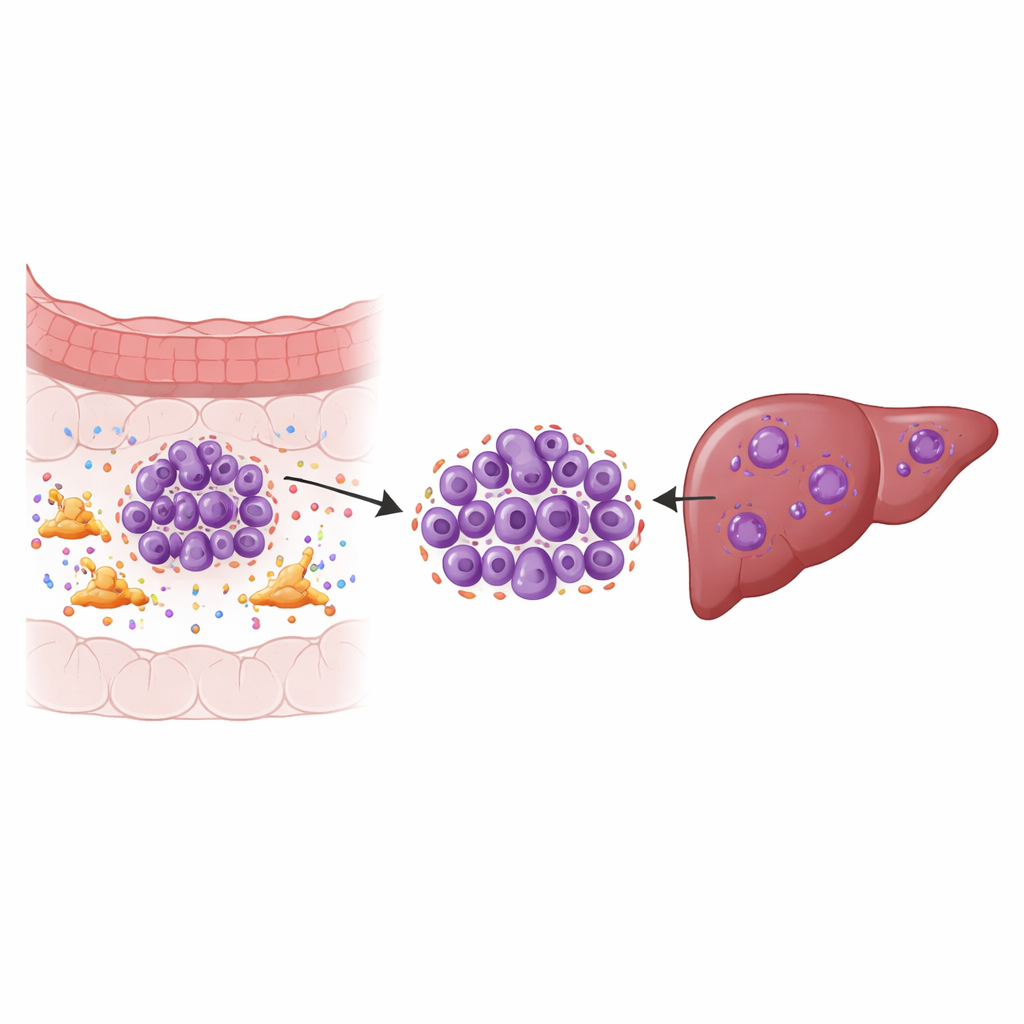
Os ajudantes ocultos ao redor do tumor
Tumores sólidos não são apenas aglomerados de células cancerígenas; são ecossistemas. Um morador-chave desse ecossistema é o fibroblasto associado ao câncer, um tipo de célula do tecido conjuntivo que remodela a área ao redor do tumor e secreta muitos sinais moleculares. Usando sequenciamento de RNA de célula única em amostras de tumores primários colorretais, metástases hepáticas correspondentes, tecidos normais próximos e sangue, os pesquisadores mapearam nove tipos celulares principais e depois se concentraram nas próprias células tumorais. Eles descobriram subgrupos tumorais específicos no fígado que mostravam fortes sinais de instabilidade cromossômica — erros frequentes em como os cromossomos são copiados e divididos — o que está ligado a crescimento rápido, resistência ao tratamento e pior sobrevida.
Uma pontuação numérica para células tumorais perigosas
Para entender quais cânceres têm maior risco, a equipe construiu um “índice de instabilidade” composto que capturou múltiplas camadas de evidência: padrões de expressão gênica, mudanças inferidas no número de cópias cromossômicas e genes conhecidos relacionados à instabilidade. Células tumorais com pontuações altas foram muito mais comuns em metástases hepáticas do que em tumores primários. Essas células de alto índice exibiam ciclo celular hiperativo, mais atividade de dano e reparo de DNA, e características associadas à invasão e disseminação. Em outras palavras, quanto mais instáveis os cromossomos, mais agressivas e adaptáveis pareciam as células cancerígenas — apoiando a ideia de que a instabilidade não é apenas um efeito colateral do câncer, mas um motor de sua progressão.
Um sinal secreto dos fibroblastos
A próxima pergunta foi o que, no ambiente tumoral, poderia estar empurrando as células cancerígenas para esse estado instável. Ao analisar como diferentes tipos celulares “conversam” entre si por meio de moléculas sinalizadoras, os pesquisadores encontraram comunicação especialmente forte entre fibroblastos e as células tumorais com instabilidade cromossômica. Um grupo particular de fibroblastos estava enriquecido em metástases hepáticas e associado a pior sobrevida dos pacientes. Quando os genes ativos nesses fibroblastos foram comparados com os daqueles nas células cancerígenas de alto índice de instabilidade, um se destacou: CCDC3, uma proteína pouco estudada produzida principalmente por fibroblastos e muito mais abundante em lesões hepáticas do que em tumores primários. Pacientes cujos tumores apresentavam níveis mais altos de CCDC3 tendiam a viver menos, sugerindo que esse sinal pode ser um promotor-chave da doença agressiva.
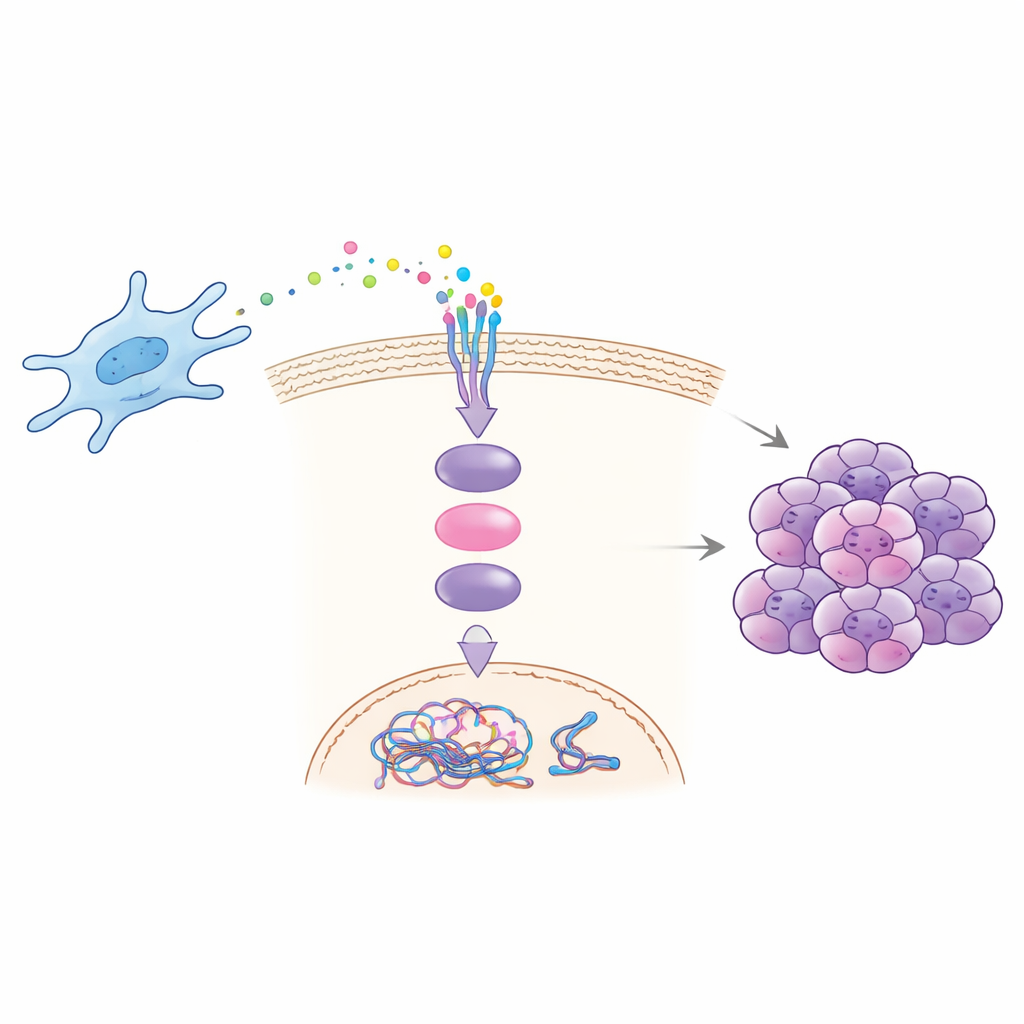
Como um sinal desencadeia uma reação em cadeia
Experimentos em laboratório e em animais revelaram como CCDC3 impulsiona a malignidade. Fibroblastos extraídos de metástases hepáticas secretaram mais CCDC3 e, quando cultivados com células cancerígenas, aumentaram a capacidade dessas células de migrar, invadir, formar colônias e apresentar sinais de instabilidade cromossômica. A adição de CCDC3 purificado às células cancerígenas reproduziu esses efeitos, enquanto bloquear CCDC3 nos fibroblastos os reduzía. A equipe mostrou que CCDC3 se liga a um receptor chamado CXCR3 nas células cancerígenas, que então ativa uma proteína sinalizadora bem conhecida dentro da célula, STAT3. Uma vez ativado, STAT3 viaja ao núcleo e aumenta diretamente a produção de CDT1, uma proteína que ajuda a licenciar a replicação do DNA. O excesso de CDT1 perturba o tempo e a precisão normais da cópia do DNA, promovendo erros cromossômicos e instabilidade.
Do mecanismo ao potencial tratamento
Ao bloquear seletivamente cada etapa dessa cadeia — CCDC3, CXCR3, STAT3 ou CDT1 — os pesquisadores conseguiram atenuar o comportamento invasivo e o crescimento das células cancerígenas em cultura e em modelos murinos. Camundongos recebendo CCDC3 adicional desenvolveram tumores maiores e mais metástases hepáticas, enquanto aqueles tratados com um anticorpo contra CCDC3 ou um inibidor de STAT3 apresentaram crescimento tumoral mais lento e menos lesões hepáticas. Essas descobertas definem uma rota clara de sinalização de fibroblastos para tumor que conecta o microambiente tumoral ao caos genético interno das células cancerígenas. Para os pacientes, esse trabalho sugere que direcionar o eixo CCDC3–CXCR3–STAT3–CDT1, ou usar os níveis de CCDC3 como um sinal de alerta de doença agressiva, poderia um dia ajudar a prevenir ou tratar metástases hepáticas do câncer colorretal.
Citação: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Palavras-chave: câncer colorretal, metástase hepática, microambiente tumoral, instabilidade cromossômica, fibroblastos associados ao câncer