Clear Sky Science · it
Combinare l’IA per rivelare le vie mediate da CCDC3 nella metastasi epatica del cancro colorettale
Perché questa ricerca è importante
Il cancro colorettale è uno dei tumori più diffusi al mondo e molte morti si verificano solo dopo che la malattia si è diffusa al fegato. I medici sanno che i tumori con cromosomi altamente instabili tendono a essere più aggressivi e più difficili da trattare, ma non era chiaro in che modo le cellule non tumorali circostanti contribuiscano a spingere i tumori verso questo stato pericoloso. Questo studio scopre una linea di comunicazione nascosta tra le cellule di supporto intorno al tumore e le cellule tumorali, rivelando una catena di eventi che genera caos genetico e alimenta le metastasi epatiche—e indicando nuovi modi per bloccarla.
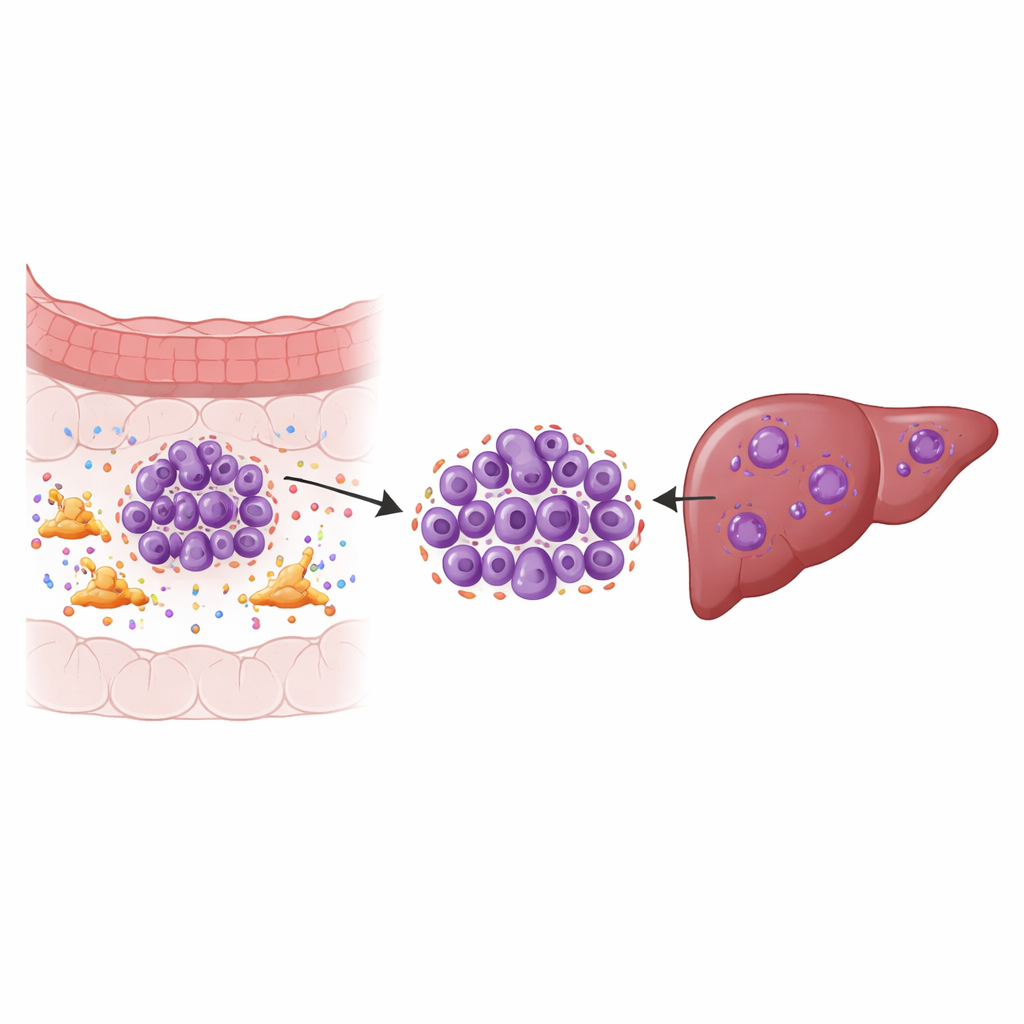
Gli aiutanti nascosti intorno al tumore
I tumori solidi non sono solo ammassi di cellule tumorali; sono ecosistemi. Un abitante chiave di questo ecosistema è il fibroblasto associato al cancro, un tipo di cellula del tessuto connettivo che rimodella l’area intorno al tumore e secerne molti segnali molecolari. Usando il sequenziamento dell’RNA a singola cellula su campioni di tumori colorettali primari, metastasi epatiche corrispondenti, tessuti normali vicini e sangue, i ricercatori hanno mappato nove tipi cellulari principali per poi concentrarsi sulle cellule tumorali stesse. Hanno scoperto sottogruppi tumorali specifici nel fegato che mostravano forti segnali di instabilità cromosomica—frequenti errori nella copia e nella divisione dei cromosomi—collegata a crescita rapida, resistenza ai trattamenti e scarsa sopravvivenza.
Un punteggio numerico per le cellule tumorali pericolose
Per capire quali tumori sono maggiormente a rischio, il team ha costruito un «indice di instabilità» composito che raccoglieva più livelli di evidenza: schemi di espressione genica, cambiamenti inferiti nel numero di copie dei cromosomi e geni noti per essere legati all’instabilità. Le cellule tumorali con punteggi elevati erano molto più comuni nelle metastasi epatiche che nei tumori primari. Queste cellule ad alto indice mostravano un ciclo cellulare iperattivo, maggiore attività di danno e riparazione del DNA e caratteristiche associate all’invasione e alla diffusione. In altre parole, più i cromosomi erano instabili, più le cellule tumorali apparivano aggressive e adattabili—a sostegno dell’idea che l’instabilità non sia solo un effetto collaterale del cancro, ma un motore della sua progressione.
Un segnale segreto dai fibroblasti
La domanda successiva era cosa, nell’ambiente tumorale, potesse spingere le cellule tumorali verso questo stato instabile. Analizzando come diversi tipi cellulari «parlano» tra loro tramite molecole segnale, i ricercatori hanno trovato una comunicazione particolarmente forte tra i fibroblasti e le cellule tumorali con instabilità cromosomica. Un gruppo particolare di fibroblasti era arricchito nelle metastasi epatiche e collegato a una peggiore sopravvivenza dei pazienti. Quando i geni attivi in questi fibroblasti sono stati confrontati con quelli nelle cellule tumorali ad alta instabilità, uno è emerso in modo evidente: CCDC3, una proteina poco studiata prodotta principalmente dai fibroblasti e molto più abbondante nelle lesioni epatiche che nei tumori primari. I pazienti i cui tumori presentavano livelli più elevati di CCDC3 tendevano ad avere una sopravvivenza più breve, suggerendo che questo segnale potrebbe essere un promotore chiave della malattia aggressiva.
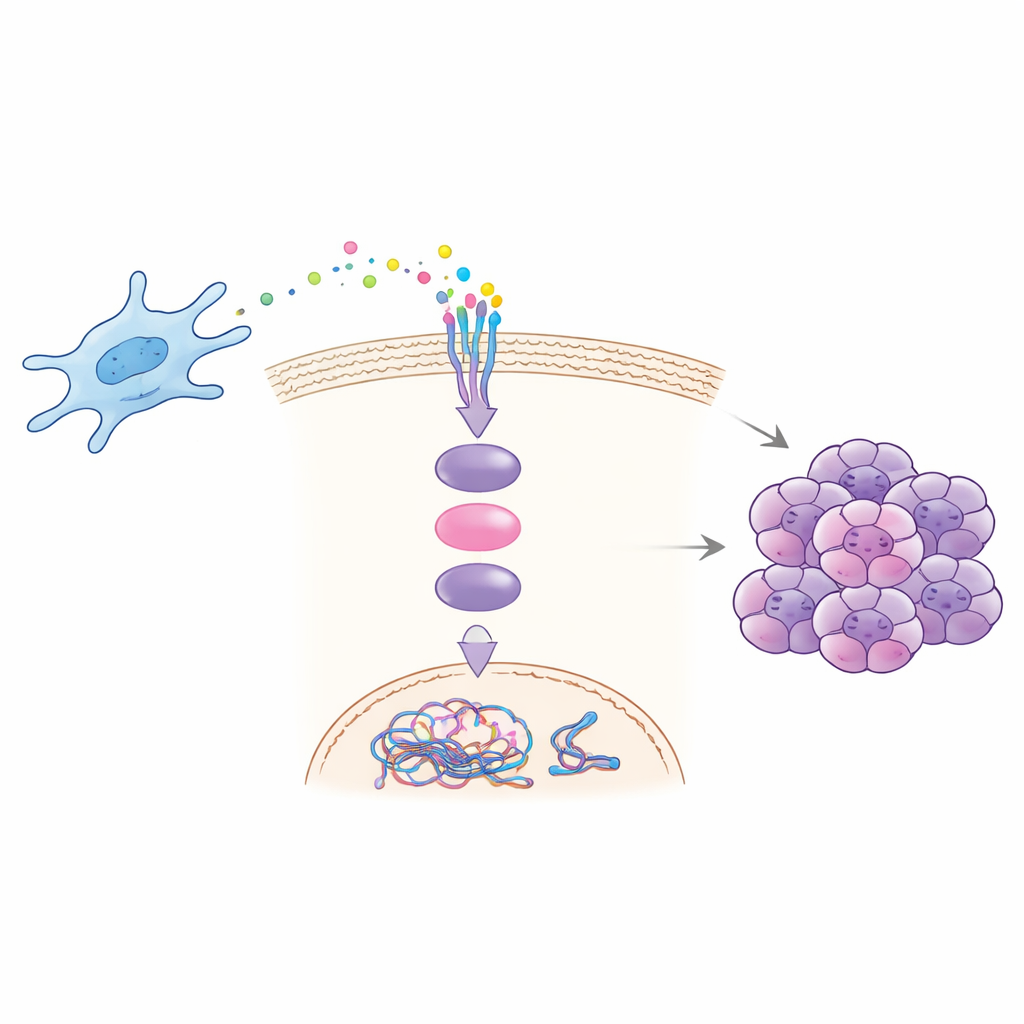
Come un segnale innesca una reazione a catena
Esperimenti in laboratorio e su animali hanno rivelato come CCDC3 guida la malignità. I fibroblasti prelevati da metastasi epatiche secernono più CCDC3 e, quando coltivati con cellule tumorali, aumentano la capacità delle cellule cancerose di migrare, invadere, formare colonie e mostrare segni di instabilità cromosomica. L’aggiunta di CCDC3 purificato alle cellule tumorali riproduceva questi effetti, mentre bloccare CCDC3 nei fibroblasti li riduceva. Il gruppo ha dimostrato che CCDC3 si lega a un recettore chiamato CXCR3 sulle cellule tumorali, che attiva poi una nota proteina di segnalazione all’interno della cellula, STAT3. Una volta attivata, STAT3 viaggia nel nucleo e aumenta direttamente la produzione di CDT1, una proteina che aiuta a regolare l’avvio della replicazione del DNA. Un eccesso di CDT1 altera il normale timing e la precisione della copiatura del DNA, favorendo errori cromosomici e instabilità.
Dal meccanismo al potenziale trattamento
Bloccando selettivamente ogni passaggio di questa catena—CCDC3, CXCR3, STAT3 o CDT1—i ricercatori sono riusciti a ridurre il comportamento invasivo e la crescita delle cellule tumorali in colture e in modelli murini. I topi a cui è stato somministrato CCDC3 supplementare sviluppavano tumori più grandi e più metastasi epatiche, mentre quelli trattati con un anticorpo contro CCDC3 o con un inibitore di STAT3 mostravano crescita tumorale più lenta e meno lesioni epatiche. Questi risultati definiscono una chiara via di segnalazione fibroblasto→tumore che collega il microambiente tumorale al caos genetico interno nelle cellule cancerose. Per i pazienti, questo lavoro suggerisce che mirare all’asse CCDC3–CXCR3–STAT3–CDT1, o usare i livelli di CCDC3 come segnale di allarme di malattia aggressiva, potrebbe un giorno aiutare a prevenire o trattare le metastasi epatiche del cancro colorettale.
Citazione: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Parole chiave: cancro colorettale, metastasi epatica, microambiente tumorale, instabilità cromosomica, fibroblasti associati al cancro