Clear Sky Science · fr
Combiner l’IA pour révéler les voies médiées par CCDC3 impliquées dans les métastases hépatiques du cancer colorectal
Pourquoi cette recherche est importante
Le cancer colorectal est l’un des cancers les plus fréquents dans le monde, et de nombreux décès surviennent lorsque la maladie s’est propagée au foie. Les cliniciens savent que les tumeurs présentant une grande instabilité chromosomique ont tendance à être plus agressives et plus difficiles à traiter, mais on ne comprenait pas clairement comment les cellules non cancéreuses environnantes contribuent à pousser les tumeurs vers cet état dangereux. Cette étude met au jour une voie de communication jusque-là cachée entre les cellules de soutien autour de la tumeur et les cellules cancéreuses, révélant une chaîne d’événements qui provoque le chaos génétique et alimente les métastases hépatiques — et indiquant de nouvelles pistes pour l’arrêter.
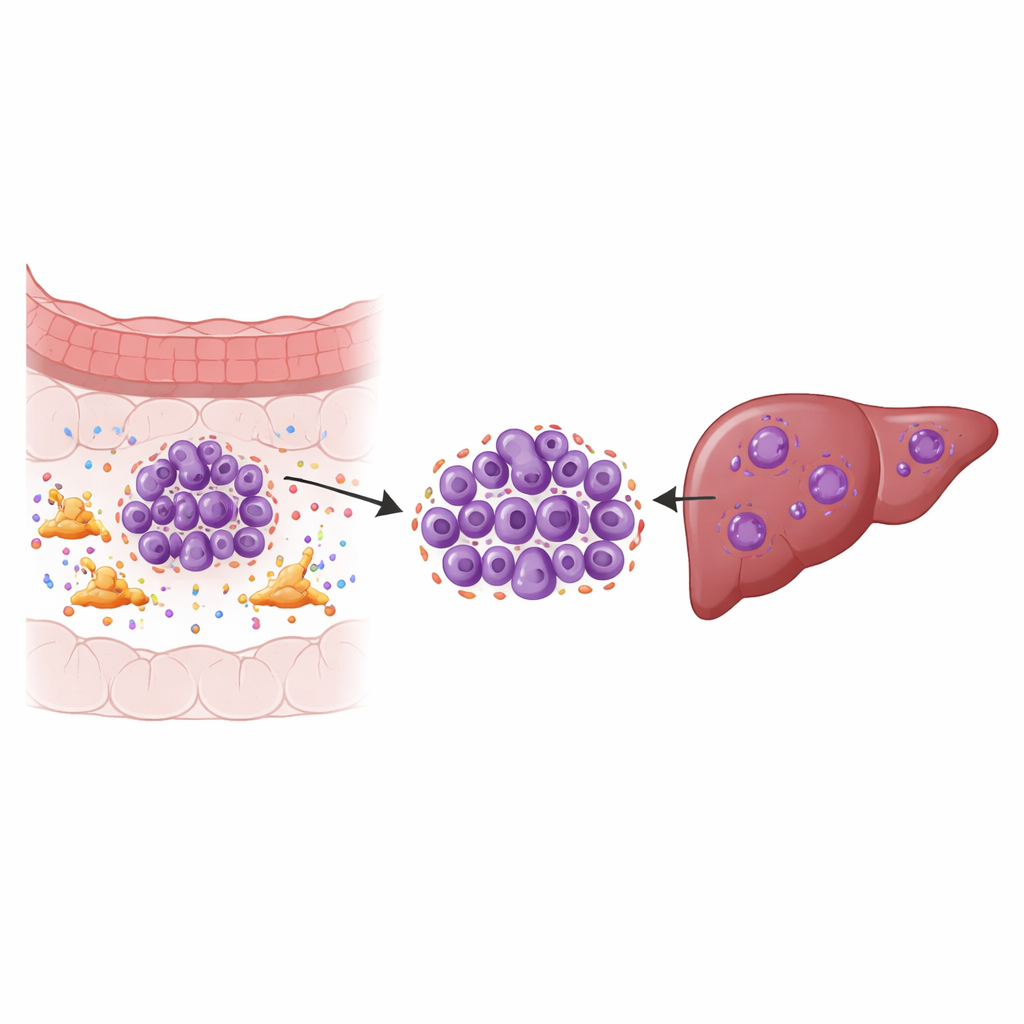
Les aides invisibles autour de la tumeur
Les tumeurs solides ne sont pas de simples amas de cellules cancéreuses ; ce sont des écosystèmes. Un habitant clé de cet écosystème est le fibroblaste associé au cancer, un type de cellule du tissu conjonctif qui reconfigure la zone autour de la tumeur et sécrète de nombreux signaux. En utilisant le séquençage ARN unicellulaire sur des échantillons de tumeurs colorectales primaires, de métastases hépatiques correspondantes, de tissus normaux adjacents et de sang, les chercheurs ont cartographié neuf types cellulaires majeurs puis se sont concentrés sur les cellules tumorales elles‑mêmes. Ils ont découvert des sous-groupes tumoraux spécifiques dans le foie montrant de fortes signatures d’instabilité chromosomique — des erreurs fréquentes lors de la copie et de la répartition des chromosomes — ce qui est associé à une croissance rapide, à la résistance aux traitements et à un pronostic défavorable.
Un score numérique pour les cellules tumorales dangereuses
Pour déterminer quels cancers étaient les plus à risque, l’équipe a construit un « indice d’instabilité » composite qui intégrait plusieurs niveaux de preuves : profils d’expression génique, changements inférés du nombre de copies chromosomiques et gènes connus liés à l’instabilité. Les cellules tumorales ayant des scores élevés étaient bien plus fréquentes dans les métastases hépatiques que dans les tumeurs primaires. Ces cellules à indice élevé présentaient un cycle cellulaire hyperactif, davantage d’activités de dommage et de réparation de l’ADN, et des caractéristiques associées à l’invasion et à la dissémination. En d’autres termes, plus les chromosomes étaient instables, plus les cellules cancéreuses semblaient agressives et adaptables — soutenant l’idée que l’instabilité n’est pas seulement un effet secondaire du cancer, mais un moteur de sa progression.
Un signal secret venu des fibroblastes
La question suivante était : qu’est‑ce dans le microenvironnement tumoral qui pourrait pousser les cellules cancéreuses vers cet état instable ? En analysant la façon dont les différents types cellulaires « communiquent » via des molécules de signalisation, les chercheurs ont trouvé une communication particulièrement forte entre les fibroblastes et les cellules tumorales à instabilité chromosomique. Un groupe particulier de fibroblastes était enrichi dans les métastases hépatiques et associé à une survie patient plus mauvaise. En comparant les gènes actifs dans ces fibroblastes avec ceux des cellules cancéreuses à instabilité élevée, un gène a émergé : CCDC3, une protéine peu étudiée produite principalement par les fibroblastes et beaucoup plus abondante dans les lésions hépatiques que dans les tumeurs primaires. Les patients dont les tumeurs présentaient des niveaux plus élevés de CCDC3 avaient tendance à avoir une survie plus courte, ce qui suggère que ce signal pourrait être un promoteur clé de la maladie agressive.
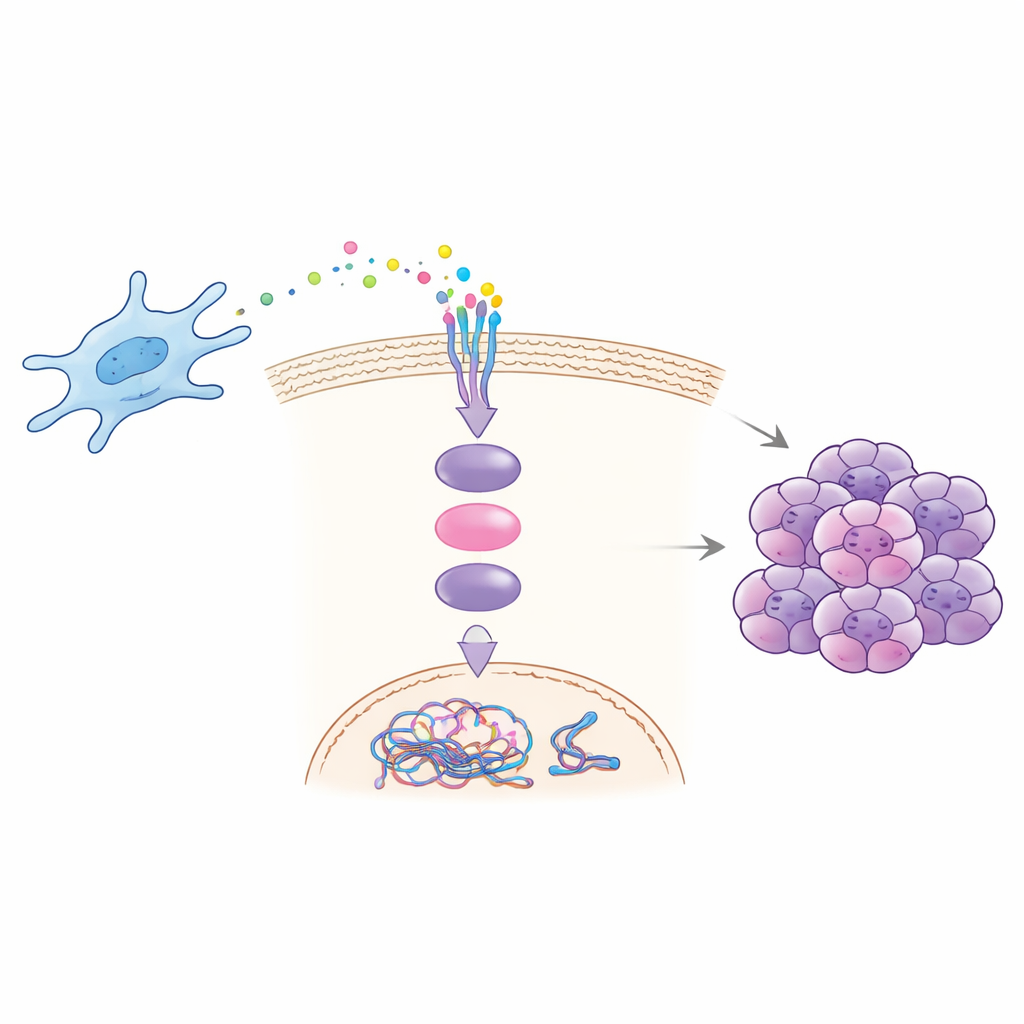
Comment un signal déclenche une réaction en chaîne
Des expériences en laboratoire et chez l’animal ont révélé comment CCDC3 favorise la malignité. Les fibroblastes prélevés dans des métastases hépatiques sécrétaient davantage de CCDC3 et, lorsqu’ils étaient mis en culture avec des cellules cancéreuses, renforçaient la capacité de ces dernières à migrer, envahir, former des colonies et afficher des signes d’instabilité chromosomique. L’ajout de CCDC3 purifié aux cellules cancéreuses reproduisait ces effets, tandis que le blocage de CCDC3 dans les fibroblastes les atténuait. L’équipe a montré que CCDC3 se lie à un récepteur appelé CXCR3 sur les cellules cancéreuses, ce qui active ensuite une protéine messagère bien connue, STAT3. Une fois activée, STAT3 se déplace vers le noyau et augmente directement la production de CDT1, une protéine qui participe à l’initiation de la réplication de l’ADN. Un excès de CDT1 perturbe la synchronisation et la précision normales de la copie de l’ADN, favorisant les erreurs chromosomiques et l’instabilité.
Du mécanisme au traitement potentiel
En bloquant sélectivement chaque étape de cette chaîne — CCDC3, CXCR3, STAT3 ou CDT1 — les chercheurs ont pu diminuer le comportement invasif et la croissance des cellules cancéreuses en culture et dans des modèles murins. Les souris recevant un excès de CCDC3 développaient des tumeurs plus volumineuses et davantage de métastases hépatiques, tandis que celles traitées par un anticorps contre CCDC3 ou par un inhibiteur de STAT3 présentaient une croissance tumorale plus lente et moins de lésions hépatiques. Ces résultats définissent une voie de signalisation claire du fibroblaste vers la tumeur qui relie le microenvironnement tumoral au chaos génétique interne des cellules cancéreuses. Pour les patients, ce travail suggère que cibler l’axe CCDC3–CXCR3–STAT3–CDT1, ou utiliser les niveaux de CCDC3 comme indicateur d’une maladie agressive, pourrait un jour aider à prévenir ou traiter les métastases hépatiques du cancer colorectal.
Citation: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Mots-clés: cancer colorectal, métastases hépatiques, microenvironnement tumoral, instabilité chromosomique, fibroblastes associés au cancer