Clear Sky Science · ru
Объединение ИИ для выявления путей метастазирования колоректального рака в печень, опосредованных CCDC3
Почему это исследование важно
Колоректальный рак — один из самых распространённых видов рака в мире, и значительная часть смертей наступает после того, как болезнь распространяется в печень. Врачи знают, что опухоли с высокой хромосомной нестабильностью обычно агрессивнее и труднее поддаются лечению, но долгое время оставалось неясным, как окружающие опухоль нормальные клетки способствуют переходу опухоли в это опасное состояние. В этом исследовании раскрывается скрытая линия связи между поддерживающими клетками вокруг опухоли и раковыми клетками, показывающая цепочку событий, которая вызывает генетический хаос и подпитывает печёночные метастазы — и указывающая на новые способы остановить этот процесс.
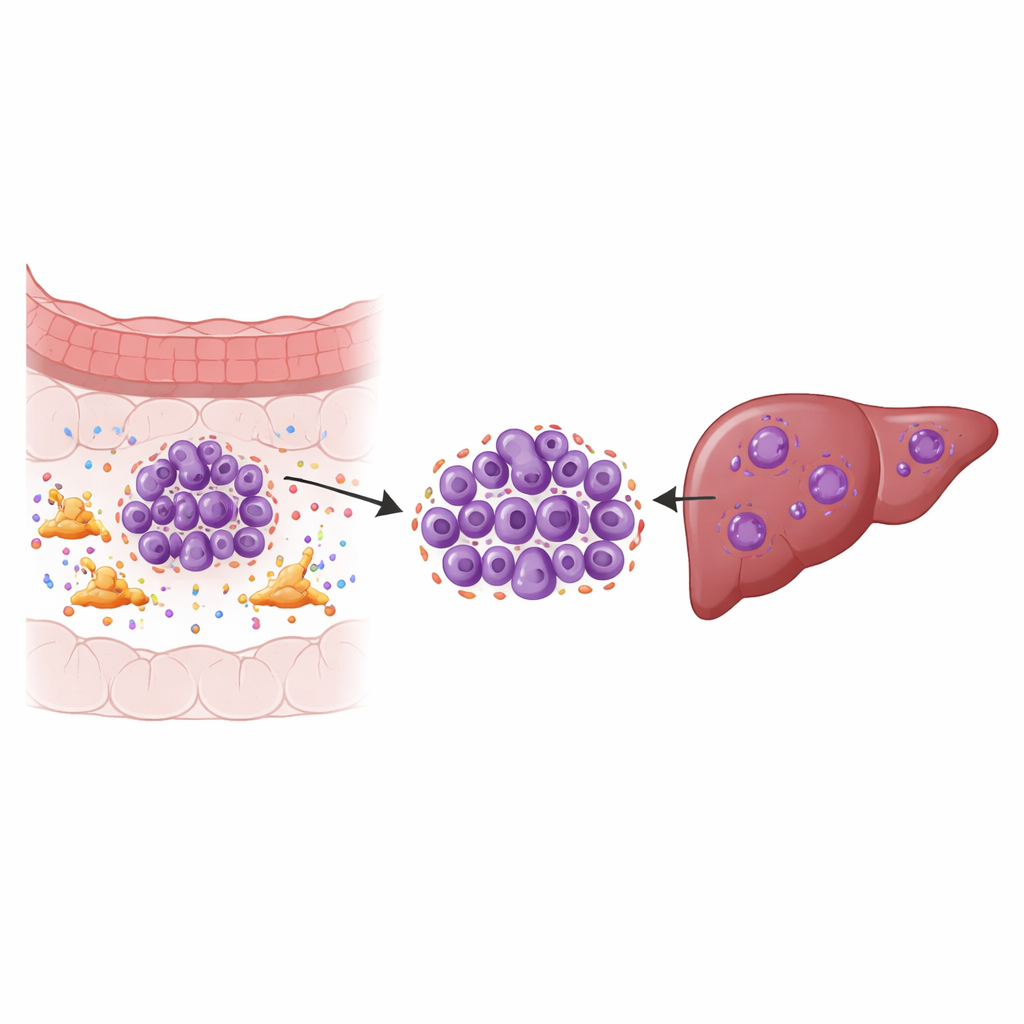
Скрытые помощники вокруг опухоли
Твёрдые опухоли — это не просто скопления раковых клеток; это экосистемы. Одним из ключевых жителей этой экосистемы являются фибробласты, ассоциированные с раком — тип соединительнотканных клеток, который ремоделирует область вокруг опухоли и выделяет множество сигнальных молекул. Применив одноклеточный РНК-секвенирование к образцам из первичных колоректальных опухолей, соответствующих печёночных метастазов, соседних нормальных тканей и крови, исследователи картировали девять основных типов клеток и затем подробно изучили сами раковые клетки. Они обнаружили специфические подгруппы опухолей в печени с выраженными признаками хромосомной нестабильности — частых ошибок при копировании и распределении хромосом — что связано с быстрым ростом, устойчивостью к лечению и плохим прогнозом.
Числовой индекс для опасных опухолевых клеток
Чтобы понять, какие опухоли находятся в наибольшей зоне риска, команда создала составной «индекс нестабильности», который объединял несколько уровней доказательств: закономерности экспрессии генов, выводимые изменения числа копий хромосом и известные гены, связанные с нестабильностью. Клетки опухоли с высокими значениями индекса встречались во много раз чаще в печёночных метастазах, чем в первичных опухолях. Эти клетки с высоким индексом демонстрировали гиперактивный клеточный цикл, повышенную активность повреждения ДНК и её ремонта, а также признаки, связанные с инвазией и распространением. Иными словами, чем более нестабильны хромосомы, тем агрессивнее и адаптивнее кажутся раковые клетки — что поддерживает идею о том, что нестабильность не просто побочный эффект рака, а движущая сила его прогрессии.
Секретный сигнал от фибробластов
Следующим вопросом было — что в микроокружении опухоли толкает раковые клетки к этому нестабильному состоянию. Анализируя, как разные типы клеток «общаются» друг с другом через сигнальные молекулы, исследователи обнаружили особенно сильную связь между фибробластами и хромосомно нестабильными опухолевыми клетками. Определённая группа фибробластов была обогащена в печёночных метастазах и связана с худшей выживаемостью пациентов. При сравнении генов, активных в этих фибробластах, с генами в опухолевых клетках с высокой нестабильностью, выделился один ген: CCDC3 — малоизученный белок, который в основном продуцируют фибробласты и который был гораздо более распространён в печёночных очагах, чем в первичных опухолях. У пациентов с повышенным уровнем CCDC3 в опухолях отмечалась более короткая продолжительность жизни, что говорит о том, что этот сигнал может играть ключевую роль в продвижении агрессивной болезни.
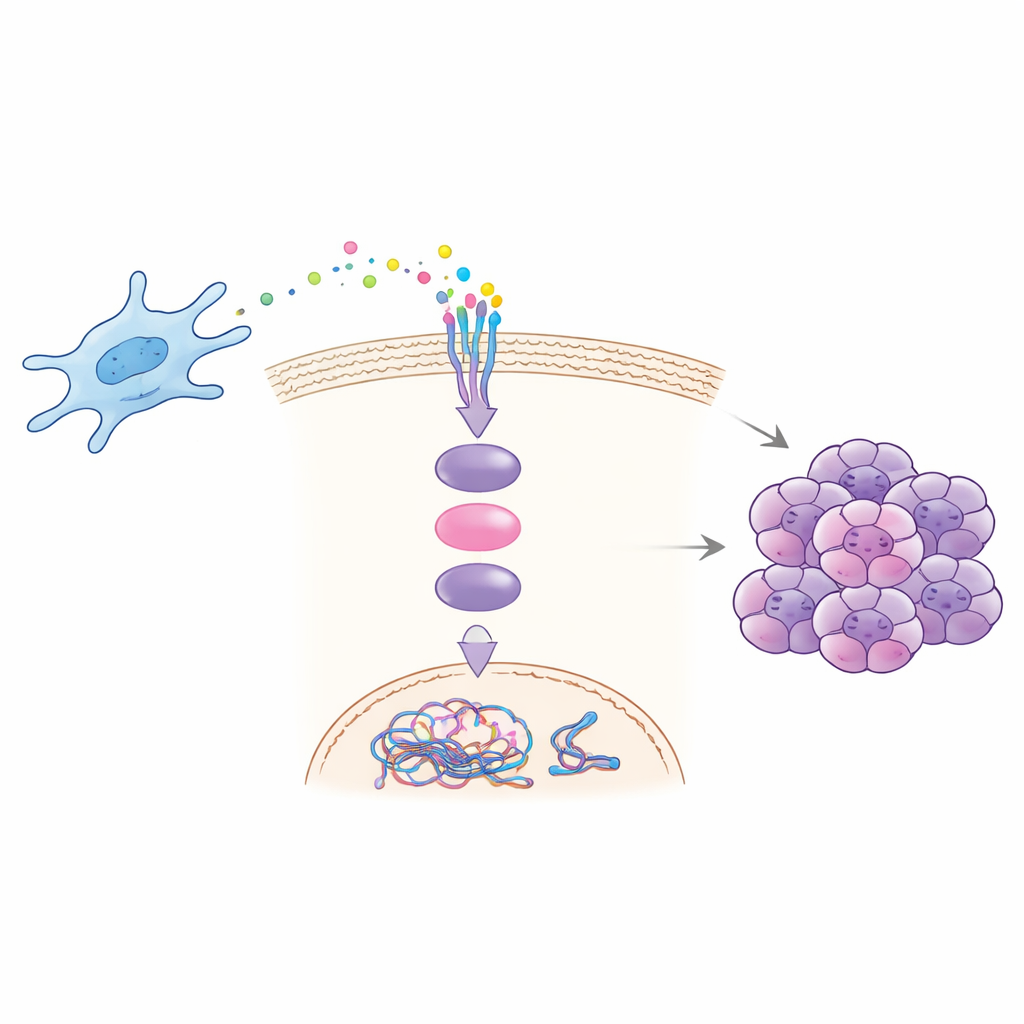
Как один сигнал запускает цепную реакцию
Лабораторные и животные эксперименты показали, как CCDC3 стимулирует злокачественность. Фибробласты, взятые из печёночных метастазов, секрецировали больше CCDC3 и, при совместном культивировании с раковыми клетками, усиливали способность последних мигрировать, проникать, образовывать колонии и проявлять признаки хромосомной нестабильности. Добавление очищенного CCDC3 к раковым клеткам воспроизводило эти эффекты, тогда как блокирование CCDC3 в фибробластах снижало их. Команда показала, что CCDC3 связывается с рецептором CXCR3 на раковых клетках, что затем активирует хорошо известный внутриклеточный посредник STAT3. После активации STAT3 перемещается в ядро и напрямую повышает продукцию CDT1 — белка, участвующего в лицензировании репликации ДНК. Избыток CDT1 нарушает нормальную синхронизацию и точность копирования ДНК, способствуя ошибкам в хромосомах и нестабильности.
От механизма к потенциальному лечению
Избирательное блокирование каждого шага этой цепочки — CCDC3, CXCR3, STAT3 или CDT1 — позволяло ослабить инвазивное поведение и рост раковых клеток в культурах и в моделях на мышах. У мышей, получавших дополнительный CCDC3, развивались большие опухоли и больше печёночных метастазов, тогда как у тех, кого лечили антителом против CCDC3 или ингибитором STAT3, рост опухолей замедлялся и число печёночных очагов уменьшалось. Эти результаты определяют ясный сигнал от фибробластов к опухоли, который связывает микроокружение опухоли с внутренним генетическим хаосом в раковых клетках. Для пациентов эта работа указывает, что нацеленность на ось CCDC3–CXCR3–STAT3–CDT1 или использование уровня CCDC3 как индикатора агрессивности заболевания могли бы в будущем помочь предотвратить или лечить печёночные метастазы при колоректальном раке.
Цитирование: Huang, R., Liu, Q., Jin, X. et al. Combining AI to reveal CCDC3-mediated pathways of colorectal cancer liver metastasis. npj Digit. Med. 9, 327 (2026). https://doi.org/10.1038/s41746-026-02457-0
Ключевые слова: колоректальный рак, метастазы в печень, микроокружение опухоли, хромосомная нестабильность, фибробласты, ассоциированные с раком