Clear Sky Science · tr
Çoklu-omik profilleme, bağışıklık tedavisi yanıtı ve prognoz ile ilişkili tümör mikroçevresi özelliklerini küçük hücre dışı akciğer kanserinde ortaya koyuyor
Bu çalışma akciğer kanseri olanlar için neden önemli
İleri evre akciğer kanseri hastalarının birçoğu artık tümörlere saldırması için bağışıklık sistemini güçlendiren immünoterapi ilaçları alıyor. Yine de pek çok hasta ya fayda görmüyor ya da kanseri yeniden nüksediyor. Bu çalışma basit ama hayati bir soruyu gündeme getiriyor: Tedaviye yanıt veren tümörlerin içinde, yanıt vermeyenlere kıyasla ne farklıdır ve bu bilgi küçük hücre dışı akciğer kanseri hastalarına daha iyi bakım sağlamak için nasıl kullanılabilir?
Tümörlerin içine hücre hücre bakmak
Araştırmacılar, immünoterapi alan (çoğunlukla kemoterapi ile birlikte) hastalardan alınan akciğer tümörlerinin ayrıntılı bir haritasını çıkarmak için birkaç güçlü genetik aracı birleştirdi. Tüm tümörün ortalamasını almak yerine, bireysel hücreleri analiz ederek bağışıklık hücrelerini, kanser hücrelerini ve destek hücreleri belirlediler. Tedavi sonrası derin şekilde küçülen tümörleri küçülmeyenlerle karşılaştırdıklarında, başarılı yanıtların belirli bir öldürücü T hücresi grubunun varlığı ve çevreleyen tümör mikroçevresinin bağışıklık saldırısına ne kadar dost veya düşman olduğuyla yakın bağlantılı olduğunu buldular.
Daha iyi sonuçlarla ilişkili özel bir öldürücü T hücresi grubu
İncelenen tüm bağışıklık hücreleri arasında, bir CD8 T hücresi alt kümesi öne çıktı. Bu hücreler ZNF683 adlı bir genin yüksek düzeyleriyle işaretleniyordu. İmmünoterapiye iyi yanıt veren hastaların tümörleri bu ZNF683-pozitif CD8 T hücreleri bakımından zengindi; yanıt vermeyen tümörlerde ise bunların sayısı çok daha azdı. Ekip, farklı kanser türleri ve geniş hasta koleksiyonları genelinde daha yüksek ZNF683 düzeylerinin genellikle daha fazla bağışıklık hücresi varlığı ve daha iyi sağkalım ile el ele gittiğini gösterdi. Ardından, bu T hücresi grubuyla ilişkili 19 gene dayanan bir risk skoru oluşturup akciğer adenokarsinomlu hastaları daha düşük riskli, bağışıklık açısından “sıcak” tümörler ve daha yüksek riskli, bağışıklık açısından “soğuk” tümörler olarak sınıflandırabildi.
Soğuk tümörler, baskılayıcı bir sinyal ve yeni bir hedef
ZNFRS skoru ile tanımlanan yüksek riskli tümörlerde faydalı bağışıklık hücreleri daha az, kanser ve myeloid hücreler ise daha fazlaydı; bu desen, immünoterapiye dirençli “soğuk” tümörlere tipiktir. Araştırmacılar bu tümörlerdeki hücrelerin birbirleriyle nasıl iletişim kurduğunu incelediklerinde, birçok sinyalin myeloid ve kanser hücrelerinden T hücreleri ve doğal öldürücü hücrelere aktığını buldular. Anahtar oyunculardan biri, myeloid veya kanser hücrelerinden salınarak bağışıklık hücrelerindeki reseptörlere giden SPP1 adlı bir sekretuvar proteindi. Bu SPP1 sinyal ağı, yanıt vermeyen ve yüksek riskli tümörlerde güçlüyken; yanıt veren ve düşük riskli tümörlerde zayıf veya yoktu; bu da SPP1’in öldürücü T hücreleri uzak tutan veya etkinliklerini azaltan bağışıklık baskılayıcı bir niş oluşturmasına yardımcı olduğunu düşündürüyor.
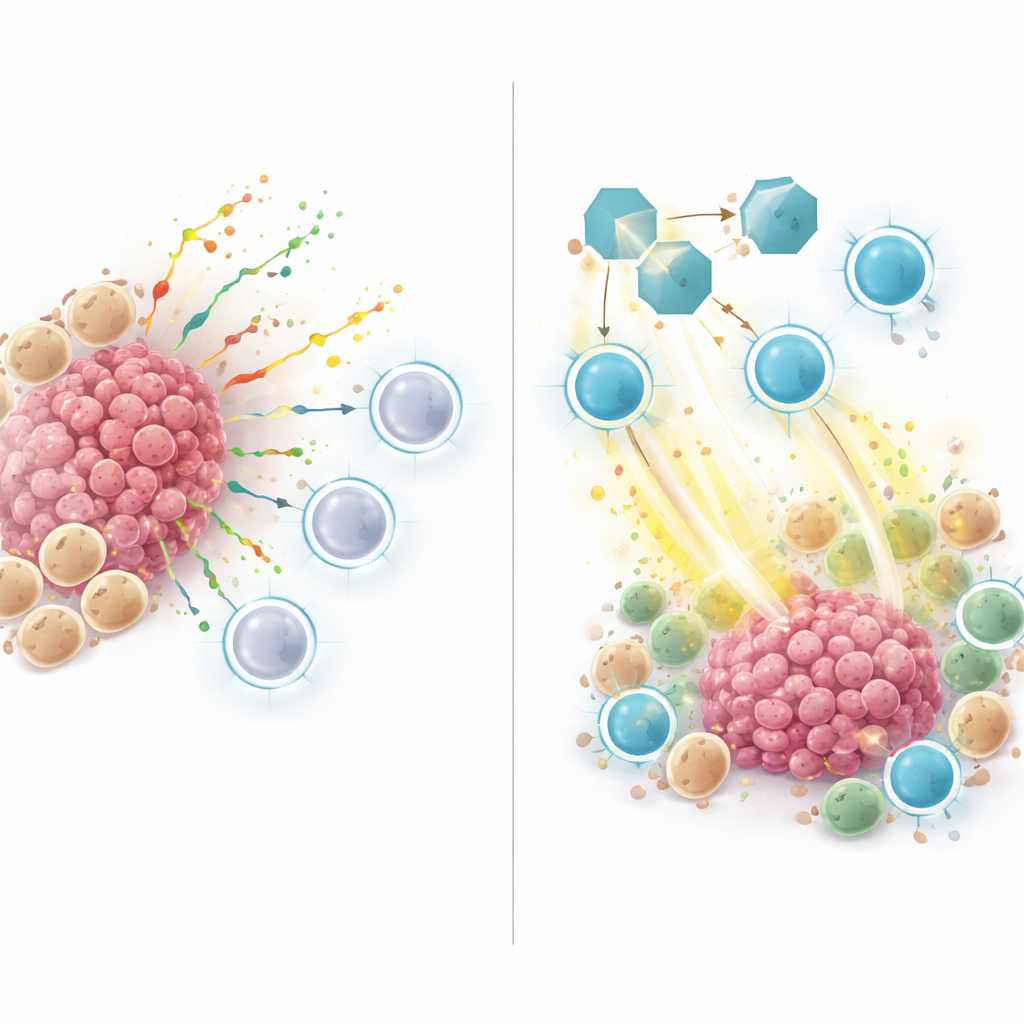
SPP1 engellemenin hayvan modellerinde test edilmesi
İnsan verilerindeki desenlerin ötesine geçmek için ekip akciğer kanserinin fare modellerine yöneldi. Tümör taşıyan farelere SPP1’i bloke eden bir antikor uyguladılar; bunu anti-PD-1 immünoterapi ilacı ile tek başına veya kombinasyon halinde denediler. SPP1’i tek başına engellemek tümör büyümesini yavaşlattı ve anti-PD-1 ile kombinasyon en iyi sonucu verdi. Mikroskop ve tek hücre analizleri, SPP1 bloke edilen farelerin tümörlerinde kanser hücrelerini öldüren toksik moleküller üreten daha fazla aktif CD8 T hücresi ve genellikle tümör büyümesini destekleyen M2-benzeri makrofajların daha az olduğunu gösterdi. Başka bir deyişle, SPP1 inhibisyonu mikroçevreyi baskılayıcı halden bağışıklık tarafından aktive edilmiş bir duruma kaydırdı.
Bu bulguların gelecekteki tedaviler için anlamı
Hekimler ve halk için ana mesaj, tümördeki bütün bağışıklık hücrelerinin eşit olmadığı ve çevresindeki ortamın onları ne kadar ağırlayıp ağırlamadığının önemli olduğu. Bu çalışma, akciğer kanserinde başarılı immünoterapi ile ilişkili özel bir öldürücü T hücresi türünü belirliyor ve tümörün bağışıklık ikliminin ne kadar “sıcak” veya “soğuk” olduğunu yansıtan bir gen tabanlı skor oluşturuyor. Ayrıca SPP1’i tümörlerin bağışıklık sisteminden kaçmasına yardımcı olan önemli bir zararlı sinyal olarak vurguluyor. Farelerde SPP1’i bloke ederek araştırmacılar öldürücü T hücreleri uyandırabildi ve standart immünoterapinin etkinliğini artırabildi. Daha fazla klinik test gerektiği halde, bu bulgular kimin immünoterapiden en çok fayda görebileceğini belirleyen kan ve doku testleri ile dirençli akciğer tümörlerini bağışıklığın daha etkili saldırabileceği hale getirebilecek kombinasyon tedavilerine giden bir yolu ortaya koyuyor.
Atıf: Zhang, L., Zeng, J., Wen, J. et al. Multi-omics profiling reveals tumor microenvironment characteristics linked to immunotherapy response and prognosis in non-small cell lung cancer. npj Precis. Onc. 10, 179 (2026). https://doi.org/10.1038/s41698-026-01474-2
Anahtar kelimeler: küçük hücre dışı akciğer kanseri, immünoterapi, tümör mikroçevresi, CD8 T hücreleri, SPP1 sinyalleşmesi