Clear Sky Science · he
מיפוי מולטי-אומיקס חושף מאפייני מיקרו-סביבת הגידול המקושרים לתגובה לאימונותרפיה ולפרוגנוזה בסרטן ריאות שאינו סוג תאי קטן
מדוע המחקר הזה חשוב לאנשים עם סרטן ריאות
רבים מחולי סרטן ריאות מתקדם כיום מקבלים תרופות אימונותרפיות שמעצימות את המערכת החיסונית לתקוף את הגידולים. עם זאת, אוכלוסייה גדולה של מטופלים אינה נהנית מהטיפול או שחוזר אצלם הסרטן. מחקר זה שואל שאלה פשוטה אך מכרעת: מה שונה בתוך הגידולים שמגיבים לטיפול אל מול אלה שאינם מגיבים, והאם הידע הזה יכול להנחות טיפול טוב יותר בחולי סרטן ריאות שאינו סוג תאי קטן?
מסתכלים לתוך הגידולים תא תא
החוקרים שילבו מספר כלים גנטיים רבי-עוצמה לבניית מפת פירוט של גידולי ריאה ממטופלים שקיבלו אימונותרפיה, לעיתים בשילוב כימותרפיה. במקום לאזן אותות על כל הגידול, הם ניתחו תאים בודדים, וזיהו תאי מערכת חיסון, תאי סרטן ותאי תמיכה. על ידי השוואת גידולים שהתכווצו באופן עמוק אחרי הטיפול לאלה שלא הגיבו, הם מצאו שתגובות מוצלחות קשורות קשר הדוק לנוכחות קבוצה מסוימת של תאי T רוצחים ולמידת הידידותיות או העוינות של מיקרו-סביבת הגידול להתקפה חיסונית.
קבוצה מיוחדת של תאי T רוצחים קשורה לתוצאות טובות יותר
מבין כל תאי המערכת החיסונית שנבדקו, תת-אוכלוסייה אחת של תאי CD8 בלטה. תאים אלה אופיינו ברמות גבוהות של גן בשם ZNF683. גידולים של מטופלים שהגיבו היטב לאימונותרפיה היו עשירים בתאי CD8 חיוביים ל-ZNF683, בעוד שבגידולים שלא הגיבו נצפו הרבה פחות מהם. הצוות הראה, בעשרות סוגי סרטן ואוספי חולים גדולים, שרמות גבוהות של ZNF683 בדרך כלל שלוותה בנוכחות חיסונית רבה יותר ובהישרדות טובה יותר. לאחר מכן הם בנו ציון סיכון המבוסס על 19 גנים הקשורים לקבוצה זו של תאי T, שיכל למיין חולי אדנוקרצינומה של הריאה לגידולים בסיכון נמוך, "חמים" חיסונית, ולגידולים בסיכון גבוה, "קרים" חיסונית.
גידולים קרים, אות מדכא ומטרה חדשה
גידולים בסיכון גבוה, כפי שהוגדרו על־פי ציון ה-ZNFRS הזה, הכילו פחות תאי חיסון מועילים ויותר תאי סרטן ותאים מיואידלים, תבנית טיפוסית של גידולים "קרים" העמידים לאימונותרפיה. כשבחנו החוקרים כיצד התאים בגידולים האלה מתקשרים זה עם זה, הם מצאו שאותות רבים זורמים מהתאים המיואידליים ומהתאי סרטן כלפי תאי T ותאי טבעיים הרג (NK). גורם מרכזי היה SPP1, חלבון מופרש שנע מתאים מיואידליים או תאי סרטן לקולטנים על תאי המערכת החיסונית. רשת האיתות של SPP1 הייתה חזקה בגידולים שלא הגיבו ובגידולים בסיכון גבוה, אך חלשה או חסרה בגידולים שהגיבו ובגידולים בסיכון נמוך, מה שמרמז ש-SPP1 מסייע ביצירת נישה מדכאת חיסון שמרחיקה תאי רוצחים או מפחיתה את פעילותם.
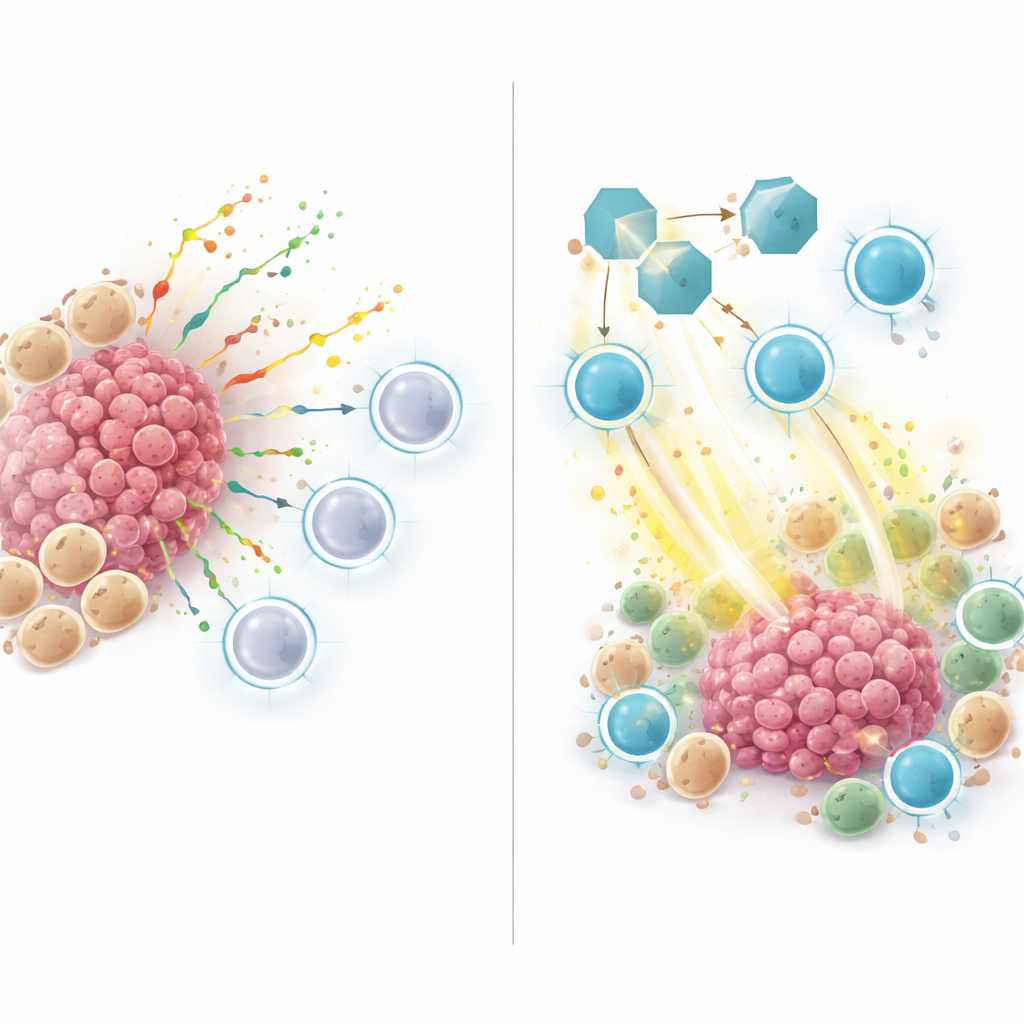
בדיקת חסימת SPP1 במודלים של בעלי חיים
כדי להתקדם מעבר לדפוסים בנתונים אנושיים, הצוות פנה למודלים של עכבר בסרטן ריאה. הם טיפלו בעכברים נשאי גידולים בנוגדן שחסם את SPP1, לבדו או בשילוב עם תרופת אימונותרפיה נגד PD-1. חסימת SPP1 לבדה האטה את גדילת הגידול, והקומבינציה עם אנטי-PD-1 הראתה את ההשפעה הטובה ביותר. תחת המיקרוסקופ ובניתוח תא-יחיד, גידולים בעכברים שטופלו בחסימת SPP1 הכילו יותר תאי CD8 פעילים המפיקים מולקולות טוקסיות המצחית תאי סרטן, ופחות מהמקרופאגים מסוג M2-like שבד"כ מקדמים גדילת גידול. במילים אחרות, עיכוב SPP1 העביר את המיקרו-סביבה ממצב מדכא למצב מופעל חיסונית.
מה זה אומר עבור טיפולים עתידיים
לקוראים כלליים, המסר המרכזי הוא שלא כל תאי המערכת החיסונית בתוך גידול הם שווים, וששכונת הסביבה יכולה לארח או לדחות אותם. המחקר מזהה סוג מיוחד של תאי רוצחים המקושר לאימונותרפיה מוצלחת בסרטן הריאה ובונה ציון מבוסס גנים המשקף עד כמה האקלים החיסוני של הגידול "חם" או "קר". הוא גם מדגיש את SPP1 כאות מזיק מרכזי המסייע לתאים להסתתר ממערכת החיסון. על ידי חסימת SPP1 בעכברים, החוקרים הצליחו להעיר תאי רוצחים ולשפר את יעילות האימונותרפיה הסטנדרטית. למרות שנדרשים ניסויים קליניים נוספים, ממצאים אלה מסמנים נתיב לפיתוח בדיקות דם ורקמות שיזהו מי הכי צפוי להרוויח מאימונותרפיה ומציעים טיפולים משולבים שעשויים להפוך גידולי ריאה עמידים לרגישים יותר להתקפה חיסונית.
ציטוט: Zhang, L., Zeng, J., Wen, J. et al. Multi-omics profiling reveals tumor microenvironment characteristics linked to immunotherapy response and prognosis in non-small cell lung cancer. npj Precis. Onc. 10, 179 (2026). https://doi.org/10.1038/s41698-026-01474-2
מילות מפתח: סרטן ריאות שאינו סוג תאי קטן, אימונותרפיה, מיקרו-סביבת הגידול, תאי CD8, איתות SPP1